2. Изучить, как влияет введение той или иной дозы предшественника на метаболическую активность клетки.
3. Обязательно учитывать радиационный эффект меченого соединения. Он может проявляться в довольно значительном изменении клеточных параметров.
4. Все, о чем говорилось выше, следует обязательно проверять при переходе к новому объекту изучения, так как существуют межтканевые и межвидовые различия в реакции клеток на одно и то же вещество.
Типы меченых соединений, используемых для введения метки в различные химические соединения, содержащиеся в тканях.
Нуклеиновые кислоты. Успехи радиоавтографии в изучении закономерностей клеточного цикла были получены во многом благодаря существованию 3Н – тимидина – предшественника синтеза ДНК, отвечающего большинству перечисленых требований.
Для клеток печени мышей показано, что 3Н-тимидин хорошо проникает в клетки, быстро включается в синтез имено ДНК (примерно через 15-20 минут после внутрибрюшинного введения). Невключившийся 3Н-тимидин деградирует до продуктов, которые не могут служить предшественниками синтеза ДНК, и уже через час выводится из организма в виде тритиевой воды. В умеренных концентрациях введенный 3Н-тимидин не влияет на параметры клеточного цикла (в клетки разных тканей тимидин проникает с разной интенсивностью и поэтому одинаковые дозы введения в организм еще не свидетельствуют об одинаковых концентрациях его в разных клетках). И, наконец, радиационный эффект 3Н-тимидина при кратковременных экспериментах незначителен.
Белки. Обычно для введения метки в новосинтезируемый белок в качестве предшественника используют какую-либо аминокислоту, например лейцин, в которую вводят 3Н. Для включения метки в новосинтезируемый коллаген прекрасным предшественником служит пролин, меченный 3Н, т. к. эта аминокислота входит в состав коллагена.
Углеводы. За синтезом гликогена можно проследить при помощи глюкозы, меченной 3Н. Если после иньекции меченой глюкозы радиоактивность регистрируется на контрольных срезах, но отсутствует на срезах, предварительно обработанных a - амилазой (фермент, расщепляющий гликоген), то обнаруженную радиоактивность можно отнести к этому полисахариду. Радиоактивность, сохраняющаяся в срезах после обработки их a - амилазой, обычно бывет обусловлена включением меченой глюкозы в гликопротеиды, протеогликаны, поскольку глюкоза может включаться в них так же, как и в гликоген.
Липиды. Синтез липидов можно изучать методом радиоавтографии, если предварительно ввести в организм или культуру меченый ацетат или другой подходящий предшественник.
Неорганические вещества. Фосфат кальция, отлагающийся в хряще или кости, можно пометить радиоактивными изотопами либо кальция (45Са), либо фосфора (32 Р). Железо, участвующее в образовании гемоглобина в процессе развития эритроцитов, можно пометить его радиоактивным изотопом (59Fe), что широко используется при изучении ряда болезней крови. В состав гормонов щитовидной железы входит йод, а поэтому можно проследить за синтезом этих гормонов, вводя в организм радиоактивный изотоп йода (131 I).
Распад изотопа с образованием ионизирующих частиц
Р а д о а к т и в н ы й р а с п а д представляет собой перегруппировку протонов и нейтронов в ядре нестабильного атома (изотопа), сопровождающуюся испусканием a-, b-частиц и g-лучей. Приод полураспада изотопа – одна из его характеристик:
14С - 5 700 лет 59Fe – 46 дней
3Н - 12,5 лет 32 Р – 14 дней
45Са - 164 дня 131 I - 8 дней
35 S - 87 дней
Период полураспада определяет время экспозиции препарата перед проявлением эмульсии. От него также зависит время работы с изотопом (коротко живущие изотопы 32Р, 131I нельзя хранить). Скорость распада необходимо также учитывать с точки зрения техники безопасности, так как при длительной работе с долго живущими изотопами растет опасность загрязнения лаборатории.
g-лучи характеризуются очень высокой проникающей способностью и соответственно низкой степенью ионизации, на регистрации которой основан метод радиоавтографии. g-излучение можно обнаружить только при прямом столкновении с электронами. Выброшенный с орбиты в результате такого столкновения орбитальный электрон может быть зарегистрирован как b-частица. Однако такое событие происходит крайне редко, и поэтому в радиоавтографии g - излучение практически не находит применения.
a- и b- частицы обладают рядом свойств (Табл. 2), которые удобны для регистрации. От массы частицы зависит форма трека, который она оставляет в фотоэмульсии. Тяжелые a - частицы дают прямолинейные треки, а значительно более легкие b - частицы при столкновении с атомными ядрами резко меняют направление и их треки имеют сложную неправильную форму.
Таблица 2
Характеристики излучения a- и b-частиц
Частица | Масса, е. м. | Заряд, е | Скорость | Энергия МэВ | Длина пробега | Относи- тельная иониза ция |
a | 4 | +2 | 0.1 С | 3 –11 | мкм | 10 000 |
b | 5,4 х10-4 | -1 | С | 0,01 – 4 | от мкм до мм | 100 |
a - частицы, испускаемые одним изотопом, имеют одинаковую энергию, в отличие от b - частиц, для которых характерен непрерывный энергетический спектр с максимальной энергией, присущей каждому изотопу. Для b - частиц 3H Еmax =18,5 кэВ, для 14С – 155 кэВ, для 32Р – 1,7 МэВ.
Относительная ионизация (I = e2/ v2), таким образом, у одного и того же изотопа будет одинаковой для всех a - частиц и различной для b - частиц.
Благодаря своей высокой ионизирующей способности a - частицы, проходя через эмульсию, образуют сотни пар ионов, активируя практически каждый кристалл галоидного серебра, с которым встречаются на своем пути. Поскольку на образование пары ионов тратится 33 эВ, то a - частица быстро теряет свою энергию и, таким образом, оставляемые ею треки будут короткими.
Низкая ионизирующая способность b - частиц приводит к тому, что они активируют далеко не каждый кристалл бромистого серебра (поэтому их треки будут состоять из редко расположенных зерен серебра); в результате энергия b - частиц теряется медленно, и следовательно, длина пробега b - частиц будет гораздо выше, чем у a- частиц.
Длина пробега и число образованных зерен серебра будут различны как у разных изотопов, так и среди b - частиц, испускаемых одним изотопом (Табл. 3).
Таблица 3
Изотопы | Длина пробега в эмульсии | Число образующихся зерен серебра |
3Н 14С 32Р | 1 – 2 мкм около 20 мкм несколько мм | 1 (редко 2) 5-6 (близко расположенные) десятки ( редко расположенные) |
Наилучшими для цитохимических целей характеристиками обладает тритий. Изотоп углерода применим для локализации веществ только в том случае, когда анализируются изолированные клетки и клеточные компоненты.
Фоторегистрация ионизирующих частиц
Регистрация a- и b- частиц достигается фотографическим способом, суть которого заключается в следующем. Фотоэмульсия представляет собой взвесь микрокристаллов галоидного (обычно бромистого) серебра в желатине. Микрокристаллы обладают дефектами в кристаллической решетке в виде скоплений ионов. Эти скопления называют центрами чувствительности. Электроны, образовавшиеся при ионизации, перемещаются в зоне проводимости кристалла и собираются в центрах чувствительности (которые оказываются своеобразными ловушками электронов). В результате создаются пары электрон-дырка-биполяроид, которые, в свою очередь, притягивают к себе ионы серебра. Таким образом, на месте центров чувствительности создаются зародыши кристаллов серебра (размером от нескольких десятков до нескольких сотен атомов) – это центры скрытого изображения.
Следующий этап – проявление эмульсии. Используют сильный восстановитель, который переводит бромистое серебро в металлическое с образованием бромистоводородной кислоты. Все ионы серебра могут быть восстановлены до атомов. Однако процесс восстановления идет гораздо быстрее в центрах скрытого изображения (чем больше центр, тем быстрее идет рост зерна серебра). Время проявления подбирается таким, чтобы видимые зерна серебра (их размер также зависит от времени проявления) сформировали только центры скрытого изображения, а размер зерен вне центра остался бы ниже разрешающей способности микроскопа.
Расположение кристаллов бромистого серебра и зерен металлического серебра полностью не совпадает, так как рост зерна серебра идет от центра скрытого изображения (центра чувствительности) в случайном направлении. Образовавшееся «зерно» серебра в электронном микроскопе выглядит в виде извитой ленты (Рис. 5). Как правило, проявленные зерна серебра в несколько раз крупнее кристаллов бромистого серебра.
Фиксация эмульсии проводится с использованием веществ, образующих с ионами серебра растворимое в воде соединение, которое вымывается из эмульсии при промывке препарата. В эмульсии остаются только желатин и зерна металлического серебра.
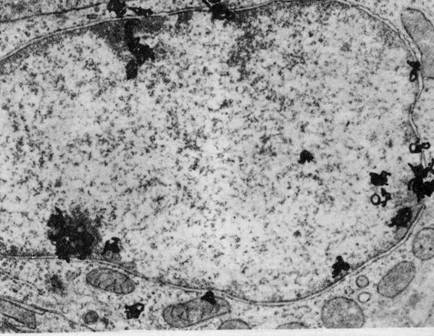
Рис. 5. Электронно-микроскопический радиоавтограф
интерфазной эпителиальной клетки из крипты тонкого кишечника мыши (х 9 500).
Эмульсии, применяемые в радиоавтографии, получили название ядерных (т. е. для регистрации ядерных распадов). Они отличаются от используемых в обычной фотографии меньшими зернами бромистого серебра (меньше 0.1 мкм, по сравнению с 0.5 – 1 мкм ) и их большей концентрацией в желатине (4:1, по сравнению с 1:1). Уменьшение размеров кристаллов бромистого серебра увеличивает разрешающую способность эмульсии, но снижает ее чувствительность, так как b - частица может «проскочить» мелкий кристалл, не успев вызвать в нем ионизацию.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 |



