Возможно, именно благодаря первым впечатляющим результатам количественная цитохимия долгое время развивалась как абсорбционная цитофотометрия нуклеиновых кислот, преимущественно ДНК. Только в последние десятилетия стали активно проводиться количественные исследования других компонентов клетки.
Спектрофотометрия
Спектрофотометрия связана с явлением поглощения света исследуемым веществом В основе абсорбционной фотометрии лежит закон Бугера-Бэра, устанавливающий экспоненциальное соотношение между поглощением монохроматического света и количеством поглощающего материала, через который проходит свет. В простейшей форме закон можно записать в следующем виде:
Ф = Фо. 10-kcd;
где Фo – световой поток, вошедший в среду; Ф – световой поток, успешно прошедший в среде с концентрацией вещества с и показателем поглощения k путь d.
Отношение величины светового потока, прошедшего через среду, к потоку, вошедшему в среду, называется пропусканием.
Пропускание можно установить, измеряя интенсивность светового потока, прошедшего через среду, -I и соотнося ее с интенсивностью светового потока, прошедшего рядом с измеряемым объектом – Io:
I/Io = Ф/Фо = 10 -kcd
Пропускание меняется от 0 до 1.
Логарифм пропускания, взятый с обратным знаком, называется оптической плотностью вещества (D):
D = lg I/Iо = - lgФ/Фо ; D = kcd
Оптическая плотность меняется от 0 (полное пропускание) до бесконечности (полное поглощение).
Если нужно определить массу вещества (m), а не его концентрацию, то вводим в формулу площадь поля (S), через которое проходит свет:
D = kcdS / S = km / S.
Если известен показатель поглощения k, то можно определить абсолютное значение массы вещества. Чаще всего показатель поглощения неизвестен, и поэтому определяется относительное количество вещества.
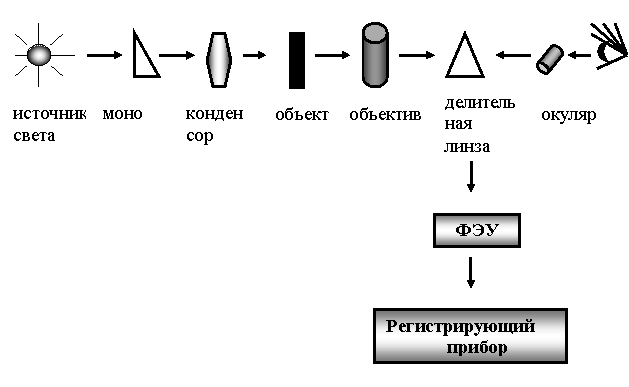
Принципиальная схема устройства цитоспектрофотометра показана на Рис.8. К постоянству источника света, к качеству монохроматора и линз микроскопа предъявляют очень жесткие требования.
Кроме фотоэлектрического существует и не получивший широкого распространения фотографический способ регистрации светового потока, при котором измерение переносится на увеличенную фотографию клетки, выполненную при освещении ее светом определенной длины волны. Предполагается, что степень почернения эмульсии соответствует плотности вещества в данном участке клетки. При всех легко обнаруживаемых недостатках фотографического способа у него есть и некоторые преимущества, например визуализация УФ - поглощения.
При адаптации спектрофотометрии, основанной на работе с гомогенными растворами, в специфике цитохимии обнаружились существенные трудности, связанные с неравномерным распределением веществ в клетке. Оказалось, что это приводит к значительным о ш и б к а м р а с п р е д е л е н и я.
При снижении оптической плотности ошибка распределения уменьшается. Однако прозрачные объекты дают большую ошибку за счет ошибки аппаратуры, т. е. сильно увеличивать прозрачность объекта нельзя. Существуют метды, позволяющие снизить ошибку распределения: плаг-метод, сканирвание, двухволновой метод.
|
Рис. 8. Схема устройства цитоспектрофотометра
П л а г-метод
Измерение оптической плотности проводят на относительно гомогенном «типичном» участке клетки и экстраполируют результат на всю площадь. При этом возникает ряд вопросов: насколько типичен выбранный участок; как подсчитать объем ядра, если оно не идеальной сферической формы; как учесть разную толщину препарата? Проблему «типичности» можно решить, измеряя несколько участков и усредняя результаты (м н о г о т о ч е ч н ы й метод). Ошибка плаг-метода и многоточечного больше 10 %.
Сканирование
Это планомерное измерение узким зондом всей поверхности объекта. Движение зонда может быть скачкообразным или нерерывным в зависимости от системы автоматического передвижения зонда и препарата относительно друг друга. Регистрация оптической плотности также автоматическая с последующим интегрированием. Ошибка метода сканирования около 1%. Ограничение применения сканирующих фотометров связано со сложностью приборов (катодно-лучевые трубки, подвижные диафрагмы), а также с тем, что на результаты измерения сильно влияют размеры зонда и толщина препарата.
Двухволновой метод
Измеряется среднее пропускание целого объекта (ядра, клетки), но делают не одно, а два измерения при разных длинах волн. Эти длины подбираются таким образом, чтобы соответствующие показатели поглощения соотносились определенным образом, например k1 = 2k2 или 2k1=3k2. Если длины волн подобраны с соблюдением этого условия, то можно сотавить систему из двух уранений с двумя неизвестными, которая успешно решается. Ошибка двухволнового метода обычно составляет 2-5%,
Еще одна трудность цитофотометрии связана с абсорбционными свойствами клеток. Собственным поглощением обладают лишь немногие клеточные компоненты, важнейшие из них (нуклеиновые кислоты и белки) – в УФ области спектра. Содержание циклических аминокислот в разных белках различно, поэтому цитофотометрия белков в УФ области не очень точна и развита слабо. Нуклеиновые кислоты находятся в преимущественном положении. УФ цитофотометрия в сочетании с методами дифференциальной экстракции успешно используется для дублирования цитофотометрических измерений в видимой области спектра.
Фотометрия в видимой области спектра – это в основном фотометрия красителей. На первое место здесь выступает специфичность красителей. Их немного: реактив Шиффа, прочный зеленый, соли тетразолия, проционовые красители и некоторые другие. Однако, встает вопрос, соответствует ли количество связавшегося красителя количеству вещества в клетке? Этот вопрос очень подробно изучен для комплекса ДНК-фуксин, образующегося при реакции Фельгена.
Оказалось, что содержание ДНК-фуксина зависит от очень многих условий. Прежде всего на него влияют в р е м я и у с л о в и я г и д р о л и з а. Оптимальным является такое время гидролиза, при котором выявляется максимальное содержание ДНК-фуксина. Подъем кривой гидролиза отражает процесс отщепления пуриновых оснований, а ее спад – деградацию ДНК.
На содержание ДНК-фуксина влияет п р о ц е с с ф и к с а ц и и; с п о с о б ы приготовления препаратов, использование разных предобработок. Различаются кривые гидролиза, проведенного в одних и тех же условиях, но для клеток разных тканей, а также для клеток одного и того же типа, но находящихся в различном функциональном состоянии.
Количественные методы все активнее внедряются в цитохимический анализ. Использование флуоресцентных красителей делает их применение возможным и для веществ, находящихся в клетке в небольших количествах. Однако применение флуоресцентных красителей для количественных оценок требует дополнительных контрольных процедур, учитывающих природу флуоресценции (тушение флуоресценции, невозможность измерения свечения внутренних слоев клетки, так как верхние слои работают как поглощающий фильтр).
Проточная цитофотометрия
Золотой век фотометрии начался с появлением проточного цитофотометра, во много раз увеличивающего скорость и точность измерительных процедур. Проточная цитофотометрия позволяет регистрировать сразу несколько клеточных параметров (например, содержание ДНК, размер клеток и их форму или общее содержание ДНК и содержание АТ - и ГЦ-богатых последовательностей). Можно получать одновременно до 6 характеристик. Это достигается применением светорассеяния под разными углами, возбуждением и флуоресценцией в двух длинах волн.
Одна из модификаций проточного цитофотометра позволяет сортировать клетки, обладающие разными свойствами. Возможность сортировки достигается быстротой анализа клеточных характеристик (с помощью компьютера) так, что на выходе из вибрирующей форсунки та капля, в которую попала клетка с заданными свойствами, заряжается положительно или отрицательно, а затем под действием электромагнитного поля отклоняется и попадает внужную пробирку. Одновременно происходит разделение на 3 фракции.
Если вместо клеточной суспензии взять суспензию хромосом, то можно успешно выделить определенные хромосомы, а затем использовать их для выделения ДНК с целью создания библиотек клонов ДНК, принадлежащей известным хромосомам.
Проточный микрофлуориметр (Рис. 9) анализирует клетки в суспензии в струе жидкости, которую пересекает луч лазера. Чтобы сконцентрировать клетки в центральной части струи и уменьшить
число агрегатов, способных забить выходное отверстие проточной камеры, используется техника тока обтекающей жидкости («рубашки»). Клетки по металлическому патрубку под давлением подаются в проточную камеру, которая промывается током обтекающей жидкости. Обтекающая жидкость с клетками выходит из камеры через апертуру, размер которой определяет диаметр выходящего потока жидкости. Частоту поступления клеток в обтекающую жидкость можно варьировать, меняя разницу в давлении между обтекающей жидкостью и вводимым образцом. Этот прием в сочетании с подбором концентрации клеток в образце позволяет создать такие условия, при которых каждая отдельная клетка последовательно проходит точку пересечения лазерного луча со струей жидкости (Рис. 9).
Источником света в проточных микрофлуориметрах служат лазеры, обычно аргоновые, но встречаются также гелий-неоновые и криптоновые. Лазеры служат источником высоко коллимированного (параллельные световые волны), монохроматического света большой интенсивности, который можно сфокусировать для передачи значительной энергии анализируемым клеткам. Как правило, аргоновые лазеры настраивают на длину волны излучения 488 нм, что обеспечивает

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 |