СПЕЦИАЛЬНОСТЬ: Общая медицина
КАФЕДРА: Биологическая химия
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ ДЛЯ ЗАНЯТИЙ
(практические, лабораторные)
КУРС: 2
ДИСЦИПЛИНА: БИОЛОГИЧЕСКАЯ ХИМИЯ
СОСТАВИТЕЛИ: ППС кафедры
Алматы, 2012 г.
Рассмотрено и одобрено на заседании кафедры биохимии
Протокол № ___ от «___» ______2012г.
Утвержден
Заведующий кафедрой биохимии,
профессор
Занятие №1
1. Тема: Правила техники безопасности
Белки Функции белков. Общие свойства белков: близкий элементарный состав, высокая молекулярная масса, большие размеры и определенная форма. Общая природа продуктов распада. Типы связей аминокислот в молекулах белков. Амфотерность белков. Цветные реакции на белки. Зависимость заряда белка от рН среды и аминокислотного состава.
2. Цели:
Сформировать правовые компетенции путём ознакомления с правилами техники безопасности. Сформировать знания о функциях и некоторых общих свойствах белков.3. Ввести новые понятия и термины
3. Задачи обучения:
Ознакомить с правилами техники безопасности при работе в биохимической лаборатории. Изучить функции белков. Изучить общие свойства белков: близкий элементарный состав белков, высокая молекулярная масса, большие размеры и определенная форма, общая природа продуктов распада и типы связей аминокислот в молекулах белков, амфотерность белков, цветные реакции на белки Стимулировать студентов к изучению профессиональной литературы и поиску информации в интернете. Ввести новые понятия: биологические функции белков – структурная, сократительная, защитная, ферментативная, регуляторная, электротрансформирующая; дисульфидная связь, гидрофобное взаимодействие неполярных групп, цветные реакции – общие реакции на белки и на отдельные аминокислоты, полноценные и неполноценные белки4. Основные вопросы темы:
5. Методы обучения и преподавания:
Устный опрос, выполнение упражнений, решение ситуационных задач, блиц-опрос, выполнение лабораторных работ, письменный опрос:разбор материала проводится по следующим вопросам:
Работа в малых группах – решение ситуационных задач:
Общая формула белка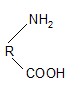
Какими свойствами обладает этот белок? Какой заряд он будет иметь при рН=4,7; 7,0; 10? Перечислите аминокислоты, входящие в состав такого белка.
Общая формула белка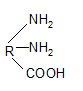
Какими свойствами характеризуется этот белок? В какой среде лежит его ИЭТ? Какой заряд он имеет в нейтральной среде? Какие аминокислоты входят в состав такого белка?
Общая формула белка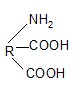
Какими свойствами характеризуется этот белок, при каких значениях рН он электронейтрален? Назовите аминокислоты, входящие в состав такого белка.
Блиц-опрос – проводится по тестовым заданиям или вопросам к блиц-опросу: студенту задается один вопрос, или преподаватель показывает тест и он сразу отвечает
6. Литература
Основная:
«Биохимия», 2007 г. стр10-17 “Биологическая химия” – Москва, 2004г., с. 16 - 59 , “Биологическая химия” – Москва, 2004г., с. 20-74Дополнительная:
Учебное пособие для самостоятельного изучения биохимии «Белки, ферменты, энергетический обмен, витамины», часть 1 – Алматы, 2009. “Биологическая химия” – Москва, 1986г., с. 24-51; 55-58. «Биохимия в схемах и рисунках», 2005г. “Биологическая химия”, Алматы, 2000, с. 85 – 134 , , Ерджанова по биохимии – Алматы, 20037. Контроль
Тестовые задания:
Какая из перечисленных групп аминокислот относится к моноаминомонокарбоновым: лейцин, валин, цистеин, аланин лизин, глутаминовая кислота, изолейцин аспарагиновая кислота, оксипролин, глицин, триптофан фенилаланин, цистеин, аргинин, лейцин метионин, серин, лизин, тирозин Какая из перечисленных групп аминокислот относится к циклическим: гистидин, пролин, валин, треонин изолейцин, серин, аргинин, оксипролин триптофан, тирозин, метионин, аспарагиновая кислота фенилаланин, гистидин, триптофан, тирозин метионин, фенилаланин, орнитин, лизин Незаменимые аминокислоты: содержат в своих молекулах разветвлённые радикалы синтезируются в животном организме не синтезируются в животном организме содержат в своём составе гетероциклы синтезируются в организме К незаменимым аминокислотам относятся: глицин, цистеин, аргинин глютаминовая, аспарагиновая кислоты триптофан, лизин треонин, валин, лейцин фенилаланин, изолейцин, метионинВыбрать соответствующую комбинацию:
Выбрать соответствующую комбинацию:
А, Б А, В Б, В Б, Г В, Д Какая из аминокислот активно участвует в процессах обезвреживания токсических продуктов обмена веществ:серин валин глицин лизин пролин В процессах метилирования участвует: аланин валин треонин метионин изолейцин Незаменимыми циклическими аминокислотами являются: тирозин фенилаланин гистидин триптофан пролин
Выбрать соответствующую комбинацию:
А, Б А, Д Б, В А, Г Б, Г Кислые свойства белкам придают аминокислоты: глицин глутаминовая кислота валин серин аспарагиновая кислотаВыбрать соответствующую комбинацию:
А, В Б, Г Б, Д А, Б Г, Д Основные свойства белкам придают аминокислоты: лизин валин глутаминовая кислота аспарагиновая кислота аргининВыбрать соответствующую комбинацию:
А, В Б, Г В, Д А, Д Г, ДВопросы:
Функции белков Общие свойства белков: близкий элементарный состав; высокая молекулярная масса; определенные формы белков и большие размеры; общие продукты распада; типы связей в молекуле белка и участие связей в молекуле белка для сохранения ее стабильности Цветные реакции на белки: общие реакции и на отдельные аминокислоты. Значение этих реакций в медицине Амфотерные свойства белков. Влияние рН среды на заряд белкаВопросы для блиц-опроса
Какие химические элементы входят в состав белков? Назовите продукты распада белков. Назовите ковалентные связи в молекуле белка. Назовите нековалентные связи в молекуле белка. Назовите 2-3 моноаминомонокарбоновые кислоты. Назовите гидрокси-аминокислоты Назовите серосодержащие аминокислоты. Назовите моноаминодикарбоновые кислоты. Назовите диаминомонокарбоновые кислоты. Назовите иминокислоты. Назовите ароматические аминокислоты. Перечислите гетероциклические аминокислоты. Какие аминокислоты называются заменимыми? Какие аминокислоты называются незаменимыми? Перечислите незаменимые аминокислоты. Какие аминокислоты относят к условно заменимым? Почему белки проявляют амфотерные свойства? От наличия каких функциональных групп в составе белковых молекул зависит их амфотерность? Какое состояние белка называется изоэлектрическим (ИЭС)? Что называется называется изоэлектрической точкой (ИЭТ)? Чему равна ИЭТ нейтрального белка? От каких факторов зависит заряд белка? Какие свойства (нейтральные, кислые, основные) будет проявлять белок, если в его составе преобладают МАМК? Какие свойства (нейтральные, кислые, основные) будет проявлять белок, если в его составе превалируют МАДК. Какие свойства (нейтральные, кислые, основные) будет проявлять белок, если в его составе преобладают ДАМК Назовите факторы устойчивости белка в растворе. Для каких целей используют общие цветные реакции? Для каких целей используют цветные реакции на отдельные аминокислоты?Занятие №2
1. Тема: Белки
Общие свойства белков: Коллоидные свойства. Реакции осаждения. Структуры белковых молекул. Классификация белков (простые и сложные). Простые глобулярные белки: представители, химические свойства, распространение в природе, роль
2. Цели:
Сформировать знания об общих свойствах белков Сформировать знания о денатурации, ренатурации, денатурирующих агентах. Формировать знания о классификации белков. Сформировать знания о простых глобулярных белках Ввести новые понятия и термины3. Задачи обучения:
Изучить общие свойства белков: коллоидные свойства, реакции осаждения, структуры белковых молекул. Дать понятия о денатурации, ренатурации, денатурирующих агентах. Ознакомить с классификацией белков. Ввести новые понятия: факторы устойчивости белка в растворе, реакции осаждения белков, денатурация и ренатурация белков, денатурирующие агенты, фракции глобулинов, электрофорез Рассмотреть структурную организацию белков, показать зависимость биологических свойств белка от первичной, вторичной, третичной, четвертичной структур. Изучить химические свойства, роль и распространение в природе альбуминов, глобулинов, протаминов и гистонов Стимулировать студента к изучению профессиональной литературы и поиску информации в Интернете.4. Основные вопросы темы:
1. Общие свойства белков:
Коллоидные свойства белков. Устойчивость белка в растворе, факторы устойчивости. Реакции осаждения и высаливание белков. Значение этих реакций в медицине.. Структуры белковых молекул. Денатурация, ренатурация.2. Классификация белков
3. Химические свойства альбуминов, глобулинов, протаминов и гистонов, роль и распространение в природе
5. Методы обучения и преподавания:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 |




