Получение ацидокомплексов в принципе сводится к взаимодействию соли одного металла с солью или кислотой другого, взятых в определенных соотношениях.
Аммиакаты и аминаты получают при взаимодействии аммиака или какого-либо органического амина с солью, а иногда с гидроксидом соответствующего металла.
Внутрикомплексные соединения — это вещества, в которых лиганд соединен с центральным атомом двумя связями.
![]() В качестве лигандов выступают вещества, содержащие определенные функциональные группы, обычно расположенные в молекуле рядом. Многие из лигандов обладают избирательным действием по отношению к определенным ионам или группе ионов. Например, на никель, висмут и кобальт специфическими группировками в органических веществах являются:
В качестве лигандов выступают вещества, содержащие определенные функциональные группы, обычно расположенные в молекуле рядом. Многие из лигандов обладают избирательным действием по отношению к определенным ионам или группе ионов. Например, на никель, висмут и кобальт специфическими группировками в органических веществах являются:
![]()
![]()
![]()
![]()
![]()
![]()
![]() — С— С— — NН—С— NН = N (S) С —N = O
— С— С— — NН—С— NН = N (S) С —N = O
![]() I ' I I
I ' I I
![]() НОN NОН SН С-ОН
НОN NОН SН С-ОН
Наиболее известными реагентами являются оксихинолин, диметилглиоксим, б-нитрозо-в-нафтол, купферрон и т. д. Внутрикомплексные соединения образуются при простом сливании растворов реактива и соответствующей соли металла.
Для осаждения комплексных соединений часто, применяют спирты — этиловый и пропиловый. Растворимость неорганических соединений, в том числе и комплексных, в системе вода — пропиловый спирт меньше. Поэтому для осаждения и промывки осадков следует отдать предпочтение пропиловому спирту.
ЛЕКЦИЯ 7
Методы очистки веществ
Для технических и научных целей в настоящее время необходимы особо чистые вещества, которые применяют в промышленности полупроводников и атомной промышленности, производстве люминофоров, некоторых жаропрочных и механически прочных материалов, производстве материалов для квантовой энергетики (лазеры) и т. д. Достаточно указать, что в важнейшем полупроводниковом материале Германии примеси меди и никеля не должны превышать 10-7%. До 1942 г. считали, что уран имеет температуру плавления, равную 1850 °С. После получения этого металла в чистом состоянии оказалось, что температура его плавления равна 1130 °С. Эти примеры показывают практическое значение очистки веществ. Необходимо отметить, что глубокой очистке подвергают уже довольно чистые вещества.
Существует несколько методов очистки веществ.
1. Транспортные химические реакции
Транспортными называются обратимые гетерогенные реакции, сопровождающиеся переносом исходного твердого или жидкого вещества из одной температурной зоны в другую в результате образования и разложения газообразных промежуточных соединений. Сущность метода очистки заключается в следующем.
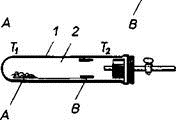
Рис. 22 Очистка веществ транспортными реакциями: 1- ампула; 2 — газ-переносчик; А - очищаемое вещество; В — очищенное вещество. |
В ампулу (рис. 22) помещают очищаемое вещество А, например никель, в ампуле имеется определенная концентрация газа-переносчика (галоген, кислород, пары воды и т. д.), в данном случае оксид углерода (II). Газ-переносчик при нагревании реагирует с очищаемым веществом с образованием летучего вещества, и за счет диффузии это вещество переносится в другой конец ампулы, где имеется другая температура. Там происходит разложение диффундирующего вещества. В приведенном примере при 50 — 80 °С (Т1) оксид углерода (II) вступает в реакцию с никелем с образованием карбонила Ni(СО)4:
Ni + 4CO = Ni(СO)4
В другом конце ампулы, имеющем температуру 180—200 °С (T2), тетракарбонил никеля разлагается. При этом выделяется очищенный никель, т. е. равновесие сдвигается в обратную сторону. Можно определить направление переноса вещества по знаку энтальпии реакции, т. е. на основании теплового эффекта. Если реакция образования газообразного вещества экзотермичная, а реакция разложения — эндотермичная, то вещество переносится в более горячую зону, которую называют зоной разложения. В противоположном случае вещество переносится в более холодную зону, где оно и разлагается.
так как при снижении температуры равновесие смещается в левую сторону.
Скорость переноса вещества зависит от многих факторов, важнейшие из них: термодинамика процесса, коэффициент диффузии газовой фазы, форма сосуда, расстояние между горячей и холодной зонами, давление в реакторе. Необходимо также учитывать химические свойства примесей в очищаемом веществе — они не должны реагировать с газом-носителем.
В настоящее время разработана количественная теория транспортных реакций и выведены уравнения, позволяющие почти количественно предсказать особенности транспорта конкретных веществ.
Существует несколько методов проведения транспортных реакций, отличающихся способом переноса веществ из одной зоны в другую.
В зависимости от температуры горячей зоны материалом является стекло (500—550 °С), тугоплавкое стекло (600—700 °С), кварц (1200—1300 °С). Длина ампул 15— 20 см, диаметр 1 —1,5 см. Ампулу закрывают пробкой с газоотводной трубкой, подключают к вакуумному насосу и отпаивают конец.
Другой конец должен немного выходить из печи и иметь температуру 50—80 °С. Иногда для соблюдения необходимого температурного режима нужно применять две электропечи. В упрощенном варианте данную реакцию можно проводить в пробирке, которая закрыта пробкой
2. Кристаллизация из расплава.
При медленном затвердевании вещества из расплава выделяются более чистые кристаллы, а примеси остаются в расплаве. Данное явление известно с глубокой древности и применялось на практике, например для вымораживания пресной воды из морской. Существует несколько вариантов этого способа глубокой очистки чистых веществ, например метод зонной плавки (рис. 24).
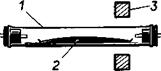
Рис. 24. Зонная плавка: 1 — трубка из кварца или тугоплавкого стекла; 2 — лодочка с очищаемым веществом; 3 — электропечь. |
Вещество в твердом виде помещают в лодочку, а ее помещают в кварцевую или стеклянную трубку, воздух вытесняют газом, он не должен взаимодействовать с очищаемым веществом. Лодочку нагревает электропечь, которую в течение 1,5—2 ч передвигают вдоль трубки. Тогда расплавленная зона медленно перемещается через твердое вещество. При этом большая часть примесей оказывается в расплаве. После окончания очистки последние затвердевшие порции вещества отбрасывают, так как примеси остаются в них.
Очистить вещество и получить его в виде монокристалла можно методом направленной кристаллизации. Для этого вещество плавят в пробирке, имеющей суженную часть (рис. 25). Среднюю и верхнюю часть ее обматывают асбестом для теплоизоляции. В пробирку помещают вещество в виде палочки или кусочков, его плавят и некоторое время выдерживают в расплавленном состоянии, чтобы оксиды всплыли на поверхность.
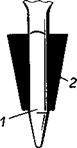 Рис. 25. Направленная кристаллизация:
Рис. 25. Направленная кристаллизация:
1 — очищаемое вещество; 2 — тепловая изоляция
Затвердевание постепенно распространяется на все вещество и заканчивается образованием монокристалла. Часть примесей переходит в верхнюю часть. Затем для отделения застывшего вещества пробирку разбивают. Для этого ее можно нагреть до 150—200 °С и опустить в холодную воду.
Этим методом можно очищать вещества, находящиеся при комнатной температуре в жидком состоянии, например многие хлориды (SnСl4, GeСl4, SiСl4 и др.) и другие соединения.
Зонная плавка может применяться также и для очистки солей, которые не разлагаются при плавлении. За ходом очистки можно следить, используя различные физические методы (электропроводность, твердость и т. д.), а также проводить анализ состава конца слитка и загрязненного.
3. Очистка водных растворов солей обработкой порошкообразными металлами, сульфидами или гидроксидами.
Равновесные состояния, возникающие при настаивании раствора соли с соответствующим металлом (например, раствора хлорида двухвалентного железа с железом), определяются окислительно-восстановительными потенциалами металла и его ионов. Чтобы установить, от каких примесей можно освободить соль, действуя на нее металлом, пользуются электрохимическим рядом напряжений. Восстанавливающийся металл выделяется на поверхности металла-очистителя и вместе с ним удаляется из раствора фильтрованием. Металл берут в виде порошка, фольги или в виде мелких гранул. Необходимое количество металла определяют характером примесей, их количеством и количеством очищаемой соли. На 100 г очищаемой соли вполне достаточно взять 0,5 г металла. Наиболее эффективна очистка этим методом солей активных металлов (магния, цинка, кадмия, алюминия и др.), так как в этом случае могут быть удалены из раствора ионы многих металлов. Остающееся количество посторонних ионов ориентировочно можно определить, используя уравнение Нернста.
В реальных условиях имеются отклонения от электрохимического ряда напряжений, связанные с пассивированием металлов и с другими причинами. Поэтому в некоторых случаях отдельные члены этого ряда могут менять свое место. Так, алюминий не выделяет металлов из раствора их нитратов, в то время как из растворов хлоридов алюминий осаждает большое число металлов.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 |