Проведение опыта. Зажигательную смесь поджигают при помощи магниевой ленты. Если имеются магниевые стружки, то можно поджечь магний и бросить его на зажигательную смесь.
Разделение продуктов реакции. После окончания реакции тигель охлаждают, разбивают и «королек» металла отделяют от шлака. Иногда кусочки металла остаются в шлаке в виде включений. В этом случае шлак нужно разбить и отделить от него металл; кусочки шлака, приставшего к металлу, удаляют с помощью молотка на стальной плите.
Выход продуктов реакции. Выход продуктов реакции в лабораторных условиях в лучшем случае составляет 80—90% от теоретического. Чаще он составляет 60—70%. Выход в значительной степени определяется чистотой отделения металла от шлака, в котором металл часто остается в виде мелких трудноотделимых включений.
Получение металлов и неметаллов восстановлением водных растворов солей
Электрохимические методы
Электролиз используется для получения электролитических покрытий металлов и для осаждения металла в виде порошка. Плотные мелкокристаллические осадки, прочно сцепленные с катодом, выделяются из электролитов, содержащих металл в составе комплексного иона. Металлы в порошкообразном состоянии образуются при больших плотностях катодного тока. В этих условиях в прикатодном слое электролита мало ионов металла, поэтому на катоде выделяется и водород.
Электролиз в каждом конкретном случае проходит при определенной разности потенциалов на электродах, которая называется напряжением разложения. Оно равно разности скачков потенциалов на электродах (в В), к которой необходимо прибавить значение омического падения напряжения в электролите:
I·l
 U =
U =
ч·S
где I — сила тока (в А), идущего через электролизер; l — расстояние между электродами (в м); ч — удельная электрическая проводимость электролита (в Сименс(См)/м); S — поверхность электрода (в м2).
Скачок потенциала на отдельном электроде вычисляется по уравнению Нернста.
RT
 E = E0 + lna
E = E0 + lna
nF
где Е – электродный потенциал Ме; Е0 – электродный потенциал при концентрации с или активности а, равной 1; R – универсальная газовая постоянная; F – постоянная фарадея; n – зарядность иона Ме; Т – температура.
Полученное значение называется равновесным потенциалом и относится к неработающему электроду. Потенциал работающего электрода (электрода, на котором идет электродный процесс) всегда больше равновесного вследствие поляризации. Поляризацией называется отклонение потенциала электрода от равновесного значения. Потенциал работающего электрода меняется в зависимости от силы тока. Эта зависимость, выраженная графически, называется поляризационной кривой. Чем круче поднимается поляризационная кривая (более сильно меняется потенциал электрода от плотности тока), тем меньше поляризация.
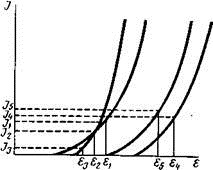
На основании поляризационных кривых можно определить условия («потенциал — плотность тока»), при которых будет выделяться одно вещество из смеси двух веществ или одновременно два вещества. На рисунке 5 приведены поляризационные кривые четырех веществ: А, В, С и D. Потенциалы выделения веществ А и В близки. При потенциале Е1 и силе тока I1 будет выделяться только одно вещество В. Если же потенциал и силу тока уменьшить до E1 и I2, то будут одновременно выделяться два вещества. При потенциале Е3 и силе тока I3 начнет выделяться вещество А. Поляризация электродов при выделении веществ В и С происходит примерно в равной степени, так как наклон поляризационных кривых по существу одинаков. Но выделяются на электродах эти вещества при разных потенциалах, например при Е4 и Е5, поэтому их легко разделить электролитическим методом. Однако в соответствии с уравнением Нернста равновесный потенциал электрода в процессе электролиза при уменьшении концентрации разряжающегося иона становится более отрицательным. Поэтому в процессе электролиза потенциалы выделения двух металлов могут сближаться. В электролит часто вводят различные добавки, изменяющие структуру осадков, улучшающие рассеивающую способность ванны и т. д. К добавкам относятся комплексообразователи.
А В С D |
Некоторые металлы не удается выделить электролизом водных растворов. Это металлы, обладающие большим отрицательным потенциалом (щелочные, щелочноземельные), а также металлы, на которых имеется небольшое перенапряжение водорода (ванадий, ниобий, тантал, титан, цирконий).
Рис. 5. Поляризационные кривые. |
|
А Б
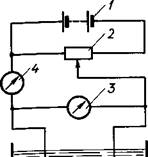
Рис. 6. Схема включения электролизеров: 1 — источник постоянного тока; 2 — реостат; 3 — вольтметр; 4 — амперметр.
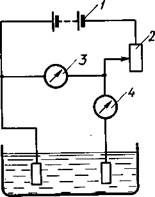
В определенных условиях они осаждаются на электроде тончайшим слоем, но затем процесс прекращается вследствие выделения на них водорода. Практически в лабораторных условиях электролиз проводят в стеклянных электролизерах или в самодельных электролизерах, изготовленных, например, из органического стекла (стеклянные ванны прямоугольной формы). Могут быть две схемы (А и Б) включения электролизера (рис. 6). Реостат 2 должен иметь достаточное сопротивление, особенно в случае А. Источником тока служит батарея аккумуляторов или выпрямиИзменяя сопротивление реостата, можно регулировать напряжение и силу тока, которые измеряются вольтметром 3 и амперметром 4. Плотность тока взаимосвязана с омическим сопротивлением ванны и напряжением. Практически плотность тока регулируется изменением подаваемого напряжения. При значительной плотности тока и при большом сопротивлении электролита напряжение может достигать 20—30 В. Для уменьшения сопротивления ванны рекомендуется расстояние между электродами делать меньше. Если электролиз проводят при повышенной температуре, ванну обогревают термостатом или в электролит помещают змеевик, через который пропускают горячую воду. Более удобны для питания электролизеров выпрямители с регулируемым напряжением, в которые вмонтированы вольтметр и амперметр. Согласно закону Фарадея определяют массу вещества, выделившегося при электролизе. За счет побочных реакций выход вещества от теоретически возможного обычно составляет 90—95%, а при выделении хрома 40—30% и ниже.
2. Восстановление веществ порошкообразными металлами, амальгамами и другими восстановителями
Возможность восстановления ионов металлов или неметаллов другими металлами может быть определена по уравнению Нернста. Для качественной оценки можно пользоваться рядом напряжений, составленным на основе стандартных электродных потенциалов окислительно-восстановительных систем.
При получении металлов восстановлением их ионов более активными металлами необходимо учитывать следующее:
1. Разность в электродных потенциалах восстанавливаемого металла и металла-восстановителя. Чем больше эта разность, тем легче идет процесс восстановления. Если использовать такие активные восстановители, как щелочные и щелочноземельные металлы, то в растворах наряду с ионами металлов восстанавливаются ионы водорода и образуются щелочи. Поэтому наиболее часто в качестве восстановителей используют цинк, кадмий или алюминий. Для восстановления меди, ртути и других подобных металлов можно воспользоваться железом.
2. Крупинки восстановителя должны быть мелкими (1 — 2мм). С большими крупинками реакция идет медленно. Они покрываются выделяющимся металлом, через который диффундируют ионы восстанавливаемого металла и металла-восстановителя.
3. Наличие оксидных пленок на поверхности восстановителя. Эти пленки имеются практически на всех металлах. Они с разной скоростью растворяются в слабокислых растворах солей, но существенного влияния на скорость взаимодействия металлов с растворами солей не оказывают. Для получения металлов таким способом к раствору соответствующей соли, взятой в избытке, добавляют металл-восстановитель. Раствор взбалтывают и оставляют на несколько часов или дней. Затем порошкообразный осадок отфильтровывают, промывают водой, спиртом и высушивают. Полученные металлы (медь, серебро, платиновые металлы) желательно промыть разбавленной кислотой.
Амальгамы, например, щелочных и щелочноземельных металлов обладают более сильными восстановительными свойствами. Но при недостатке в приэлектродном слое ионов металла восстанавливаются ионы водорода, в растворе образуется свободная щелочь, под действием которой ионы многих металлов дают осадки гидроксидов. Этот метод применим и для получения растворов или осадков солей металлов, находящихся в низшей степени окисления (например, Fе+2, Сr + 2, V+3, Мо+3 и т. д.):
2CrCl3 + Zn = ZnCl2 + 2CrCl2
Значительным неудобством метода является то, что соль получается в смеси с другой солью. Поэтому желательно в качестве восстановителя брать металл, однотипный с восстанавливаемым ионом, например:
Сu + СuС12 = 2СuС1
Fe + 2FeCl3 = 3FeCl2
В подобных случаях выделение соли не представляет трудностей. Многие соли металлов, находящихся в низшей степени окисления, а также некоторые металлы и неметаллы можно получить, используя в качестве восстановителей такие вещества, как гидразин, гидроксиламин, сернистую и щавелевую кислоты. В препаративном отношении одним из лучших восстановителей является гидразин. Он обладает не только высокими восстановительными
свойствами, но при его использовании не образуется побочных продуктов, мешающих синтезу:
2J2 + N2H4 = 4HJ + N2
ЛЕКЦИЯ 4
Хлорирование металлов, неметаллов и оксидов
1. Хлорирование металлов и неметаллов хлором
При выборе конструкции установки для хлорирования необходимо учитывать: 1) физические и химические свойства исходного вещества и получаемого хлорида; 2) чистоту хлора; 3) количество получаемого хлорида.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 |