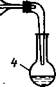Реакции хлорирования протекают при нагревании и с выделением значительных количеств теплоты. Поэтому, если хлор подают в реактор с равномерной скоростью и в нужном количестве, процесс протекает автотермично и подогревать вещество нужно только в начале реакции. Многие исходные вещества (сера, селен, цинк, кадмий, алюминий) плавятся, поэтому их следует помещать в реактор для хлорирования в лодочках. Если же вещество помещается без лодочки, то нужно обеспечить горизонтальное положение реактора, чтобы расплавленное вещество не вытекало из реактора.
Получаемые хлориды при температуре хлорирования могут испаряться или находиться в твердом или жидком состоянии, что влияет на скорость реакции. Испаряющиеся хлориды (ZnCl2, СdСl2, FеС13, А1С13) током хлора уносятся из реакционного пространства и конденсируются на более холодных стенках прибора. Если же хлорид получается в твердом (СоС12, NiС12 и т. д.) или жидком состоянии (МnС12), то он будет покрывать поверхность хлорируемого металла и замедлять реакцию хлорирования.
При давлении 1 кПа испарение хлоридов идет с небольшой скоростью, поэтому возгонку можно вести в этих условиях. При 10 кПа возгонка идет со значительной скоростью. В этом случае над хлорируемым веществом можно пропускать сильный ток хлора. Испарение хлоридов позволяет отделять продукт реакции от исходного вещества. Этим методом можно получать и плохо испаряющиеся хлориды, например хлорид МnCl2, который кипит при 1231 °С.
Оксидные пленки, имеющиеся на поверхности металлов, в большинстве случаев хлорированию не подвергаются. Следовательно, они могут загрязнять получаемый хлорид, если он не возгоняется из реакционного пространства. К. тому же они замедляют процесс хлорирования. При наличии в хлоре кислорода и паров воды эти примеси могут вступать в реакцию с хлорируемым веществом и давать оксиды. В этих случаях хлорирование веществ, обладающих большим сродством к кислороду (кремний, бор, хром) и дающих плотные оксидные пленки, сильно замедляется. В то же время хлорирование протекает при комнатной температуре, если хлор идеально чист и вещества не содержат оксидных пленок. Например, при размалывании кремния и бора в атмосфере чистого хлора хлориды легко образуются и без нагревания.
В зависимости от свойств исходных и конечных веществ для хлорирования применяют различные установки. Вещества, дающие жидкие и легкокипящие хлориды (фосфор, сера, селен, теллур, олово и др.), хлорируют в приборе (рис. 7). Для этого 5—10 г вещества помещают в трубку из тугоплавкого стекла, вытесняют хлором воздух и подогревают трубку газовой горелкой до начала реакции, что заметно по выделению теплоты и образованию своеобразного тумана. Размеры прибора и особенно размеры холодильника и приемника выбирают в соответствии с навеской хлорируемого вещества.
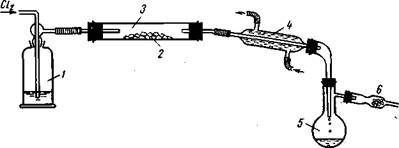
Рис. 7. Получение легкокипящих хлоридов:
1 — счетчик пузырьков с концентрированной серной кислотой; 2 — хлорируемое вещество; 3 — трубка из обычного стекла; 4 — холодильник; 5 — приемник; 6 — хлор-кальциевая трубка.
ХЛОР
|
|
|
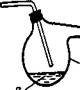
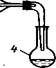
Рис 8. Получение легкокипящих хлоридов хлорированием легкоплавких металлов или неметаллов:
1 - реактор; 2 — расплавленные металл или неметалл; 3 — холодильник; 4 — приемник.
При небольшой навеске они должны быть небольшими, так как часть продукта остается на стенках холодильника и приемника. Желательно отдельные части прибора соединять на шлифах.
Для получения легкокипящих хлоридов, например хлоридов олова, серы, удобна установка, приведенная на рисунке 8.
Хлориды, которые возгоняются при температуре 100—350 °С (FеС13, А1С13, СdС12, ZпС12), получают в приборе (рис. 9). Хлорируемое вещество 2 помещают в первое колено трубки для хлорирования 3. После вытеснения из системы воздуха хлором вещество в трубке нагревают газовой горелкой и, продолжая пропускать хлор, проводят хлорирование. Хлорид собирается во втором колене трубки. После окончания хлорирования продукт перегоняют в слабом токе хлора в третье колено трубки, что позволяет получить его в более чистом виде. Для возгонки вещества нагревают соответствующее колено трубки. Необходимо следить, чтобы продукт не скапливался в узких местах трубки.
Рис. 9. Получение легковозгоняющихся хлоридов:
-счетчик пузырьков с серной кислотой; 2 — хлорируемое вещество; 3 — трубка для хлорирования; 4 — место запаивания продукта.
Затем прибор разбирают, трубку с веществом быстро закрывают пробками для предупреждения попадания влаги, воздуха и запаивают его во втором и третьем коленах.
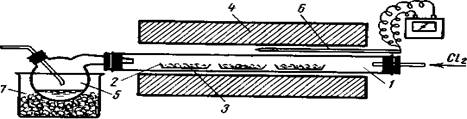
Рис. 10. Получение больших количеств легковозгоняющихся хлоридов:
1 — фарфоровая или кварцевая трубка; 2 — лодочки; 3 — хлорируемое вещество; 4 — электропечь; 5 — приемник хлоридов; 6 — термопара; 7 — охладительная смесь.
Большие количества легковозгоняющихся хлоридов удобно получать в приборе, схема которого приведена на рисунке 10. Хлорирование проводят в фарфоровой или кварцевой трубке 1, куда помещают в лодочках 2 вещество 3. Трубку нагревают электропечью 4. Получаемый хлорид током хлора уносится в приемник 5, который изготовляют из реторты. Его полезно охлаждать холодной водой. Температура контролируется термопарой 6.
Если работу проводят не под тягой, то следы непрореагировавшего хлора попадают в помещение. В этом случае желательно иметь установку, имеющую на выходном конце поглотитель (рис. 11). Поглотительную колонку 4 заполняют битым стеклом или нарезанными трубками, которые смачивают разбавленным раствором щелочи. Чтобы при возможных перерывах при подаче хлора влажный воздух не попадал в реакционную трубку, в систему включают U-образную трубку 3, наполненную хлоридом кальция.
Хлор, получаемый в лабораторных условиях окислением хлороводородной кислоты перманганатом калия или оксидом марганца (IV), содержит кислород и пары воды.
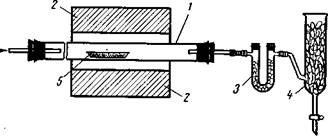
Рис. 11. Прибор для получения неиспаряющихся хлоридов с поглотителем хлора:
1 — фарфоровая или кварцевая трубка; 2 — электропечь; 3 — поглотительная трубка с хлоридом кальция; 4 — поглотительная колонка с раствором щелочи; 5 — лодочка с хлорируемым веществом.
Примеси этих веществ окисляют алюминий, титан, цирконий, кремний, бериллий, бор и т. д. Поэтому хлориды загрязняются оксидами. Следовательно, для получения чистых хлоридов необходимо или хлор подвергать специальной очистке, или хлориды отгонять из реакционного пространства. Для очистки хлора от кислорода его пропускают через раскаленную трубку, наполненную углем. Некоторые оксиды, например меди, свинца, кобальта, никеля, щелочных и щелочноземельных металлов, сравнительно легко превращаются в хлориды. Поэтому при хлорировании этих металлов хлор можно не очищать от кислорода.
2. Хлорирование металлов и неметаллов хлороводородом
Хлорирование металлов и неметаллов сухим хлороводородом протекает более спокойно, чем с хлором. Поскольку реакции идут с выделением водорода
Fe + 2HCl = FеС12 + H2
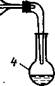
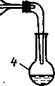
хлориды всегда получаются в низшей степени окисления. Поэтому данный метод удобен для получения CrCl2, FеС12, SnС12, SbС13 и некоторых других хлоридов. При использовании хлороводорода в отличие от хлора процесс идет, как правило, при более высоких температурах. Хлорирование проводят в фарфоровых или кварцевых трубках, куда помещают лодочку с исходным веществом (рис. 1.), или в трехколенных стеклянных трубках (рис. 2) . Хлорид остается в лодочке или возгоняется и конденсируется на холодных стенках трубки. Собирать его в том и в другом случае трудно. Для этого после охлаждения трубки лодочку быстро вынимают металлическим крючком, трубку устанавливают вертикально и, подставив к нижней ее части приемник (широкую пробирку и др.), быстро проталкивают возгон в приемник металлическим прутом.
3. Хлорирование оксидов
Хлорирование оксидов — процесс обратимый: 2МеО + 2С12 = 2МеС12 + О2
Поскольку эта реакция гетерогенная, состояние равновесия определяется соотношением концентраций хлора и кислорода в газовой фазе:
Кр = [O2]/[Cl2]2
Следовательно, действуя избытком чистого хлора на оксид, можно и сместить процесс в сторону образования хлорида. Однако при таком методе хлорирования значительная часть хлора будет расходоваться непроизводительно.
Хлориды многих элементов при 25 °С более устойчивы, чем оксиды. Оксиды щелочных и щелочноземельных металлов под действием хлора легко переходят в хлориды. В состоянии равновесия при высоких температурах в газовой фазе находится большое количество кислорода и незначительное количество хлора. Оксиды бора, кремния, бериллия, алюминия, титана и некоторых других элементов хлорируются с трудом. Практически хлорирование этих оксидов проводят в присутствии кислородотнимающего агента, облегчающего смещение равновесия в сторону образования хлорида. Из них наиболее удобно применять уголь. При хлорировании оксидов уголь окисляется главным образом до оксида углерода (II), который с хлором (при его избытке) дает фосген. Если хлор пропускать медленно через смесь оксида с избытком угля, то содержание фосгена в отходящих газах уменьшается, а содержание оксида углерода (II) увеличивается. Такие равновесные реакции с участием углерода изучены, и в некоторых случаях даже определены их константы равновесия. Уголь удобен для практического применения не только потому, что при его окислении образуются газы, легко выводимые из сферы реакции, но еще и потому, что углерод практически не хлорируется (в отличие от других веществ, отнимающих кислород).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 |