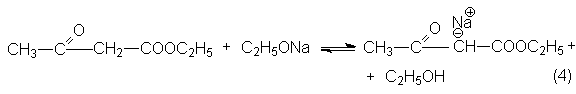
Очевидно, что продукт конденсации необходимо получить из соли енола и выделять в условиях, предотвращающих обратную реакцию распада на исходные реагенты. Наилучшим методом оказывается "замораживание" реакционной смеси для чего ее вливают в избыток холодной кислоты.
Для протекания конденсации Кляйзена необходимы следующие структурные предпосылки: исходный эфир должен иметь водородный атом при α - углеродном атоме, чтобы могли осуществиться реакции, представленные в механизме (реакции (1)-(3)) и два водородных атома при α - углероде, для того чтобы оказалось возможным смещение равновесия реакции в сторону продукта за счет образования енолят-аниона ацетоуксусного эфира.
Очевидно, что этилизобутират не вступает в присутствии этилата натрия в реакцию автоконденсации, поскольку в продукте конденсация отсутствует α - водородные атомы.
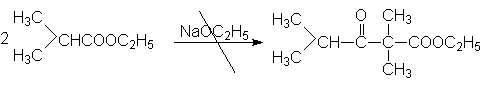
Конденсация Кляйзена может быть проведена между двумя сложными эфирами, но поскольку при этом возможно образование четырех различных продуктов, в результате реакции часто получают сложные смеси. Этого удается избежать, если один из сложных эфиров не содержит α - водородных атомов и легко реагируется с карбанионом. Реакции в этом случае напоминают перекрестную альдольную конденсацию. К числу применимых для этой цели сложных эфиров, не содержащих α - водородные атомы и обладающих высокой реакционной способностью относятся эфиры бензойной, муравьиной, щавелевой и угольной кислот.
Примеры: 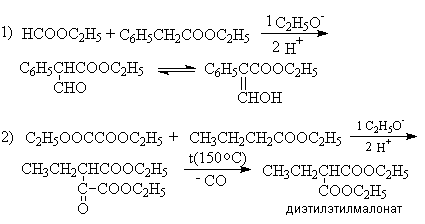
Лекция № 13-14. Реакции ароматических соединений. Правила ориентации.
Реакции ароматических карбонильных соединений подобны превращениям их алифатических аналогов. Однако необходимо отметить следующие особенности:
- карбонильные соединения аренов обладают более низкой реакционной способностью по отношению к нуклеофильным реагентам; аренкарбальдегиды и диарилкетоны не способны к енолизации; возможны реакции электрофильного замещения в ароматическом кольце.
а) Бензоиновая конденсация
При нагревании в присутствии цианидов аренкарбальдегиды образуют α - гидроксикетоны (бензоины).
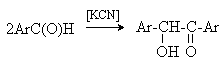
Механизм реакции:
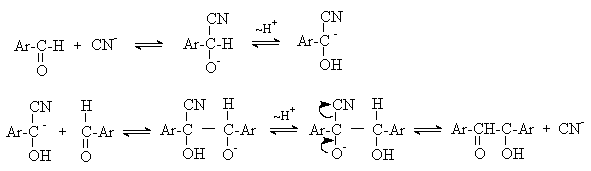
Ключевая стадия процесса – образование карбаниона за счет миграции протона от атома углерода к атому кислорода, которая становится возможной благодаря электроноакцепторному действию цианогруппы.
б) Реакция Канницаро
Аренкарбальдегиды, как альдегиды, не содержащие α - водородных атомов, вступают в реакцию Канницаро.
2ArC(O)H + NaOH → ARCOONa + ARCH2OH
Подробнее см. лек.№31-33.
в) Реакция Перкина
Аренкарбальдегиды конденсируются с ангидридами карбоновых кислот в присутствии оснований (ацетатов и карбонатов щелочных металлов, пиридина). При этом альдегид выполняет роль карбонильной, а ангидрид – метиленовой компоненты.
![]()
Механизм реакции:
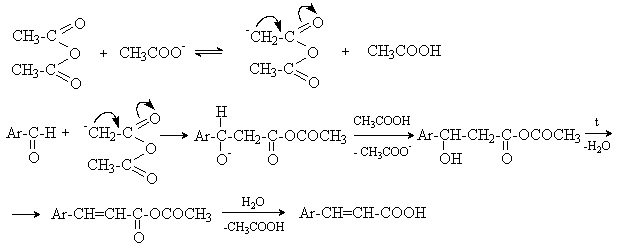
г) Автоокисление
Аренкарбальдегиды очень легко окисляются кислородом воздуха на свету.
ArCHO + 1/2O2 → ArCOOH
Процесс протекает по свободнорадикальному механизму через промежуточное образование стабильных ароильных радикалов Ar-C. =O.
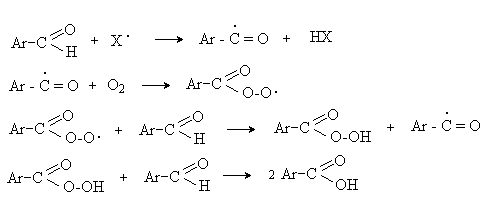
д) Хлорирование
Аренкарбальдегиды легко хлорируются по свободнорадикальному механизму с образованием хлорангидридов.
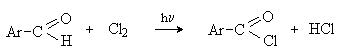
Механизм:
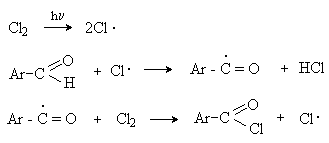
Важнейшие представители
Бензальдегид – бесцветная жидкость с запахом горького миндаля. Получают из толуола прямым окислением или хлорированием до бензальхлорида с последующим гидролизом. Как альдегид, не содержащий α - водородных атомов, бензальдегид выступает в реакциях конденсации в качестве метиленовой компоненты. При конденсации его с ацетальдегидом образуется коричный альдегид:
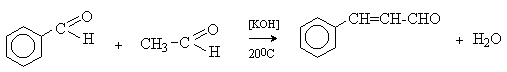
а при конденсации с с ацетофеноном – халкон:
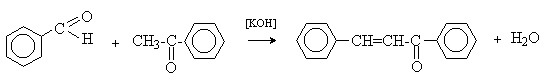
Коричный альдегид обладает свойствами α,β-непредельных карбонильных соединений. Используется в парфюмерии и пищевой промышленности.
Бензофенон – бесцветное кристаллическое вещество. В промышленности его получают окислением дифенилметана. Для бензофенона характерно образование стабильного анион-радикала синего цвета при взаимодействии с металлическим натрием.
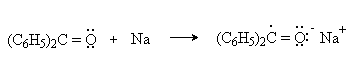
Такие анион-радикальные соли называют металлкетилами. Их относительная устойчивость связана со стабилизирующим влиянием на свободнорадикальный центр двух бензольных ядер и отрицательно заряженного атома кислорода.
Дибензоил – желтое кристаллическое вещество. Образуется при окислении бензоина.
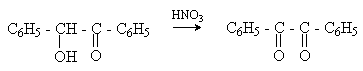
При нагревании со спиртовым раствором щелочи дибензоил претерпевает перегруппировку с образованием бензиловой кислоты (бензиловая перегруппировка).
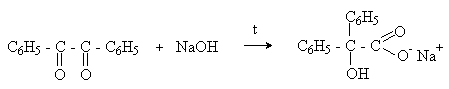
Механизм:
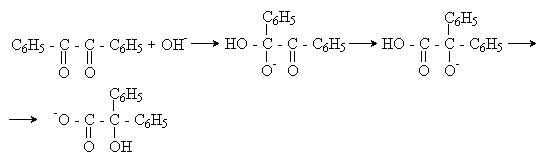
Лекции №19-22. Реакции диазотирования.
ДИАЗОСОЕДИНЕНИЯ
Вопросы.
Ароматические диазосоединения. Алифатические диазосоединения.Диазосоединения содержат группу N2, причем один атом азота связан с органическим радикалом, а другой - с гетероатомом. Ароматические и алифатические диазосоединения сильно различаются по строению, стабильности и реакционной способности.
1. Ароматические диазосоединения
Классификация и номенклатура
Ароматические диазосоединения имеют общую формулу ArN2X. В зависимости от типа связи между фрагментамиArN2 и X различают следующие типы диазосоединений.
Соединения, содержащие ионную связь (соли диазония):
ArN2+X-
X - – анион сильной кислоты с низкой нуклеофильностью, в том числе комплексный ион (Cl-, Br - HSO4-, BF4-, SbF6-, PF6-), например:

Соединения, содержащие ковалентную связь:
Ar-N=N-X
X= - CN, - OCOCH3, - I, - SO3H, - OH, - OAr, - NH-Ar
Например:
C6H5-N=N-CN | C6H5-N=N-OH | C6H5-N=N-O - Na+ |
бензолдиазоцианид | бензолдиазогидроксид | бензолдиазотат натрия |
Основной тип ароматический диазосоединений – соли арендиазония.
Методы получения солей арендиазония
Основной метод получения солей арендиазония – диазотирование. Процесс диазотирования выражается следующим суммарным уравнением.
ArNH2 + NaNO2 + 2 HX → ArN+=N X - + NaX + 2 H2O
(X= Cl, HSO4, BF4 и др.)
Механизм реакции диазотирования
Механизм включает cтадии нитрозирования амина. Нитрозирующими агентами являются соединения общей формулы O=N-X. Сама азотистая кислота (X=OH) является слишком слабым электрофильным реагентом, поэтому для ускорения процесса требуется присутствие сильной кислоты, в водном растворе которой азотистая кислота частично протонируется с образованием очень активного электрофильного агента - нитрозацидий-катиона:
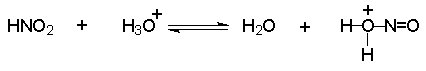
Этот катион гораздо быстрее реагирует с неорганическими анионами, присутствующими в растворе, чем с амином. В результате образуются новые нитрозирующие реагенты: азотистый ангидрид, хлористый или бромистый нитрозил.
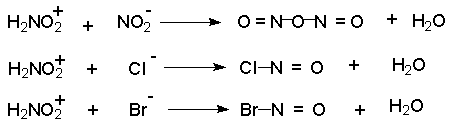
В разбавленных водных растворах серной, фосфорной, хлорной и других кислот с малонуклеофильными анионами нитрозирующим агентом является азотистый ангидрид N2O3 . При диазотировании в растворах HCl и HBr электрофильными агентами являются соответственно NOCl и NOBr. В сильно кислой среде активной частицей является, вероятно, катион H2NO2+. Наиболее активный нитрозирующий агент - нитрозилсерная кислота получается при взаимодействии нитрита натрия с концентрированной серной кислотой.
2 H2SO4 + NaNO2 --- O=N-OSO3H + NaHSO4 + H2O
Диазотирование всегда проводят в кислой среде, где протолитическое равновесие сильно смещено вправо.
![]()
Тем не менее диазотированию подвергается амин в виде свобoдного основания.
Механизм диазотирования включает образование нитрозамина, таутомерное превращение его в диазогидроксид, протонированная форма которого отщепляет молекулу воды с образованием катиона диазония.
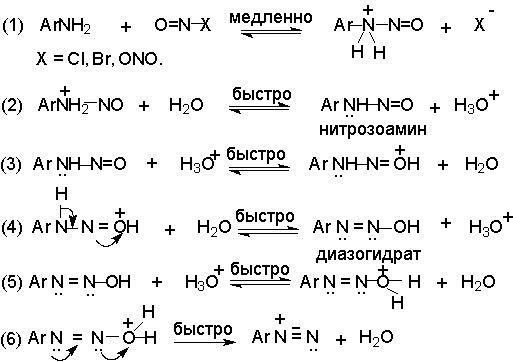
Лимитирующей стадией процесса является образование катиона N-арилнитрозоаммония. Далее следует ряд быстрых протолитических равновесий. На стадии (4) происходит отщепление протона от азота или кислорода, поскольку исходный катион формально является аналогом аллильного катиона. Депротонирование кислорода приводит к исходному субстрату - нитрозамину, тогда как депротонирование азота ведет к образованию конечного продукта - соли арендиазония.
Условия проведения реакции диазотирования
Диазотирование - экзотермическая реакция, сопровождающаяся выделением большого количества теплоты, поэтому процесс проводят при охлаждении, поддерживая температуру в интервале 0-5о, чтобы не допустить разложения термически неустойчивой соли арендиазония.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 |



