ЛЕКЦИЯ №5-6
Металлотермические методы получения металлов, их сплавов и неметаллов.
Восстановление оксидов. Металлотермическими реакциями называют реакции, протекающие между оксидами и металлами и приводящие к получению металлов в сплавленном виде за счет большого выделения теплоты. Если же выделяющейся теплоты не хватает для расплавления продуктов, то металл получается в виде мельчайших капелек, т. е. порошка.
Данный метод, был открыт в 1856 г. . Возможность его определяется физико-химическими свойствами исходных и получаемых веществ и тепловыми условиями проведения реакций.
Наиболее часто в качестве восстановителя применяют алюминий. Для образования сплавленного блока металла количества выделяющейся теплоты должно хватить на нагревание веществ выше температуры плавления наиболее тугоплавкого из получаемых компонентов, а также на тепловые потери за время от начала процесса до окончания расслаивания продуктов на шлак и металл. При восстановлении большинства оксидов (Fе2О3, Fе3О4, Со3О4, СоО, NiO, МnО2, Мn2О3, Мn3О4, СгО3, МоО3, V2О5 и др.) алюминием выделяющейся теплоты вполне достаточно и на нагревание продуктов реакции, и на тепловые потери. В этом случае получается металл, который оседает на дно тигля. Восстановление Мn2О3, МnО2, Со3О4 алюминием протекает с большой скоростью, с разбрасыванием реакционной смеси. Большая часть этих оксидов в зоне реакции разлагается с выделением кислорода и образованием Мn3О4, СоО. Выделяющийся кислород разбрасывает реакционную массу и перемешивает продукты, что мешает полному осаждению получаемого металла на дно тигля. Поэтому эти оксиды нельзя применять для получения марганца, кобальта и их сплавов.
Частичное разложение и испарение наблюдается при алюминотермическом восстановлении оксида хрома (VI) и оксида молибдена (VI). Эти оксиды также нельзя непосредственно использовать для алюмотермического получения металлов. Но их можно применять в качестве добавок к различным оксидам при получении сплавов. Для уменьшения испарения оксида молибдена (VI) в шихту добавляют фторид кальция.
Оксиды используют для получения двух-трехкомпонентных сплавов. При восстановлении некоторых оксидов (Сr2О3, Nb2О5, Та2О5, SiO2, TiO2, ZrО2, В2О3) алюминием выделяющейся теплоты недостаточно для нагревания продуктов реакции выше их температур плавления. Но если к ним добавить необходимое количество легковосстанавливаемых оксидов, то реакция
Сr2О3 + Fе2О3 + 4А1 = 2Сr + 2Fе + 2А12О3
пройдет и сплав осядет на дно тигля.
Чтобы получился двухкомпонентный сплав, можно предложить следующий метод расчета. Восстановление оксида алюминием или другим металлом сопровождается выделением определенного количества теплоты, которое должно нагреть продукты реакции до соответствующей температуры:
q
 t=
t=
Cp
где q — удельная теплота реакции, т. е. количество теплоты, выделяющейся на 1 г реакционной массы; Cр — средняя удельная теплоемкость продуктов реакции.
Но с начала реакции до окончания расслаивания продуктов на шлак и металл часть теплоты теряется. Поэтому реальная температура нагревания продуктов реакции составит:
q-q1
 t = *q,
t = *q,
q*Cp
где q1 — количество теплоты, теряемой реакционной массой;
q-q1
 - доля потерь теплоты.
- доля потерь теплоты.
q
Если принять, что теплоемкость продуктов реакции, т. е. металла и оксида алюминия, и тепловые потери являются постоянной величиной, то q-q1
q-q1
 t = K*q, где К=
t = K*q, где К=
q
В действительности теплоемкости получаемых металлов несколько отличаются. Соотношение между массой металла и оксида алюминия меняется в зависимости от состава исходного оксида и атомной массы металла. Тепловые потери также меняются. При большом количестве шихты они меньше, а когда берут небольшие массы веществ (в лабораторных опытах), они больше.
Коэффициент К будет иметь приближенное значение. Поэтому при расслаивании продуктов реакции на шлак и металл можно дать только приближенную оценку температуры.
Для определения минимальной массовой доли легковосстанавливаемого оксида, который необходимо добавить к трудновосстанавливаемому, составим уравнение:
w1(q1-q2)
 q = + q2
q = + q2
100
Это уравнение определяет удельную теплоту реакции восстановления смеси двух оксидов, в котором w1 — массовая доля легковосстанавливаемого оксида в смеси, q1 — удельная теплота его восстановления, q2 — удельная теплота восстановления трудновосстанавливаемого оксида.
Если w1 = 100%, то q = q1, если w1 =0, то q = q2•
Подставим значение q из последнего уравнения в уравнение t = Кq и получаем следующую формулу для вычисления оксида:
t w1(q1-q2)
![]()
 = + q2,
= + q2,
K 100
|
![]() t
t
( K )
 w1 =
w1 =
q1 – q2
Примем значение t равным температуре плавления наиболее тугоплавкого из получаемых компонентов. Обычно им является шлак — оксид алюминия, плавящийся при 2050 °С. При таком условии массовая доля (w1) легковосстанавливаемого оксида в смеси с трудновосстанавливаемым является минимально необходимой при алюминотермическом восстановлении смеси двух оксидов.
Если в реакции участвуют оксиды состава МеО, относительное содержание сплава в продуктах реакции повышается, а суммарная теплоемкость продуктов реакции понижается и коэффициент К имеет значение, равное 0,8.
При восстановлении оксидов алюминием металлы и неметаллы получаются в сплавленном виде и оседают на дно тигля. При использовании в качестве восстановителя магния и кальция металлы получаются в виде порошка. Это можно объяснить тем, что образующийся оксид магния имеет высокую температуру плавления, во время реакции не расплавляется и изолирует друг от друга отдельные мельчайшие капли металла.
При проведении алюминотермических реакций необходимо соблюдать некоторые правила предосторожности. Алюминии берут в виде мелких крупинок. Порошкообразный алюминий, имеющийся в продаже под названием алюминиевой пудры, непригоден (он содержит окисленный металл). С неокисленным алюминием реакции протекают слишком бурно, происходит разбрасывание шихты что снижает выход получаемого металла.
Оксиды а также реактор (тигель) необходимо предварительно просушить при 150-200 °С (при наличии влаги реакционная смесь разбрасывается). После этого оксиды растирают в порошок и отделяют на сите от неразмельченных частичек. Высушенные и размельченные исходные вещества отвешивают на технических весах и тщательно перемешивают. При проведении реакции следует брать не менее 25—30 г исходных веществ (суммарно). С большим количеством веществ реакции идут еще лучше, и выход металлов увеличивается. Масса алюминия должна быть равна теоретически рассчитанной.
Чтобы получить металл или сплав без алюминия, следует брать его несколько меньше теоретически рассчитанного на 1-2 %.
В качестве восстановителя можно использовать смеси порошкообразных металлов, а также смеси металлов с кремнием, например:
4Сr2О3 + 3Мg + 6А1 = 8Сr + 3Мg(А1О2)2
Несмотря на то что алюминат магния плавится при 2135 °С, т. е. выше, чем оксид алюминия, реакции со смесью восстановителей идут лучше. Это объясняется тем, что при использовании данной смеси металлов теплоты выделяется больше, чем при использовании в качестве восстановителя алюминия. Например, алюминий оксид хрома (III) непосредственно не восстанавливает ввиду недостаточного количества выделяющейся теплоты. Этот оксид восстанавливает смесь алюминия с магнием или кальцием. Для проведения реакции нужна зажигательная смесь.
Приготовление зажигательной смеси. Существует несколько рецептов приготовления зажигательной смеси: 1) 9 мас. ч. растертого пероксида бария смешивают с 1 мас. ч. порошкообразного алюминия; 2) берут 3 мас. ч. растертого нитрата калия и 1,3 мас. ч. алюминиевой пудры; 3) готовят смесь 4 мас. ч. растертого пероксида бария и 1 мас. ч. порошкообразного алюминия и добавляют 0,7 мас. ч. отдельно растертого хлората калия. Зажигательную смесь хранят в сухой, хорошо закупоренной стеклянной банке; приготовлять ее в больших количествах не рекомендуется.
Заполнение реактора шихтой. В качестве реактора используют магнезиальные или корундовые тигли, так как они термически стойки и вещества при работе с ними меньше загрязняются. Фарфоровые тигли, как правило, разрушаются. Поэтому их нужно помещать в песок, чтобы расплавленная масса не выливалась. Более удобны шамотовые или глиняные тигли, но в этом случае продукт несколько загрязняется кремнием и другими веществами.
Тигель 1 (рис. 3) заполняют на 3/4 его высоты смесью из оксида и восстановителя, утрамбовывают, делают небольшое углубление и засыпают сверху тонким слоем (около 1 —1,5 мм) зажигательной смеси. Ленту магния 4 вставляют в углубление, которое затем заполняют зажигательной смесью в форме горки. Если лента магния покрыта слоем оксида, ее следует очистить ножом.
Реакцию можно проводить в песке или в оксиде магния, предварительно прокаленных. В таком материале, насыпанном в стальной ящик, делают углубление, в которое и помещают реакционную смесь в бумажном кульке (рис. 4).
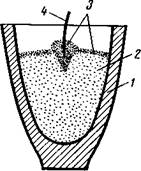
рис.3 Восстановление оксидов в тигле:
1 — тигель; 2 — смесь оксидов с алюминием; 3 — зажигательная смесь; 4 — лента магния.
рис.4 Восстановление оксидов в песке: 1 — металлический ящик; 2 — песок; 3 — бумажный кулек; 4 — смесь оксидов с алюминием; 5 — зажигательная смесь; 6 — лента магния. |
Меры предосторожности. Реакцию проводят в вытяжном шкафу, откуда убирают все легковоспламеняющиеся материалы. Тигель помещают на песок. Работают в защитных очках!

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 |



