Для хлорирования применяют также тетрахлорид углерода, фосген или хлориды серы, т. е. вещества, в которых имеется элемент-восстановитель, отнимающий кислород от оксида. По-видимому, из указанных веществ наилучшими хлорирующими свойствами обладает тетрахлорид углерода. При его взаимодействии с устойчивыми оксидами углерод восстанавливается до оксида углерода (II), который с избытком хлора дает фосген:
SiО2 + 2ССl4 = SiС14 + 2СОС12
Сr2О3 + 3ССl4 = 2СrС13 + 3СОС12
При хлорировании менее устойчивых оксидов углерод тетра-хлорида переходит главным образом в оксид углерода (IV), например:
2СuО + ССl4 = 2СuС12 + СО2
Поэтому при использовании для хлорирования тетрахлорида углерода отходящие газы необходимо направить в хорошую тягу.
Примеси оксидов других элементов, имеющихся в исходном веществе, также подвергаются галогенированию. При этом между галогенидами и оксидами устанавливается равновесие, смещенное в сторону образования наиболее устойчивого галогенида или оксида, например:
2Fе2O3 + 3SiCl4 = 4FеCl3 + 3SiO2
Для хлорирования готовят смесь из оксида и угля. Уголь берут в некотором избытке по сравнению с теоретическим расчетом, считая, что он в данном процессе окисляется до оксида углерода (II).
Если получаемый хлорид при комнатной температуре — легкоиспаряющаяся жидкость (ТiС14, SnС14, SiСl4), то хлорирование проводят в установке получения легкокипящих хлоридов с использованием электропечи.
Если же получают трудноиспаряющийся хлорид, например хлорид хрома (III), то он в виде возгона скапливается на более холодных стенках трубки, в ее отводящем конце.
Продукты возгонки прочно удерживаются на стенках трубки. Поэтому после окончания реакции и охлаждения трубки в слабом токе хлора сначала удаляют непрореагировавшую массу. Для этого трубку ставят вертикально и осторожно постукивают ее концом о твердую поверхность. Затем продукт снимают стеклянной палочкой или металлическим прутом на лист гладкой бумаги.
Для хлорирования оксидов тетрахлоридом углерода используют другой прибор (рис. 12). Оксид помещают в одной или двух лодочках в фарфоровую или кварцевую трубку. Тетрахлорид углерода наливают в перегонную колбу 1. После нагревания печи до соответствующей температуры пускают слабый ток хлора (1—2 пузырька в счетчике пузырьков). Образующийся хлорид возгоняется и оседает на холодных стенках трубки. Не вступивший в реакцию тетрахлорид углерода и фосген отводят в тягу. Этот метод не рекомендуется применять для хлорирования оксидов, образующих жидкие хлориды (например, тетрахлориды титана, олова), так как продукт обычно загрязняется тетрахлоридом углерода.
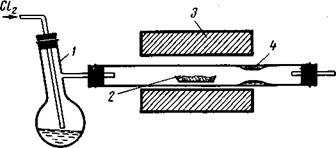
Рис. 12. Хлорирование оксидов тетрахлоридом углерода:
1 — колба с тетрахлоридом углерода; 2 — лодочка с хлорируемым веществом; 3 — электропечь; 4 — возгон хлорида.
Некоторые оксиды, например V2O5, МоО2, WО2, при хлорировании дают оксихлориды. Реакции протекают при небольшом нагревании (300—400 °С). Оксихлориды имеют невысокие температуры кипения, поэтому для их получения можно применять простейшие установки для получения легковозгоняющихся хлоридов. Оксид помещают в первое колено трубки, а возгон оксихлорида собирают во втором или третьем колене и запаивают.
Бромирование металлов, неметаллов и оксидов
1. Бромирование металлов и неметаллов бромом
Присоединение брома к металлам или неметаллам идет с выделением меньшего количества теплоты, чем при хлорировании, но реакции бромирования при нагревании протекают быстро.
Все лабораторные способы бромирования можно разделить на две группы:
1. Подвод брома к веществу осуществляется за счет естественной диффузии брома.
2. Бром подводят к веществу газом-носителем: азотом, водородом, оксидом углерода (IV).
Бромирование по первому методу осуществляется в запаянных ампулах. Одна из форм ампулы приведена на рисунке 13, А. В нее помещают вещество и наливают по расчету, но с небольшим избытком бром. Затем ампулу запаивают по линии ав и после охлаждения переворачивают (рис. 13, Б). При этом бром стекает во второе колено. Для проведения реакции трубку для бромирования устанавливают горизонтально (рис. 13, В). Укрепив ее в штативе, осторожно нагревают конец трубки с металлом. Нагревание удобнее вести в
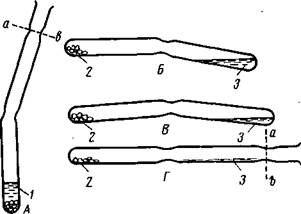
Рис. 13. Бромирование металлов и неметаллов: / — бром; 2 — бронируемые вещества; 3 — бром.
трубчатой печи, вставив в нее пробирку на небольшую глубину, температуру следует поднимать медленно, со 100 до 250—300 °С.
Описанная методика пригодна для получения бромидов, не возгоняющихся при температуре реакции, например: СdBr2, СrВr3 , МgВr2 , РbВr2, SnВr2 и др.
Этим же способом можно получить бромиды, которые при температуре реакции (около 300 °С) возгоняются. В этом случае бром берут в некотором недостатке. Образующийся бромид возгоняется во второе колено трубки; он скапливается в суженной части пробирки. После того как весь бром вступит в реакцию, нужно большую часть бромида перегнать в верхнюю половину пробирки. Для этого левую, суженную часть ее нагревают до 300—350 °С горелкой или электропечью. Бромид возгоняется с большой скоростью при давлении его паров 10 кПа или выше. После окончания реакции бромид запаивают в ампуле. Полученное вещество может содержать небольшое количество растворенного брома.
Некоторые металлы, например алюминий, цинк и др., вступают в реакцию с жидким бромом уже при комнатной температуре. В этих случаях для разделения исходных веществ используют ампулу, конструкция которой изображена на рисунке 13, Г. Сначала в ампулу помещают металл, а затем, расположив ее горизонтально, в другое колено при помощи пипетки наливают бром. Затем ампулу запаивают по линии ав и, не переворачивая ее, нагревают металл.
2. Бромирование металлов и неметаллов бромоводородом или смесью брома с другими газами.
При использовании индифферентного газа (Н2, Не, СО2) в качестве переносчика паров брома применяют установку, приведенную на рисунке 14.
Рис. 14. Прибор для бромирования с использованием газа-переносчика:
1 — четырехколенная трубка; 2 — бронируемое вещество; 3 — бром.
Металл или неметалл помещают в первое колено четырехколенной стеклянной трубки и включают ток газа, который захватывает пары брома, находящиеся в реторте. В качестве резервуара для брома можно также использовать пробирку или перегонную колбу. После вытеснения воздуха из трубки нагревают ее первое колено А до 400—450 °С, продолжая пропускать газ-переносчик. Трубку с перетяжками применяют в том случае, когда температура возгонки бромидов лежит в пределах 100—350 °С. Тогда большая часть продукта собирается во втором колене трубки. При нагревании в пламени газовой горелки бромид перегоняют в слабом токе газа в третье колено. Повторная возгонка позволяет получить бромид в чистом состоянии. Бром нужно брать в недостатке по сравнению с теоретически необходимым количеством, чтобы его полностью использовать. После окончания реакции пары брома вытесняют из трубки индифферентным газом, прибор разбирают и трубку закрывают пробками. Затем продукт запаивают в последнем колене на газовой горелке. При наличии в газах-переносчиках примесей кислорода или паров воды бромирование замедляется вследствие образования на поверхности вещества оксидной пленки. Такие металлы, как ванадий, тантал, молибден, вольфрам, дают летучие оксибромиды, которые загрязняют полученный бромид. Поэтому следует очистить применяемые газы, пропуская их через трубку, наполненную магниевыми стружками и нагретую до 500—550 °С.
Если получаемый бромид не возгоняется, то реакция идет медленно, так как продукт реакции покрывает поверхность исходного вещества.
Для проведения реакции при 500—1000 °С может служить установка для хлорирования оксидов тетрахлоридом углерода. которая (рис. 12). В перегонную колбу наливают бром. В качестве переносчика брома применяют азот, водород или аргон. Если давление паров бромида при температуре реакции меньше 1 кПа, то большая часть бромида остается в лодочке. При большем давлении пара (5 кПа и более) он возгоняется и конденсируется в холодном конце трубки. После окончания реакции, которая длится 1,5—2ч, печь выключают и, продолжая пропускать очень слабый ток газа-носителя, трубку охлаждают. Затем прибор разбирают и лодочку быстро вынимают. Если продукт находится в лодочке, то его с помощью скальпеля быстро вынимают и помещают в пробирку для запаивания. Если же вещество возгоняется, то его снимают со стенок трубки стеклянной палочкой или металлическим стержнем на лист гладкой бумаги и быстро пересыпают в пробирку для запаивания.
Смесь азота и водорода, используемая в качестве переносчика брома, легко приготовить из аммиака. Раствор аммиака подогревают в колбе. Выделяющийся аммиак поступает в трубку, в которой находятся мелкие железные стружки или тонкая железная проволока, нагретые до 700—1000 °С. При этой температуре аммиак практически полностью разлагается на азот и водород. Он не нуждается в какой-либо специальной очистке и пригоден при получении большинства бромидов.
Оксид углерода (IV) в качестве переносчика брома можно применять только в том случае, если он не окисляет бромируемый металл или неметалл. При бромировании бора, кремния, магния, бериллия и элементов подгрупп хрома, ванадия, марганца применять оксид углерода (IV) нельзя, также нежелательно бромировании элементов подгруппы железа.
3. Бромирование металлов и неметаллов бромом в присутствии воды
Бромирование металлов в водных растворах приводит к образованию кристаллогидратов. В коническую колбу на 100— 150 мл помещают 3—5 г металла в виде порошка, тонкой проволоки или стружек, к которому приливают 15—20 мл воды и теоретически рассчитанное количество брома. Бром наливают небольшими порциями (тяга!) из мерного цилиндра. Иногда реакция присоединения брома идет с большой скоростью, особенно когда используется мелкодисперсный порошок металла, при этом выделяется теплота и жидкость закипает, поэтому для охлаждения колбу помещают в холодную воду. После окончания реакции к раствору добавляют небольшое количество металла и кипятят для удаления возможных следов брома. Горячий раствор бромида профильтровывают и кристаллизуют.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 |



