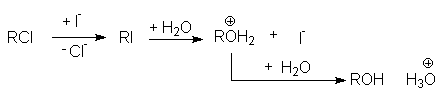
Конкуренция реакций нуклеофильного замещения
При проведении реакций нуклеофильного замещения в реакционных смесях могут присутствовать несколько нуклеофилов. В этих случаях имеет место конкуренция нескольких нуклеофильных реакций:
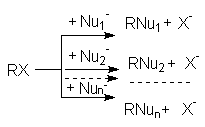
Из схемы конкуренции видно, что увеличение выхода любого из продуктов достигается увеличением избытка нуклеофила, ответственного за его образование. Так, при реализации щелочного гидролиза хлоралканов протекают следующие реакции
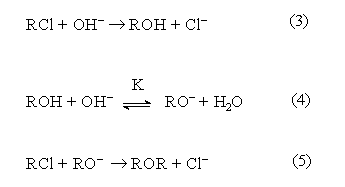
Можно видеть, что соотношение скоростей основной реакции (3) и побочной реакции образования простого эфира (5) определяется конкурентным взаимодействием
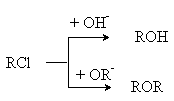
и увеличение выхода основного продукта, спирта, может быть обеспечено увеличением избытка гидроксил-аниона. Поскольку соотношение ![]() определяется в соответствие с равновесием (4) равенством
определяется в соответствие с равновесием (4) равенством
![]()
факторами увеличения выхода спирта являются увеличение избытка воды и снижение конверсии хлоралкана (что равносильно понижению концентрации спирта).
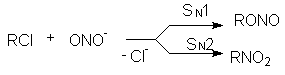
Некоторые нуклеофилы обладают двумя реакционными центрами и поэтому дают разные продукты замещения. При этом преимущественное образование продукта замещения по тому или иному реакционному центру определяется правилом Корнблюма: Если реакция протекает по SN2-механизму, то нуклеофил реагирует с субстратом своим более нуклеофильным (поляризуемым) центром. Если реакция протекает по SN1-механизму, то нуклеофил реагирует с субстратом своим более электроотрицательным основным центром. Примером ионов с двойственной реакционной способностью (амбидентных ионов) являются цианид-анион С≡ N и нитрит-анион

Эти анионы в зависимости от механизма реакции, определяемого условиями их проведения и структурой субстрата, могут давать следующие продукты
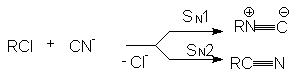
Подобная ситуация имеет место при обмене галогенов. Реакция SN2 всегда протекает в сторону замещения более электроотрицательного атома на более нуклеофильный (поляризуемый) (F и Cl на Br и J). Однако при SN1-замещении образуется продукт с более электроотрицательным заместителем (например, RF из RСl). Для изменения механизма используют соли или катализаторы с сильно электрофильным катионом (AgF, HgF2, SbF3, SbF5):
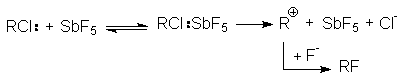
Лекция №11-12. Реакции карбоновых кислот и их производных с нуклеофильными реагентами.
Реакции нуклеофильного замещения
Ацилгалогениды легко реагируют с различными нуклеофильными реагентами, причем эти реакции не требуют катализа. Общая схема этих реакций может быть представлена уравнениями
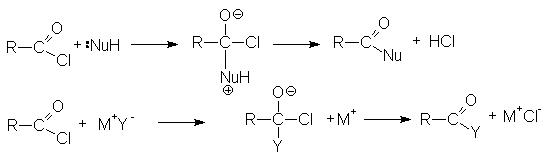
Важными реакциями нуклеофильного замещения по ацильному углероду являются:
Гидролиз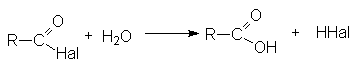
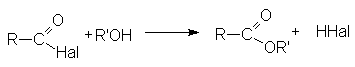
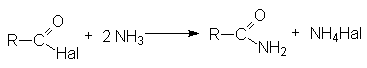
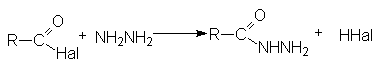
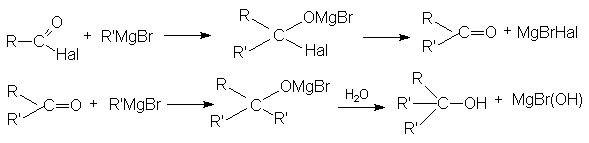
По этому суммарно реакцию можно представить следующей схемой
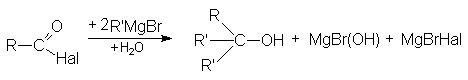
Реакции восстановления
Восстановление натрийборгидридом или литийалюминий гидридом.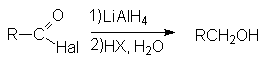
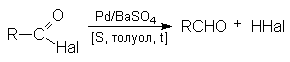
Реакция с диазометаном (реакция Арндта-Эйстерта)
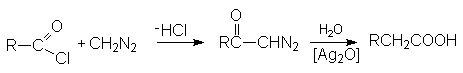
Эта реакция является синтетическим средством увеличения длины углеводородных цепей органических соединений на один атом углерода.
АНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
Строение ангидридов выражается следующей общей формулой
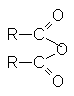
Химические свойства ангидридов карбоновых кислот
Одна ацильная группа действует на другую как сильный акцептор, поэтому на карбонильном атоме углерода концентрируется достаточно высокий положительный заряд. Это обусловливает высокую реакционную способность ангидридов в реакциях нуклеофильного замещения
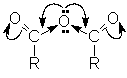
Реакция нуклеофильного замещения
Ангидриды карбоновых кислот легко реагируют с различными нуклеофильными реагентами, хотя скорость реакции меньше, чем в случае ацилгалогенидов.
Общий механизм реакции ангидридов карбоновых кислот с нуклеофилом может быть представлен схемой:
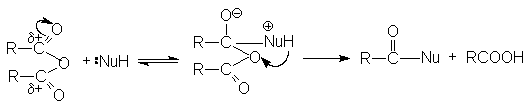
Можно видеть, что в результате реакции кроме продукта нуклеофильного
замещения 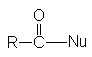 образуется карбоновая кислота.
образуется карбоновая кислота.
Важнейшими реакциями нуклеофильного замещения с участием ангидридов карбоновых кислот является:
Гидратация.
(RCO)2O + H2O → 2RCOOH
(RCO)2O + R'OH → RCOOR' + RCOOH
(RCO)2O + 2NH3 → RCONH2 + RCOONH4
К е т е н
Кетен формально может рассматриваться как ангидрид уксусной кислоты.
CH2=C=O + H2O → CH3CHO
Химические свойства
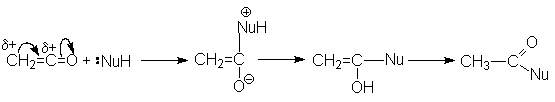
Химическое поведение кетена определяют два фактора: напряженность
![]()
молекулы и высокий положительный заряд на карбонильном углероде
Наиболее типичными реакциями кетенов являются реакции нуклеофильного присоединения.
Наиболее важными среди этих являются реакции гидратации, образования ангидридов сложных эфиров и амидов карбоновых кислот:
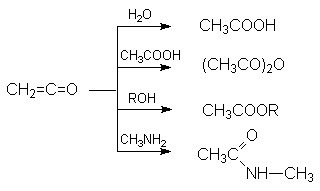
Поскольку в результате этих реакций не образуется каких-либо других продуктов, то кетен является идеальным ацилирующим агентом.
СЛОЖНЫЕ ЭФИРЫ
Сложные эфиры – производные карбоновых кислот, которые можно рассматривать как результат замещения гидроксильной группы карбоновой кислоты на алкоксирадикал 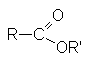
Химические свойства
Объектами нуклеофильной атаки могут быть ацильный или алкильный углерод. В то же время кислотность водородных атомов при α - углеродном атоме радикала кислоты обусловливает склонность сложность эфиров к реакции конденсации.
Реакции нуклеофильного замещения
Гидролиз.
Различают кислотнокаталитический гидролиз и основной гидролиз (омыление). Кислотный гидролиз представляет собой обратимую реакцию.
![]()
Механизм этой реакции – см в разделе Кислотно-каталитическая этерификация – Химические свойства карбоновых кислот.
Реакция омыления необратима. Основание не только ускоряет реакцию гидролиза, но выступает в качестве реагента. Эффективность реакции обусловлена высокой нуклеофильной активностью гидроксил-анионов.
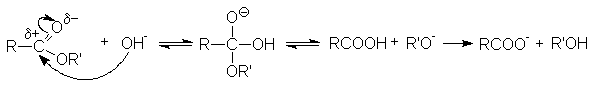
RCOOR' + NaOH → RCOONa + R'OH
Аммонолиз.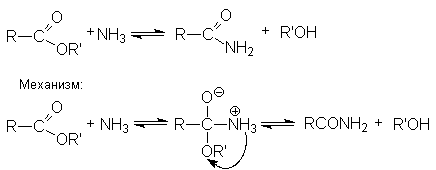
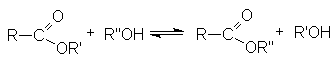
Реакция катализируется кислотами или основаниями.
Взаимодействие с магний - и литий-органическими соединениями.а) Реакция с магнийорганическими соединениями подобна реакции с галогенангидридами.
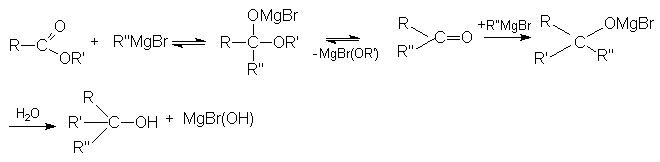
б) Взаимодействие с Li-органическими соединениями.
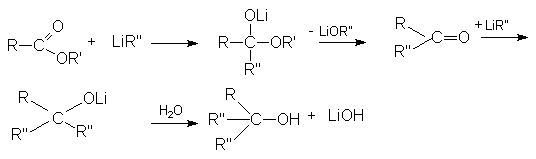
Реакции восстановления.
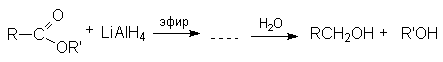
Реакции конденсации
Конденсация Кляйзена – наиболее важная в синтетическом отношении реакция. Ее стехиометрический результат заключается в автоконденсации этилацетата, катализируемая этилатом натрия. 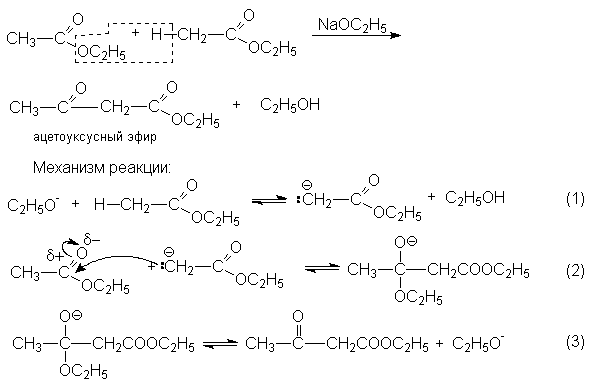
Условия равновесия неблагоприятны для всех трех стадий. Поэтому равновесие брутто-реакций существенно смещено в левую сторону.
Факторами смещения равновесия могут быть: отгонка этилового спирта, применение избытка этилата натрия. Последний метод оказывается эффективным, так как этанол более слабая кислота, чем енол сложного эфира, и избыток этилата смещает равновесие нацело вправо вследствие превращения β - кетоэфира в соль енола.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 |



