Такие устойчивые оксиды, как SiO2, МnО, TiO и др., практически водородом не восстанавливаются, так как для получения даже небольших количеств металла нужны огромные количества абсолютно сухого водорода. Например, константа равновесия реакции восстановления
![]()
![]() SiO2 + 2H2 Si + 2H2O
SiO2 + 2H2 Si + 2H2O
при 1200 °С равна 10-65. Поэтому для получения, например, 1 г кремния восстановлением его оксида SiO2 требуется совершенно сухой водород массой 6·1064 г. Если же водород содержит следы паров воды, то они будут окислять кремний до его оксида.
Реакции восстановления оксидов начинаются при температуре около 200 — 400 °С и в большинстве случаев идут с небольшими скоростями. Металлы, получаемые при умеренных температурах, часто обладают пирофорностью, т. е. вспыхивают на воздухе. Объясняется это не только большой поверхностью порошкообразного металла, но также и тем, что пирофорные металлы имеют искаженную кристаллическую решетку, повторяющую в какой-то степени кристаллическую решетку исходного оксида. Перестройка решетки и поверхностное окисление металла приводят к его разогреванию и к самовозгоранию на воздухе.
Для получения пирофорных металлов необходимо брать оксиды, прокаленные при невысоких температурах.
Если температура восстановления близка к температуре плавления, металлы получаются в виде плотной губки. В сплавленном виде металлы получаются при более высоких температурах, чем их температуры плавления. Это можно объяснить тем, что на поверхности образующихся мельчайших капелек металла имеется слой адсорбированного водорода и оксидов трудновосстанавливаемых металлов, которые в незначительном количестве почти всегда присутствуют в виде примесей в исходных оксидах. Выбор метода восстановления определяется свойствами исходного оксида, а также соответствующей формой получения металла (в виде пирофорного порошка, губки или в сплавленном виде).
Если температура восстановления выше 600 — 650 °С, то реакцию проводят в трубчатых электропечах (рис. 1). Предварительно установку проверяют на герметичность.
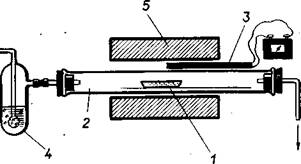
Рис. 1. Восстановление оксидов водородом:
1—лодочка с оксидом; 2 — фарфоровая или кварцевая трубка; 3 — термопара с пирометрическим гальванометром; 4 —промывалка; 5 — электропечь.
При температуре 550—600 °С и ниже реакцию можно вести не в лодочке, а прямо в стеклянной трубке или в трубке с перетяжками (рис. 2).
В такой реактор при помощи узкого шпателя или стеклянной трубки вводят 2—3 г оксида и нагревают его в токе водорода. Если полученный металл окисляется на воздухе, его следует после окончания реакции запаять в той же трубке. Для этого после охлаждения металла в токе водорода трубку отсоединяют от источника водорода, вынимают пробки и оставляют ее на 5—7 мин в наклоненном положении. Затем трубку запаивают. Водород для восстановления получают или в аппарате Киппа, или в электролизере. Собранный прибор перед работой проверяют на герметичность поместив один конец в воду. Если водород проходит через слой воды, то прибор герметичен.
Окончание реакции восстановления оксидов определить довольно трудно. Об этом можно судить по изменению цвета или уменьшению массы оксида, но только в том случае, если он имеет постоянный и известный состав. В тех случаях, когда восстановление проводят в прозрачных трубках и при температуре, немного превышающей точку плавления металла, об окончании реакции можно судить по образованию металлических корольков. Если восстанавливаются малостойкие оксиды, то в конце трубки собирается вода, что является признаком окончания реакции.
Описанным методом можно получать: в восьмой группе периодической системы — железо, кобальт, никель и платиновые металлы. Малостойкие оксиды, например платины, могут при нагревании в атмосфере водорода быстро разлагаться, что иногда приводит к взрыву.
В седьмой группе — рений. Оксид марганца (IV) также легко восстанавливается водородом, но конечным продуктом восстановления является прочный оксид марганца (II).
В шестой группе — молибден, вольфрам и теллур. Оксид хрома (III) можно восстанавливать водородом, но константа равновесия реакции восстановления очень мала, поэтому хром этим методом практически не получают, так как для образования даже незначительных количеств металла необходимо большое количество совершенно сухого водорода.
В пятой группе — сурьма, висмут.
В четвертой — германий, олово, свинец.
Углерод этим методом получить нельзя, так как восстановление идет только до оксида углерода (II):
![]()
![]() СО2 + Н2 СО + Н2О
СО2 + Н2 СО + Н2О
В третьей группе — галлий, индий, таллий.
Во второй группе — цинк, кадмий, ртуть.
Реакция с цинком дет при температуре выше температуры испарения цинка, поэтому образующийся цинк током водорода уносится из зоны реакции, конденсируется на холодном конце трубки и частично окисляется парами воды.
При нагревании оксида ртути в атмосфере водорода может произойти взрыв образующейся гремучей смеси.
В первой группе — медь, серебро, золото. Оксиды серебра и золота при нагревании в атмосфере водорода могут вызвать взрыв. Поскольку оксиды этих металлов разлагаются при простом нагревании, описанный метод для их получения не используют.
Получение оксидов с низшей степенью окисления
Оксиды элементов с различной степенью окисления восстанавливаются ступенчато:
![]()
![]()
![]() МnO2 Mn2O3 Mn3O4 MnO
МnO2 Mn2O3 Mn3O4 MnO
Каждая из этих реакций восстановления имеет свою константу равновесия.
На основании значения констант равновесия реакций восстановления оксидов водородом можно решить вопрос о максимально необходимом количестве водорода, о минимальном количестве паров воды в газовой фазе.
Например, константы равновесия реакции восстановления Fе2О3 до Fе3О4, Fе3О4 до FеО и FеО до Fе при температуре 727 °С соответственно равны 2·104, 2,5 и 0,39.
[H2O] 2·104·100

 Кр = = 2·104 = , Откуда [H2O] = 99,99 %
Кр = = 2·104 = , Откуда [H2O] = 99,99 %
[100-H2O] 1 + 2·104
То есть получение Fе3О4 восстановлением Fе2О3 трудно, так как в газовой фазе в состоянии равновесия присутствуют только следы водорода и 99,99% паров воды.
Получение металлов и низших хлоридов восстановлением соответствующих высших хлоридов
Некоторые безводные хлориды, например СгС12, FеС12, ТiС13 и др., в которых элементы находятся в низшей степени окисления, получаются восстановлением соответствующих хлоридов водородом. Поскольку большинство исходных хлоридов сильно гигроскопичны, восстановление следует проводить в той же установке, в которой получают хлориды. Об окончании восстановления хлорида до металла судят по прекращению образования хлороводорода. Для этого конец газоотводной трубки опускают в пробирку с раствором нитрата серебра. Если же образуется хлорид с меньшей степенью окисления, который может восстанавливаться до металла, то об окончании реакции судят по изменению цвета исходного и цвету получаемого хлорида.
Реакции гидрирования
Металлы, получаемые восстановлением их оксидов водородом, в той или иной степени насыщаются водородом. Во многих случаях образуются фазы внедрения — твердые растворы водорода в металле. При этом поглощается теплота, а растворимость водорода увеличивается с повышением давления. Так ведут себя железо, кобальт, никель, хром, молибден, алюминий, серебро, платина и другие металлы.
Щелочные и щелочноземельные металлы дают при нагревании в атмосфере водорода соединения типа МеН и МеН2. Реакции протекают с выделением теплоты. Некоторые металлы образуют гидриды нестехиометрического состава. К ним относятся соединения титана, циркония, ванадия, ниобия, тантала, вольфрама, церия, лантана и т. д.
Реакцию гидрирования, т. е. присоединения водорода к металлам и неметаллам, проводят в тех же приборах, что и реакции восстановления водородом (рис. 1 и 2).
Получают гидриды щелочных и щелочноземельных металлов при температуре 400—700 °С в трубке (стеклянной, фарфоровой или кварцевой) (рис. 1,2). Натрий, калий, рубидий, цезий можно помещать непосредственно в трубку, так как со стеклом они почти не реагируют (небольшое взаимодействие наблюдается с натрием). Этот метод удобен тем, что гидрид можно в этой же трубке запаять. Реакцию следует проводить при температуре возгонки щелочного металла. Гидриды переносят в пробирку и запаивают. Если для хранения используют трубку, где был получен гидрид Ме, то сначала ее предварительно охлаждают в токе водорода, пропускают через нее осушенный азот и закрывают (неплотно) с двух сторон пробками. Затем отпаивают концы трубки в непосредственной близости от гидрида. • Гидриды лития и щелочноземельных металлов нужно получать в железных или никелевых лодочках (фарфоровые или кварцевые лодочки загрязняют гидрид кремнием). Гидриды этих металлов устойчивы на воздухе, и их можно переносить в трубку для запаивания. Чтобы исключить разрушение материала трубки от паров металла, ее внутренние стенки защищают листовым железом. После окончания гидрирования продукт охлаждают в токе водорода. Гидрид вынимают из лодочки скальпелем или узкой стамеской и быстро переносят в пробирку и запаивают. Предварительно пробирку заполняют сухим оксидом углерода (IV).
Щелочные и щелочноземельные металлы часто содержат на поверхности оксиды, гидроксиды, нитриды, карбонаты, поэтому их очищают. Для этого кусок металла помещают в фарфоровую чашку, заливают тонким слоем осушенного эфира и соскабливают с него скальпелем поверхностную корку. После этого пинцетом металл переносят в другую чашку с небольшим количеством эфира и отмывают от приставших кусочков посторонних веществ. Затем металл помещают в трубку для гидрирования и пропускают водород для удаления остатков эфира. После полного вытеснения воздуха можно нагревать трубку. Водород не должен содержать кислорода и паров воды, поэтому его следует тщательно очистить.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 |



