С помощью качественных реакций в водном извлечении из сбора было установлено наличие флавоноидов, фенолкарбоновых кислот, гликозидов, аскорбиновой кислоты, аминокислот и полисахаридов.
Методом бумажной хроматографии в присутствие свидетелей РСО и хроматографически чистых образцов подтверждено наличие: на уровне РСО ликуразида (Rf~0,11); на уровне ГСО лютеолин-7-гликозида (Rf~0,53); на уровне РСО танина (Rf~0,61).
При длине волны 254 нм видны 11 флуоресцирующих пятен: на уровне РСО ликуразида (Rf~0,11); на уровне РСО лютеолин-7-гликозида (Rf~0,53); на уровне РСО танина – пятно коричневатого цвета (Rf~0,61); на уровне РСО галловой кислоты – пятно сине-фиолетового цвета (Rf~0,93).
Полученные данные подтверждены методом ВЭЖХ. Результаты исследований представлены в таблице 3.
Таблица 3
Результаты исследования фенольных соединений сбора методом ВЭЖХ.
Номер пика | Идентифицировано | % Содержание в выделенной смеси (метод внутренней нормализации) |
1 | Галловая кислота | 11,58 |
2 | Катехин | 5,88 |
3 | Хлорогеновая кислота | 6,22 |
4 | Кофейная кислота | 28,03 |
5 | Лютеолин-7-гликозид | 13,70 |
6 | Ликуразид | 1,79 |
7 | Кверцетин | 15,31 |
8 | Дигидрокверцетин | 2,43 |
9 | Апигенин | 2,06 |
Общий вид хроматографического профиля фенольных соединений представлен на рисунке 1.
Рис. 1. Идентификация фенольных соединений в сборе методом ВЭЖХ
1 - галловая кислота; 2 - катехин; 3 - хлорогеновая кислота; 4 - кофейная кислота; 5 - лютеолин-7-гликозид; 6 - ликуразид; 7 - кверцетин; 8 - дигидрокверцетин; 9 - апигенин
Методом ВЭЖХ осуществлено определение содержания органических кислот, в ходе которого в составе сбора идентифицированы: щавелевая, винная, маликовая, янтарная, бензойная, салициловая кислоты.
Результаты идентификации органических кислот в анализируемом сборе представлены в таблице 4.
Таблица 4
Результаты идентификации органических кислот в сборе методом ВЭЖХ.
Номер пика | Идентифицировано | Времена удерживания, мин | Содержание в выделенной смеси, % (метод внутренней нормализации) |
1 | Щавелевая кислота | 4,99 | 59,01 |
2 | Винная кислота | 5,89 | 11,27 |
3 | Маликовая кислота | 6,63 | 24,63 |
4 | Янтарная кислота | 10,23 | 0,31 |
5 | Бензойная кислота | 14,93 | 0,21 |
6 | Салициловая кислота | 15,84 | 4,57 |
Общий вид хроматографического профиля органических кислот представлен на рисунке 2 .
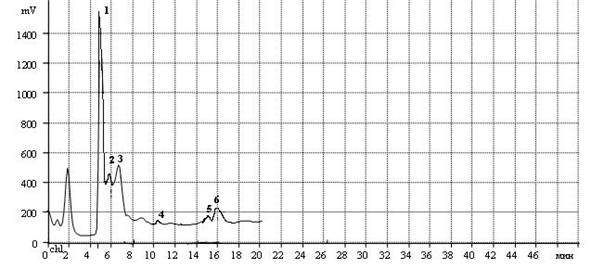
Рис.2. Идентификация органических кислот в сборе методом ВЭЖХ
1 - щавелевая кислота; 2 - винная кислота; 3 - маликовая кислота; 4 - янтарная кислота; 5 - бензойная кислота; 6 - салициловая кислота.
Поскольку в разработанном сборе содержится трава душицы и тысячелистника, основным компонентом которых является эфирное масло, нами был изучен состав эфирного масла выделяемый из анализируемого сбора.
Анализ проводили в стандартных условиях с использованием РСО гераниола, L-пинена, β - пинена, борнилацетата и тимола. Детектирование проводили с использованием анисового альдегида. В данных условиях в испытуемом образце было обнаружено 11 пятен. Из них идентифицировано 5 пятен на уровне пятен РСО, 6 пятен не идентифицировано.
Результаты идентификации эфирного масла в анализируемом сборе представлены в таблице 5.
Таблица 5
Результаты идентификации компонентов эфирного масла методом ТСХ.
Rf | Rf РСО | Идентифицировано | ||||
Гераниол | Тимол | L-пинен | β-пинен | борнилацетат | ||
0,05 0,11 0,16 0,20 0,25 0,33 0,45 0,67 0,73 0,75 0,98 | 0,25 | 0,75 | 0,45 | 0,33 | 0,73 | Гераниол β-пинен L-пинен Борнилацетат Тимол |
Для определения содержания эфирных масел в сборах использовали метод перегонки с водяным паром с подбором оптимальных условий количественного определения. Результаты исследований представлены в таблице 6.
Таблица 6
Влияние условий перегонки на выход эфирного масла из сборов.
Навеска сырья, г | Выход эфирного масла, % | ||||||||
Степень измельченности и время перегонки и время перегонки | |||||||||
1 мм | 2 мм | 3 мм | |||||||
1ч | 2ч | Зч | 1ч | 2ч | Зч | 1 ч | 2ч | Зч | |
Сбор | |||||||||
10,0 | 0,10± 0,003% | 0,15± 0,005% | 0,15± 0,005% | 0,08± 0,002% | 0,12± 0,004% | 0,12± 0,004% | 0,09± 0,003% | 0,11± 0,004% | 0,12± 0,004% |
С помощью метода ВЭЖХ установлен качественный и количественный состав аминокислот. В результате идентифицировано наличие 16 аминокислот: лизин (5,3%), метионин (0,08%), гистидин (2,8%), аргинин (8,5%), треонин (4,9%), серин (6,6%) пролин (6,2%), глицин (10,5%) валин (6,6%), изолейцин (3,2%), лейцин (8,0%), тирозин (2,8%), фенилаланин (2,9%) аланин (10,0%) глутаминовая кислота (12,0%), аспарагиновая кислота (8,7%).
Учитывая литературные данные, подтверждающие широкий спектр фармакологического действия фенольных соединений, а также принимая во внимание результаты предыдущих исследований, подтвердившие присутствие фенольной фракции в анализируемом сборе, мы сочли целесообразным привести количественную оценку суммы флавоноидов в пересчете на рутин и фенолкарбоновых кислот в пересчете на хлорогеновую кислоту.
Для разработки методики количественной оценки суммы действующих веществ нами были подобраны оптимальные условия проведения анализа: выбор экстрагента, его соотношение с сырьем, размер частиц сырья и время экстракций. Результаты представлены в таблице 7.
Таблица 7
Выбор оптимальных условий экстракции флавоноидов
Изучаемый параметр | Содержание флавоноидов, % |
Концентрация этилового спирта | |
Н2О | 0,086 ± 0,004 |
25% | 0,124 ± 0,005 |
50% | 0,284 ± 0,011 |
70% | 0,455 ± 0,018 |
96% | 0,138 ± 0,005 |
Продолжение таблицы 7

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



