cCR – клинический полный ответ
cPR – клинический частичный ответ
cNR – нет ответа (стабилизация)
cNA – клинически не оценивался
В таблице 24 представлена частота местно-региональных рецидивов в группах пациентов с HER2-позитивным РМЖ, получавших различные виды неоадъювантной терапии. В работе оценена их частота на протяжении 5,5 лет (медиана наблюдения 3,2 года).
У пациентов, получавших неоадъювантную анти-HER2 таргетную терапию в комбинации с антрациклин-таксан содержащей химиотерапией не наблюдалось случаев местного рецидива после органосохраняющей операций при медиане наблюдения 3,5 года.
Табл. 24 Частота местных рецидивов после органосохраняющих операций и мастэктомий в зависимости от вида неоадъювантной терапии больных HER2-позитивным РМЖ. (медана наблюдения 5,5 лет)
Неоадъювантная химиотарапия + анти-HER2 терапия | Неоадъювантная химиотарапия | |||
Число пациентов | Число пациентов с рецидивом n (%) | Число пациентов | Число пациентов с рецидивом n (%) | |
Органосохраняющие операции | 22 | 1 (4,5%) | 11 | 3 (27,2%) |
Мастэктомия | 74 | 6* (8,1%) | 77 | 10* (12,9%) |
*р=0.08
При более длительном периоде наблюдения (медиана наблюдения 5,5 лет) число местно-региональных рецидивов увеличилось, особенно в группе пациентов с HER2-позитивным РМЖ, получавших одну неоадъювантную химиотерапию без таргетной терапии (табл. 24).
5-летние отдаленные результаты лечения изучены у 82 больных, получавших неоадъювантную химиотерапию с анти HER2 терапией и у 83 больных, получавших одну (такую же как в основной группе) химиотерапию. За этот период зарегистрировано 33 события (местно-региональный рецидив, отдаленные метастазы, контралатеральный РМЖ, смерть) в основной (анти-HER2) группе т. е. у 40% пациентов и 44 «события» в группе одной неоадъювантной химиотерапией т. е. у 53% пациентов.
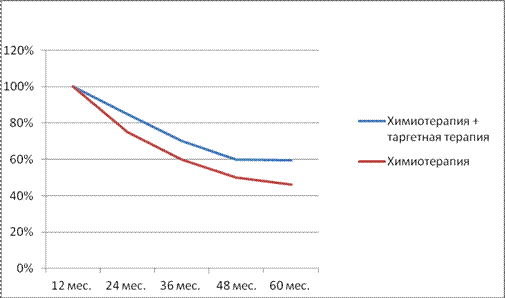
Рис. 17 Показатели 5-летней выживаемости без событий [EFS] у пациентов получавших химиотерапию + таргетную терапию против химиотреапии.
Показатель 5-летней выживаемости без событий [event-free survival - EFS] в группе таргетной терапии равнялся 59,7%, а в группе получавших одну химиотерапию 46,1% (р=0.024) (рис.17). Безотносительно объема операции (мастэктомия или органосохраняющая операция) наблюдаются такие же тенденции к более высокой выживаемости (EFS) в группах пациентов, получивших дополнительно к антрациклин таксаны-содержащей неоадювантной химиотерапии - анти - HER2 терапию.
Как уже указывалось, среди HER2-позитивных пациентов у 36% наблюдались ER/PR позитивные опухоли (у 29 пациентов основной и у 30 пациентов из группы одной неоадъювантной химиотерапии).
Эти пациенты отнесены в группу люминального В (HER2-позитивного подтипа РМЖ).
У пациентов люминальной группы (HER2+/ER+) оказались более низкие показатели без событийной выживаемости (EFS) 5-летней выживаемости 49% в основной (таргетной группе) и 36% в группе одной неоадъювантной химиотерапией [р=0.046].
Такие же тенденции более низкой выживаемости у пациентов люминальным В подтипом (HER2+/ER+) отмечены как после мастэктомии, так и после органосохраняющих операций (т. е. безотносительно объема операции) в группе таргетного неоадъювантного лечения.
Таким образом, проведение неоадъювантной системной терапии, вариант который определяется биологическим подтипом РМЖ, в большинстве случаев позволяет выполнить хирургический этап лечения, вплоть до органосохраняющих операций, особенно при люминальном А подтипе заболевания.
Заключение
Рак молочной железы — самое частое онкологическое заболевание женщин экономически развитых стран. Около 100 случаев РМЖ на 100000 населения регистрируется в странах Европы, в РФ Заболеваемость составила в 2012 г 41,6 и менее 20 случаев—в странах Азии. В 2011 году в целом по России учтено 57 875 случаев рака молочной железы, в том числе, среди женского населения—57534, среди мужского— 341 случай. В структуре онкологической заболеваемости женского населения России рак молочной железы занимает первое место 20,4%. В России ежегодно (2011) от рака молочной железы умирает более 23 000 (23 320) женщин.
Благодаря более широкому применения маммографии и ультразвукового обследования несколько увеличивается удельный вес относительно ранних стадий РМЖ подвергающихся лечению.
Вместе с тем число пациентов с местно распространенными опухолями (IIB, IIIA стадий) молочных желез, подвергающихся неоадъювантной терапии с последующим хирургическим этапом лечения, остается значимым (около 35 % по , 2012г.).
Несмотря на большой арсенал современных противоопухолевых препаратов и совершенство хирургической техники возникают рецидивы опухолей молочной железы, что крайне негативно влияет на ближайшие и отдаленные результаты лечения РМЖ.
В работе получены следующие результаты: Рецидивы чаще имели место в возрастной группе от 20 до 40 лет (9,3%), тогда как в остальных группах этот показатель колебался от 5,3 до 5,9%.
Обращает на себя внимание относительно не большой удельный вес люминальных А и В опухолей (49,9%). Преобладали опухоли с прогностически не благоприятным трижды-негативным РМЖ (41,3%). В значительной мере это связано с преобладанием IIIB стадии у женщин моложе 50 лет (47,2%). Средний возраст включённых в исследование пациентов равняется 47 годам. Известно, что в молодом возрасте реже встречаются гормонозависимые (ER/PR+) опухоли.
Чаще всего местные рецидивы развиваются в группе пациентов получавших «другие» схемы химиотерапии (CMF), риск развития рецидива увеличивается до 18,2%.
В 200 (69,9%) случаях была выполнена радикальная мастэктомия. В этой группе пациентов было диагностировано 6(3,0%) местных рецидивов. Рецидивы встречались у пациентов которые получали антрациклин содержащие и таксан содержащие режимы ПХТ в 4(3,9%) и 2 (3,6%) случаях соответственно.
Органосохраняющие операции были выполнены у 86 (31,1%) пациентов. Выявлено 11 (12,8%) рецидивов РМЖ. Рецидивы встречались при всех неоадъювантных режимах системной терапии.
На основании послеоперационного гистологического исследования выявлено 200(69,9%) пациентов с инвазивным протоковым РМЖ, количество рецидивов в этой группе составило 13 (6,5%) .
Рецидивы также встречались в группе больных с протоковым раком без инвазии In situ из 17 (5,9%) выявленных пациентов наблюдалась у 1 (7.7%) пациента, и в группе с pCR из 44(15,4%) больных выявлено у 3 (6.8%).
У пациентов с инвазивным дольковым раком 21 (7,3%) и дольковым раком без инвазии In situ 4 (1,4%) рецидивы не наблюдались.
Рецидивы опухоли преимущественно встречаются у пациентов с позитивными лимфатическими узлами.
При сравнительном анализе с другими подгруппами становится ясно что Люминальный А подтип РМЖ является самым безопасной группой для выполнения органосохраняющих операций после НАХ при местно-распространённом раке молочной железы.
При люминальном В HER2 позитивном подтипе РМЖ достоверной разницы возникновения рецидивов после радикальных мастэктомий и органосохраняющих операций не выявлено, но имеется тенденция к увеличению риска рецидива при выполнении органосохраняющих операций.
При трижды негативном подтипе РМЖ имеются некоторые отличия радикальных мастэктомий от органосохраняющих операций, с тенденцией к увеличению количества рецидивов при выполнении органосохраняющих операций с 2,9% при выполнении радикальных мастэктомий до 12,% после органосохраняющих операциях. Просматривается некоторая тенденция к более высокой частоте рецидивов у пациентов с HER2–позитивным и трижды негативным подтипами, подвергавшихся органосохраняющему лечению (18.2% и 12% соответственно).
При люминальном В HER2 негативном подтипе РМЖ имеется достоверная разница в возникновении рецидивов после радикальных мастэктомий и органосохраняющих операций. У пациентов с органосохраняющими операциями количество рецидивов доходит до 21,4% в группе пациентов с мастэктомиями это значение равно 1,9%.
Полный патоморфологический регресс после неоадювантной химиотерапии достигнут у 65 из 286 больных (т. е. в 22,7% случаев). Местный рецидив опухоли при 10-летнем сроке наблюдения возникли у 2 пациентов (3%). У 2 пациентов (6%), подвергавшихся органосохраняющим операциям. Таким образом, сужение объема хирургического вмешательства до органосохраняющей операции почти не сказывается на риске местного рецидива заболевания.
Больные достигшие полный клинический регресс, в основном (81 из 102, или 79,4%) подверглись органосохраняющему лечению с относительно редкими случаями возникновения местных рецидивов за 10 лет наблюдения.
Подавляющее число пациентов с частичным клиническим ответом на неоадъювантное лечение (180 из 184 или 97,8%) подверглись мастэктомии, также с редким возникновением местного рецидива (2,2%).
При 3й-4й степени патоморфологического регресса по Miller-Payne, местный рецидив возник у 15 из 221 пациентов (6,7%). Чаще местные рецидивы возникали при трижды-негативном и HER2-позитивном РМЖ у пациентов, подвергавшихся органосохраняющему лечению в сравнении с мастэктомией (p<0.05).
Полный патоморфологический регресс (pCR) [5 ст. по Miller Paine] достигнут у 65 (22,7%) , резедуальная опухоль [от II до IV степени регресса по Miller Paine] выявлена у 221 (77,3%) пациента.
У 33 больных достигших pCR выполнена органосохраняющая операция, у 32 радикальная мастэктомия. Частота возникновения местных рецидивов в группе органосохраняющего лечения равнялась 2(6,0%), у пациентов после радикальных мастэктомий 2 (6,3%)
Полученные данные свидетельствуют о том что при достижении полного патоморфологического рекгесса (pCR) после НАХ риск местного рецидива не зависит от объема хирургического вмешательства.
При патоморфологических признаках, обычно связываемых с угрозой рецидива, выяснилось, что расстояние от определяемой остаточной инвазивной опухоли до края хирургического препарата оказалось менее 5 мм у 17,1% пациентов из всех случаев местного рецидива, мультицентричность опухоли у 11,8%, наличие рядом с резидуальной инвазивной опухолью внутрирпротокового компонента (EIC) или дуктальной карциномы in situ (DCIS) у 11,8% пациентов. Удаление менее 8 подмышечных лимфоузлов у пациентов с метастазами в 4х и более лимфоузлах привело к региональному рецидиву в 11,7% случаев.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 |



