Второй раздел основан на ретроспективном анализе ранее проведенных в отделении клинических испытаниях, в том числе в рамках многоцентровых и международных протоколов. При этом в анализ включались только те пациенты, которые проходили обследование и лечение в НИИ онкологии им. .
По сути дела в работе рассматривается только два клинических испытания, начатых 8-10 лет назад. Прежде всего речь идет об изучении эффективности неоадъювантной эндокринотерапии в сравнении с химиотерапией у постменопаузальных женщин с ER-положительным местно-распространенным РМЖ. Второе испытание касалось пациентов с местно-распространенным HER2-позитивным РМЖ. Почему потребовался ретроспективный анализ этих рандомезированных перспективных исследований, результаты которых давно опубликованы? Дело в том, что в этих исследованиях, как и в подобных других испытаниях неоадъювантной ставились сначала узкие задачи: оценка частоты и величины клинического ответа, степени патоморфологических ответов и показателей перехода неоперабельных опухолей в операбельные.
Все указанные задачи остаются актуальными и в наше время. Но нас интересуют отдаленные последствия неоадъюванного лечения, сравнивая эффективность различных видов и режимов терапии. Успехи молекулярной генетики и широкое внедрение иммуногистохимических исследований опухоли позволяют определить биологический подтип РМЖ при анализе «ретроспективного материала».
Анализ непосредственных и отдаленных результатов неоадъювантной терапии в зависимости от биологического подтипа РМЖ позволяет определить наиболее адекватные и эффективные виды лечения этих опухолей.
В работе использована информация о пациентах, полученная из базы данных на более чем 5000 больных раком молочной железы (РМЖ), получавших лечение в отделении опухолей молочной железы НИИ онкологии им. проф. в период с 2000 года по 2012 год. В основу работы были положены как проспективные, так и ретроспективные данные.
База данных содержит следующую информацию:
1) возраст пациента на момент начала хирургического лечения или неоадъювантной терапии.
2) результаты диагностических методов исследования (маммография, ультразвуковое исследование молочных желез, пункционная биопсия, трепан-биопсия);
3) вид неоадъювантного системного лечения;
4) эффект неоадъювантного системного лечения по данным маммографии и ультразвукового исследования, оцененный по критериям RECIST 1.1 (частичный регресс, полный регресс, стабилизация, прогрессирование);
5) объем хирургического лечения;
6) гистологическое исследование операционного материала;
7) стадия заболевания согласно клиническим рекомендациям ESMO (2012г.);
8) степень гистологической злокачественности опухоли (G);
9) уровень экспрессии рецепторов эстрогенов (ER) и рецепторов прогестерона (PR), HER2, Ki67 (если определялись);
10) вид адъювантного лечения;
11) статус больного на протяжении 5, 10-летнего периода наблюдения (жив, умер, причина смерти, дата местно-регионарного рецидива, дата появления отдаленных метастазов и их локализация.
Рис.1 ДИЗАЙН КЛИНИЧЕСКОГО ИССЛЕДОВАНИЯ
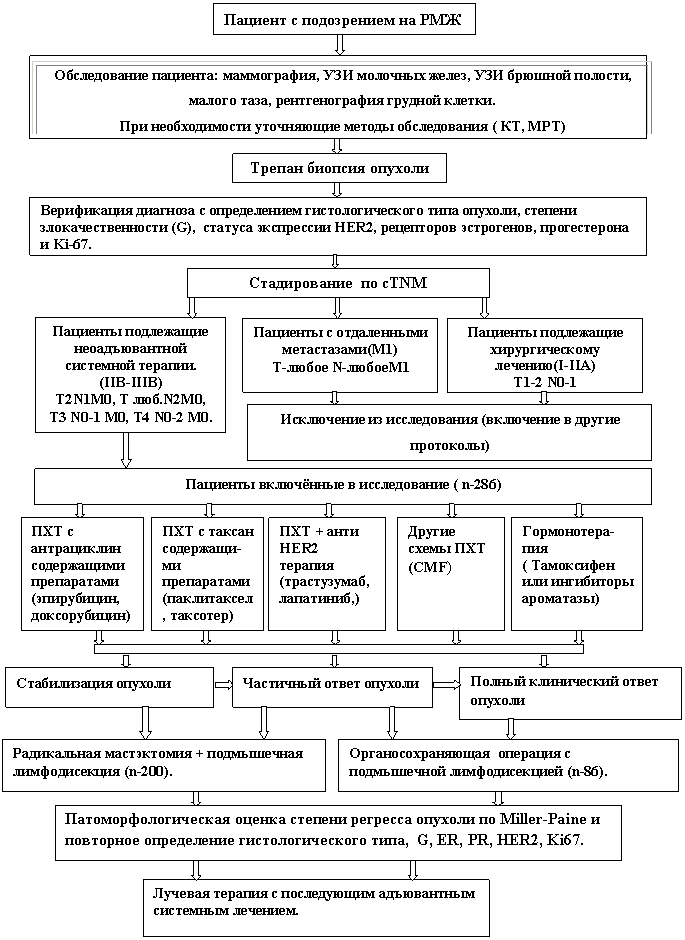
Из базы данных НИИ онкологии им. отобраны 286 больных с местно-распространённым (Т2-4N0-3M0) РМЖ получавшие неоадъювантную лекарственную терапию, с последующим выполнением хирургического этапа лечения (радикальная мастэктомия или органосохраняющая операция).
Непосредственным материалом исследования были истории болезни, амбулаторные карты, протоколы операций, данные телефонного опроса, информация, собранная в клинических отчетах, карт патоморфологического и иммуно-гистохимического исследований.
Критерии включения:
1) Гистологически подтвержденный РМЖ с IIB-IIIB стадиями.
2) Отсутствие отдаленных метастазов (M1), подтвержденное дополнительными методами исследований (УЗИ, радиоизотопные исследования (сканирование скелета), компьютерная томография грудной клетки, брюшной полости и малого таза, магнитно-резонансная томография у части больных).
3) Не менее одного измеряемого очага по категориям RECIST 1.1.
4) Фракция выброса левого желудочка ≥ 60%.
5) Нормальные гематологические и биохимические показатели крови.
6) Отсутствие тяжелой сопутствующей патологии, способной препятствовать проведению планируемого лечения или адекватному наблюдению.
7) Письменное согласие пациента.
Критерии исключения:
1) Наличие отдаленных метастазов (М1).
2) Билатеральный РМЖ.
3) Пациенты с тяжелой сопутствующей патологией, включая заболевания сердца по классификации NYHA класс ≥II.
4) Беременность и лактация.
5) Синхронные и метахронные злокачественные опухоли других локализаций в анамнезе.
6) Недавнее использование исследуемых препаратов.
Период включения в: исследование январь 2000- декабрь 2012г. Возраст больных включенных в группу исследования колебался от 23 лет до 81года, средний возраст пациенток составлял 47 лет. Самая многочисленная группа женщин, 151 (52,8%), принадлежала к возрастному интервалу от 51 года и старше, в группу больных от 41 до 50 лет вошли 92(32,2%) женщины и в группу от 20 до 40 лет вошли 43 женщины (15,0%). ( рис 2).
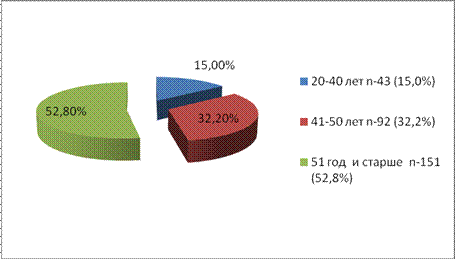
Рис. 2 Распределение пациентов по возрасту.
Как указано в дизайне исследования (рис 1) всем пациентам до начала лечения проведена трепан биопсия опухоли молочной железы.
Исследование производят под местной анестезией 0,5% раствором новокаина или лидокаина. С помощью специального биопсийного пистолета (система Bard-Magnum) эта процедура позволяет осуществить забор образцом тканей молочной железы достаточные для последующего патоморфологического исследования. Метод применяется для биопсии опухолей молочной железы с использованием стереотаксических адаптеров для фиксации к системным установкам(УЗИ, КТ, МРТ) и при работе вручную (рис 3).

Рис 3. Биопсийный пистолет для выполнения трепан биопсии.
После гистологической верификации диагноза больные проходили комплексное обследование включающее в себя: маммографию, УЗИ молочных желез, УЗИ брюшной полости, малого таза, рентгенографию грудной клетки, остеосцинтиграфию, компьютерную томографию (КТ) грудной клетки, брюшной полости и малого таза. При неясных заключениях УЗИ и маммографии выполняли магнитно резонансная томография (МРТ) молочных желез.
Пациенты были разделены на группы в зависимости от клинической стадии (сTNM) заболевания, до проведения неоадъювантной системной терапии (табл. 1).
Табл. 1. Распределение пациентов по сTNM до начала неоадъювантной системной терапии.
Стадии до операции по cTNM | Количество пациентов n (%). |
T2N1 | 62 (21,7%) |
T3N0 | 14 (4,9%) |
T1N2 | 5 (1,7%) |
T2N2 | 44 (15,4%) |
T3N1 | 50 (17,5%) |
T3N2 | 30 (10,5%) |
T4N0 | 12 (4,2%) |
T4N1 | 34 (11,9%) |
T4N2 | 5 (10,5%) |
TлюбаяN3 | 5 (1,7%) |
Всего | 286 (100,0%) |
При патоморфологическом исследовании определялись следующие параметры:
1. Гистологический тип рака – инвазивный протоковый, дольковый и другие особые (формы);
2. Степень инвазии опухоли (инвазивный рак, инвазивный рак с выраженным интрадуктальным компонентом или инвазией жировой клетчатки, мышц или других анатомических структур );
3. Размер опухоли (в наибольшем измерении);
4. Характер роста опухоли (отграниченный или инфильтрирующий);
5. Оценка степени злокачественности (G) опухоли по Bloom и Richardson в модификации Elston-Ellis (I степень злокачественности – низкая, с суммарным количеством баллов от 3 до 5 баллов; II степень злокачественности – промежуточная – умеренная, степень соответственно 6-7 баллов; III степень злокачественности – высокая, 8-9 баллов);
6. Количество пораженных метастазами лимфатических узлов/ количество удаленных лимфоузлов.
7. Иммуногистохимическое определение экспрессии рецепторов эстрогенов (ER) и прогестерона (PR). Для оценки результатов экспрессии ER и PR использовалась (Allred Score) балльная шкала, в которой учитывается не только процент окрашенных клеток, но и степень выраженности экспрессии антигена (0-2 балла - негативный результат; 3-5 балла позитивный результат; 6-8 баллов – высокая экспрессия).
8. Для оценки экспрессии HER2 использовали градации: 0- отсутствие окрашивания; 1+ - слабое окрашивание мембраны опухолевых клеток; 2+ - средняя интенсивность окрашивания более 10% опухолевых клеток; 3+ - сильная степень окрашивания более 30% опухолевых клеток. Опухоль, оцениваемую как 0 или 1+ считали HER-2- отрицательной, а 2+ - потенциально положительный, 3+ - положительной по HER2/neu. При окрашивании (2+) препарат опухоли направлялся на FISH-тест для определения амплификации гена и HER2-позитивности.
ER и\или PR позитивные опухоли выявлены у 124 пациентов (43,4%), рецептор-негативные опухоли оказались у 162 пациентов (56,6%).
На основании ИГХ, степени злокачественности опухоли (G) пациенты были распределены на биологические подтипы РМЖ до проведения системного неоадъювантного лечения (рис 4).
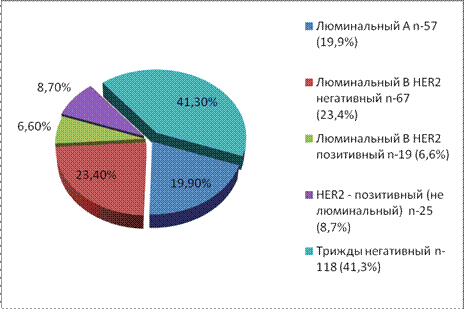
Рис. 4 Биологические подтипы РМЖ по данным имммуногистохимического исследования трепан биопсии (до неоадъювантного системного лечения)
Обращает на себя внимание относительно не большой удельный вес люминальных опухолей (49,9%), а люминальный А всего 19,9%. Преобладали опухоли с самым прогностически не благоприятным трижды-негативным РМЖ (41,3%). В значительной мере это связано с преобладанием IIIB стадии у женщин моложе 50 лет (47,2%). Средний возраст включённых в исследование пациентов равняется 47 годам. Известно, что в молодом возрасте реже встречаются гормонозависимые (ER/PR+) опухоли.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 |



