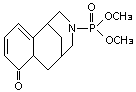
Результаты II фазыклинических испытаний: «Оценка эффективности и безопасности препарата «Цитафат» (ТОО «Карагандинский фармацевтический завод», Казахстан) в дозе 10 мг/кг при в/в капельном введении в 200 мл стерильного 5% раствора глюкозы у больных с токсическим поражением/алкогольной болезнью печени».Каждому пациенту вводился или исследуемый препарат Цитафат, или плацебо или референтный препарат (сравнения) Эссенциале. Анализ общего характера и спектра гепатопротекторного действия исследуемых препаратов проводился с учетом динамики ферментных проб печени, кроме этого, детальному изучению были подвергнуты данные субъективного самочувствия пациентов, а также данные УЗИ обследований. При оценке эффективности препаратов учитывалось, что его назначение происходило в комплексе с другими лекарственными средствами согласно утверждённых клинических протоколов диагностики и лечения токсических гепатопатий в зависимости от вида отравления.
Таким образом, результаты, полученные в ходе проведения II фазы клинического испытания «Оценка эффективности и безопасности препарата «Цитафат» (ТОО «Карагандинский фармацевтический завод», Казахстан) в дозе 10 мг/кг при в/в капельном введении в 200 мл стерильного 5% раствора глюкозы у больных с токсическим поражением/алкогольной болезнью печени» показали наличие у исследуемого препарата Цитафатцитопротекторного, гипохолестеринемического и сахароснижающего эффектов при хорошей переносимости и безопасности.
Результат исследования показывает, что гепатопротекторная активность нового препарата «Цитафат», по предварительным данным клинических исследований, в 7-8 раз превышает самый сильный на сегодняшний день гепатопротектор – германский препарат «Эссенциале».
Подтверждением успешной терапии препаратом «Цитафат» является не только быстрая нормализация основных биохимических показателей функционирования печени (АЛТ, АСТ, билирубин, ХС, сахар крови, ГГТП, амилаза, ЩФ) по сравнению с группой «Эссенциале» и плацебо в рамках краткосрочной терапии препаратом «Цитафат», но и достижением частичного клинического эффекта на 3 сутки терапии и положительная УЗИ динамика у большинства пациентов. В связи с чем, рекомендуется продолжить исследования «Цитафата» в III фазе на большем количестве пациентов и сделать окончательные выводы о его эффективности и безопасности.
4.7 Изучение антиоксидантной активности на вольтамперометрическом анализаторе СТА [78]
Исследования проводили на вольтамперометрическом анализаторе СТА в комплекте с ПК. В работе использовали метод катодной вольтамперометрии. В качестве модельной реакции рассматривали процесс ЭВ О2, который идентичен восстановлению кислорода в клетках и тканях организма. Для оценки влияния исследуемых веществ рассматривали зависимости предельного тока первой волны ЭВ О2 от концентрации их в объеме раствора и от времени протекания процессаЭВ О2 в их присутствии.
Вопросы кислородного метаболизма в организме человека являются объектами постоянного внимания медиков, химиков и биохимиков. Особенно сейчас, когда очевидно, что избыточное содержание кислорода и его активных радикалов вызывают радикально-цепные процессы окисления в клетках организма, приводя к значительным нарушениям в их нормальном метаболизме.
Активность образца определяли, используя метод катодной вольтамперометрии, в частности процесс электровосстановления кислорода (ЭВ О2). Модельная реакция ЭВ О2, протекает на электроде по механизму, аналогичному восстановлению кислорода в тканях и клетках организма:
О2 + е–![]() О2я - (1)
О2я - (1)
О2я - + Н+![]() HO2я (2)
HO2я (2)
HO2я + Н+ + е-![]() Н2О2 (3)
Н2О2 (3)
Н2О2 + 2Н+ + 2е-![]() 2Н2О (4)
2Н2О (4)
В данном случае рассматривается первая волна ЭВ О2 (восстановление кислорода до пероксида водорода) с образованием активных кислородных радикалов: О2-, НО2-⋅ (выражения 1-3). Предполагается, что вещества реагируют с кислородом и его активными радикалами на поверхности индикаторного электрода, что отражается в изменении катодного тока ЭВ О2. [6]. Методика эксперимента [79] заключалась в съемке вольтамперограмм катодного ЭВ О2 с помощью вольтамперометрического анализатора, подключенного совместно с ПК. Использовался постоянно-токовый режим катодной вольтамперометрии, скорость развертки потенциала W= 30 мВ/с, рабочий диапазон потенциалов от 0.0 до –0.7 В, время перемешивания раствора 20 сек, время успокоения 10 сек. Электрохимическая ячейка представляла собой стеклянный стаканчик с раствором фонового электролита и опущенными в него индикаторным ртутно-пленочным электродом, хлорид-серебряным электродом сравнения и хлорид-серебряным вспомогательным электродом. В качестве фонового раствора выбран фосфатный буфер с рН 6.86, близкому к физиологическому значению, объемом 10 мл. Активность исследуемого вещества по отношению к ЭВ О2 определялась по следующей методике: снимались вольтамперограммы тока ЭВ О2 в отсутствии исследуемого вещества (фоновая кривая) по описанному выше способу. При отсутствии посторонних пиков фоновый раствор считался чистым. Затем в ячейку добавлялось исследуемое вещество с известной концентрацией (брали объем аликвоты 0.1 мл на 10 мл объема фонового электролита) и снималась катодная вольтамперограмма ЭВ О2 при тех же условиях. Измерения повторялись не менее 3 раз через определенный промежуток времени (180 с) и каждый раз оценивалось значение предельного тока ЭВ О2.
Изменение тока ЭВ О2 по своему абсолютному значению свидетельствует о том, что исследуемый образец реагируют с кислородом и его активными радикалами, в исследуемом растворе. Степень изменения тока ЭВ О2 являлась показателем активности исследуемого образца.
По полученным данным строилась зависимость относительного изменения тока ЭВ О2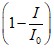 от времени протекания процесса в присутствии одной концентрации исследуемого образца.
от времени протекания процесса в присутствии одной концентрации исследуемого образца.
По линейной части графика и по тангенсу угла наклона касательной к данному участку кривой рассчитывался коэффициент активности образцов — K, мкмоль/(л⋅мин) по формуле:
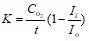 , (5)
, (5)
где Со2– концентрация кислорода в исходном растворе без вещества, мкмоль/л;
Ii – текущее значение предельного тока ЭВ О2, мкА;
Iо‑ значение предельного тока ЭВ О2 в отсутствии вещества в растворе, мкА;
t‑ время протекания процесса, мин.
Обсуждение результатов
Влияние образца на процесс ЭВ О2 проявилось в уменьшении катодного тока, что свидетельствует об антиоксидантном действии образца по отношению к образующимся в ходе электродного процесса радикалам кислорода. Кроме того, наблюдался сдвиг потенциала катодного тока ЭВ О2 в положительную область потенциалов. Все вышесказанное предполагает наличие механизма ЕС (электрохимическая-химическая стадии), который включает последующую химическую реакцию взаимодействия антиоксидантов с активными кислородными радикалами. Общую схему наблюдаемого электродного процесса с последующими химическими реакциями взаимодействия антиоксидантов с активными кислородными радикалами можно выразить следующим образом (рис. 4.4).
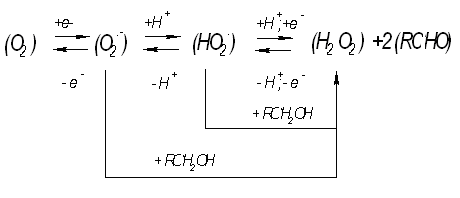
Рисунок 4.4- Схема взаимодействия антиоксидантов с активными формами кислорода, образующимися в процессе ЭВ О2.
Антиоксидантную активность образца определяли, используя выражение (5).результаты представлены в таблице 4.1
Как видно из таблицы 4.1, антиоксидантное действие образца 1 по отношению к образующимся радикалам кислорода более выражено, что и наблюдается в увеличении коэффициента К.
Таблица 4.1- Антиоксидантная активность образца №1по отношению к ЭВ О2, (n=5, p=0.95)
Концентрация | Среднее значение, K, мкмоль/л мин | Стандартное отклонение, S | Относительное стандартное отклонение, Sr | Стандартное отклонение среднего, Sx | Доверительный интервал, Д |
| |||||
0,00001 г/мл | 0,183 | 0,032 | 0,174 | 0,019 | 0,05 |
0,0001 г/мл | 0,280 | 0,012 | 0,043 | 0,007 | 0,02 |
0,001 г/мл | 0,399 | 0,045 | 0,113 | 0,026 | 0,07 |
Таким образом, исследуемый образец значительно влияет на процесс ЭВ О2, уменьшая катодный ток, при этом наблюдался сдвиг потенциала катодного тока ЭВ О2 в положительную область потенциалов. Взаимодействие с кислородными радикалами для образца соответствует схеме на рисунке 4.4

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 |