При сравнении спектров аминофосфонатов 1a-h и цитизина наблюдается сдвиг сигналов протонов С8. Это, по-видимому, связано с тем, что неподеленная пара электронов соседнего атома азота, занимающая экваториальное положение в цитизине, при замещении атома водорода на более сложный радикал, становится аксиальной. Благодаря этому становится возможной делокализация неподеленной пары электронов на разрыхляющую орбиталь С-Н связи, что приводит к увеличению экранирования этих протонов.
Помимо сигналов протонов, характерных для алкалоидной части молекулы в спектре имеется интенсивный сигнал шести протонов СН3О группы в области 3,69 м. д. с КССВ, равной 3JРН = 10,5 Гц. Протоны СН3-С группы дают интенсивный синглет в сильном поле при 0,88 м. д.
Рентгеноструктурное исследование (рисунок 2.1), проведенное на примере диметил-2-(N-цитизинил)-2-изобутилфосфоната 1f, подтверждают структуру синтезированных аминофосфонатов 1a-h.

Рисунок 2.1 – Молекулярная структура диметил-2-(N-цитизинил)-2-изобутилфосфоната 1f.
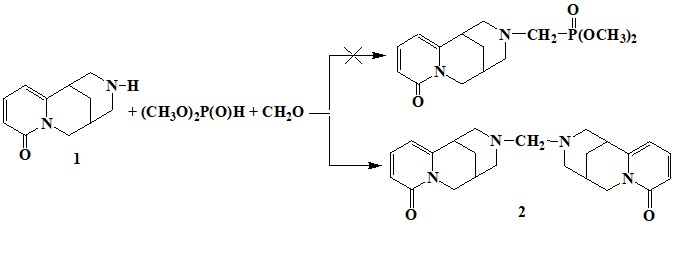
При использовании в качестве карбонильного соединения – параформа в условиях реакции Кабачника-Филдса, реакция протекает с образованием N, N-дицитизинилметана 2 [52]. Установлено, что диметилфосфит не успевает участвовать в реакции, т. к. цитизин быстрее конденсируется с формальдегидом с образованием соответствующего продукта конденсации 2. Это обусловлено, по-видимому, большей нуклеофильностьюцитизина по сравнению с диметилфосфитом и высокой реакционной способностью формальдегида.
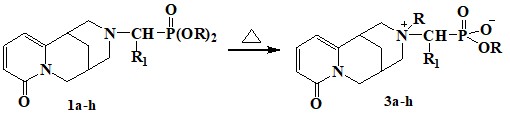
При изучении влияния температурного фактора на выходы целевых аминофосфонатов цитизина 1a-h авторами работы [56] установлена возможность превращения их во внутренние соли 3a-h. Образование внутренних солей (до 20%) аминофосфонатов 1a-h наблюдалось при увеличении продолжительности кипячения реакционной смеси цитизин-альдегид-диалкилфосфит в бензоле (до 5 ч и более) или проведении реакции в более кипящих растворителях (диоксан, толуол, ксилол). Установлено, что с уменьшением алкилирующей способности аминофосфонатов, т. е. с увеличением эфирного радикала при атоме фосфора, уменьшается количество образующегося остатка и выход целевых аминофосфонатов повышается.
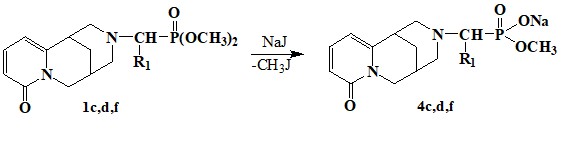
При синтезе фосфорильных соединений деалкилированием эфирной группы можно получить водорастворимые их производные. Так, в [57] осуществлено моно-деалкилирование диметил-2-(N-цитизинил)-2-алкил(арил)фосфонатов 1c, d,f с эквимолярным количеством иодид-ионов в абсолютном ацетоне. Синтезированные натриевые производные аминофосфонатов цитизина 4c, d,f представляют собой белые с желтоватым оттенком порошкообразные вещества, легко растворимые в воде и спирте.
Синтезированные аминофосфонатные производные цитизина 1c, d,f прошли первичные испытания на гепатопротекторную активность. В результате скрининговых исследований установлено, что соединение диметил-2-(N-цитизинил)-2-изобутилфосфонат 1f оказывает защитное действие при отравлении гепатотропным ядом ССl4 и обладает выраженным гепатопротекторным действием.
2.3 Синтез фосфорпроизводного природного алкалоида цитизин – О, О-диметил-N-цитизинилфосфата
Фосфорорганические соединения со связью P-N представляют одну из больших групп среди фосфорсодержащих лекарственных препаратов. Методы получения биологически важных амидофосфатов хорошо изучены и широко используются в препаративной химии. Одним из методов синтеза амидофосфатов на основе аминов является реакция Тодда-Атертона. Взаимодействие диалкилфосфористых кислот с алкалоидом цитизином в условиях реакции Тодда-Аттертона осуществляли в среде бензола в присутствии четыреххлористого углерода и триэтиламина по следующей схеме [49]:
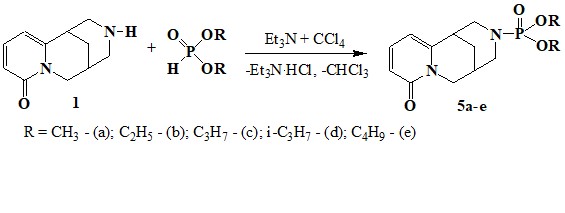
Синтезированные амидофосфаты 5а-е с метильным и изопропильным радикалами представляют собой белые кристаллические вещества.
В спектрах ИК соединений 5а-е присутствуют интенсивные полосы поглощения, характерные для фосфорильной группы (Р=О) с максимумом 1265-1270 см-1, в интервале частот 1025-1050 см-1 наблюдается полосы для Р-О-С-группы, а в области 825-835 см-1 расположены полосы поглощения для связи P-N.
При анализе ЯМР 1Н спектра амидофосфата 5а наряду с сигналами протонов для алкалоидной части присутствуют сигналы неэквивалентных метокси-группы, которые проявляются в виде дублета дублетов в области 3,20-3,55 м. д., что является следствием спин-спинового взаимодействия с ядром атома фосфора.
При анализе спектра ЯМР 1Н О, О-диметил-N-цитизинилфосфата5а три группы сигналов низкого поля соответствуют протонам α-пиридинового ядра. Сигналы при 7,30 м. д. соответствуют β-протону. Расщепленный дублет при 6,09 м. д. соответствует γ-протону, а расщепленный дублет при 6,36 м. д. - α-протону. Следующая группа линий, представляющая собой сложный сигнал в области 3,81-4,12 м. д. соответствует аксиальному и экваториальному протонам в положении С10. Эта группа сигналов является АВ-частью системы АВХ, где Х – протон в положении С9. Экваториальный протон при С10 смещен в более слабое поле по сравнению с аксиальным. Группа линий в области 3,52-3,60 м. д. представляет собой сигналы пяти протонов, находящихся при С11, С13 и третичного протона С7. Протоны метокси-группы у атома фосфора неэквивалентны и они проявляются в области 3,30 и 3,44 м. д. в виде двух расщепленных дублетов. Два третичных протона в положениях С7 и С9 у метиленового мостика не эквивалентны, так как протон при С7 находится в α-положении к двойной связи и подвержен влиянию анизотропии к ней, вследствие чего смещен в более слабое поле (δ 3,03-3,10 м. д.) относительно протона С9. А широкий синглет в области 2.43 м. д. принадлежит протону С9. Группа линий в области 1,91-2,03 м. д. относится к протонам С8.
С целью установления пространственного строения амидофосфатов было проведено рентгеноструктурное исследование О, О-диметил-N-цитизинилфосфата 5а (рисунок 2.2). Установлено, что координация атома фосфора в исследуемом соединении – искаженная тетраэдрическая, обычная для фосфатных группировок. Дигидропиридиновый цикл плоский, карбонильный атом кислорода отклоняется от этой плоскости незначительно. Тетрагидропиридиновый цикл принимает конформацию софы. Пиперидиновый цикл имеет почти идеальную конформацию кресла.
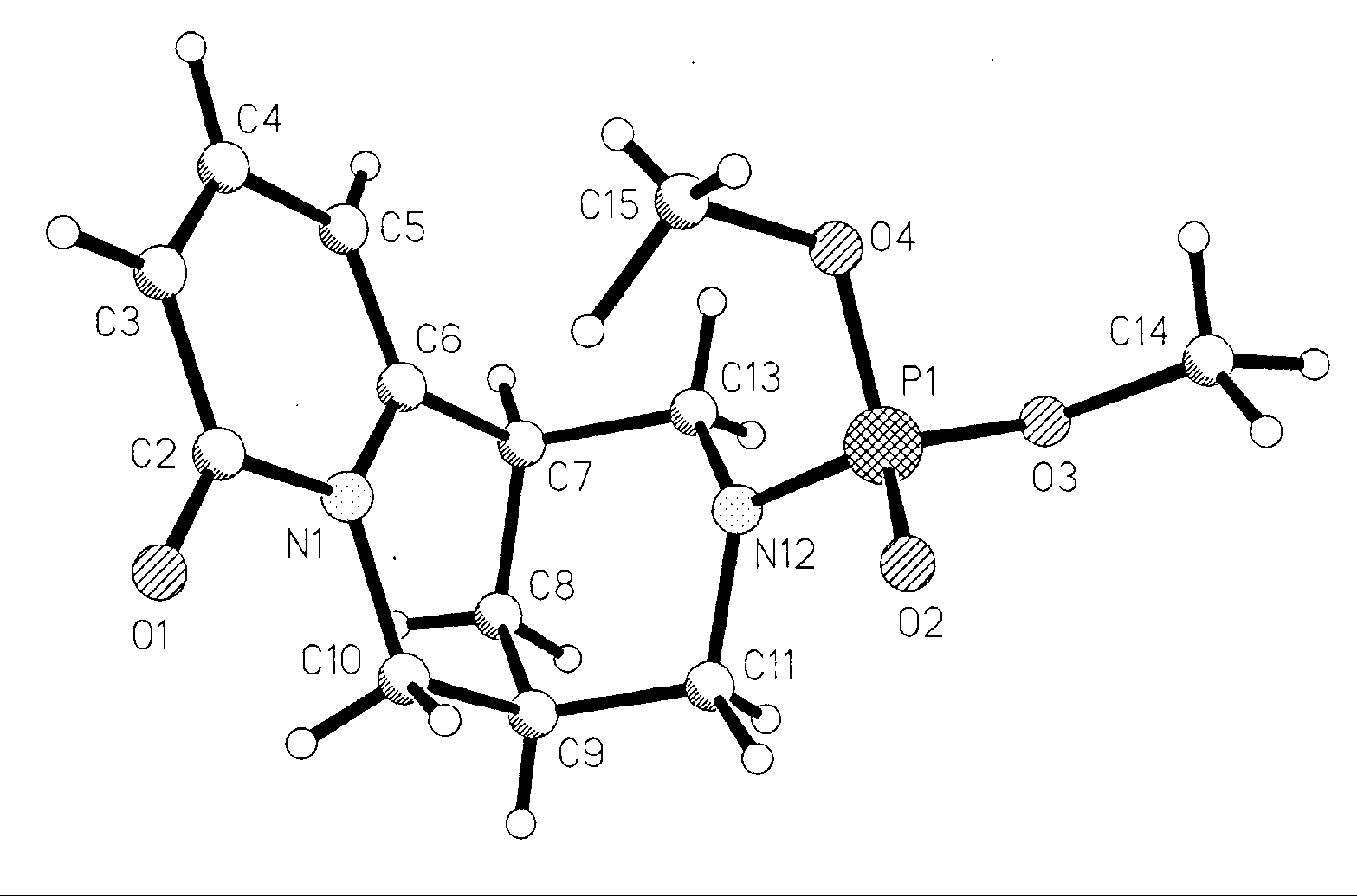
Рисунок 2.2 - Общий вид молекулы О, О-диметил-N-цитизинилфосфата 5а
С целью повышения выхода О, О-диметил-N-цитизинилфосфата 5а изучено взаимодействие цитизина с диметилфосфитом в условиях межфазного катализа в присутствии каталитических количеств 18-краун-6 [58]. Процесс проводили при комнатной температуре, в качестве растворителя использовали смесь бензола и тетрагидрофурана в соотношении 3,5:1. Сравнительный анализ результатов синтеза показал, что в условиях реакции межфазного катализа целевой продукт образуется с более высоким (на 10-12%) выходом по сравнению с процессом, проведенным в классических условиях реакции Тодда-Атертона.
Амидофосфаты 5b, c,е описаны и в работе [59].
В [60] описывается препаративный электросинтез О, О-диалкил-N-цитизинил-фосфатов 5а-е. Изучение электрохимического поведения цитизина позволило определить условия для получения амидофосфатов электрохимическим методом (рисунок 2.3). Анодное поведение цитизина изучено на стационарном и вращающемся платиновом и графитовом электродах в ацетонитриле на фоне NaClO4. На вольтамперограммахцитизина как на платине, так и на графите наблюдаются две необратимые волны окисления. Порядок реакции электроокисленияцитизина для области потенциалов 0,4-1,0 В (для первой волны) и концентрация субстрата ниже 1⋅10-2 М составляет 0,60-0,68, значение кажущегося коэффициента переноса равно 0,35±0,07 на платине и графите соответственно. Отсутствие независимости величины предельного тока от числа оборотов вращающегося дискового электрода свидетельствует о кинетической природе электродного процесса.
Препаративный электросинтез ацетонитрильного раствора смеси цитизина и диалкилфосфористых кислот в присутствии каталитических количеств иодид-ионов приводит к синтезу О, О-диалкил-N-цитизинилфосфатов 5а-е [60]. Максимальный выход продуктов 5а-е (65-70%) наблюдается на платиновых электродах при плотности тока 4-5 мА/см2, что соответствует области потенциалов окисления иодид-ионов (Еа = 0,40-0,45 Вотн. 0,01 М Ag/AgNO3 в ацетонитриле).
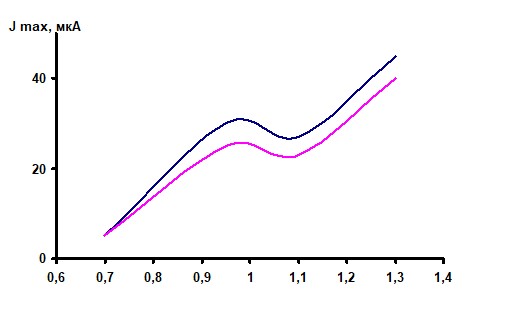
Рисунок 2.3 – Вольтамперограмма окисления цитизина (5⋅10-3 М) на
платиновом электроде в ацетонитриле на фоне 0,1 М растворе NaClO4 при различныхскоростях развертки потенциалов V, мВ/с: 1, 3 – 40; 2 – 20; 4 – 80
Известно, что в химии фосфорсодержащих природных веществ долгое время применялись почти исключительно классические методы фосфатной химии. Богатые возможности химии соединений трехвалентного фосфора с этой целью долго не использовались. Так, в работе [61] с целью расширения арсенала биологически активных веществ на основе алкалоида цитизина осуществлен синтез О, О-диалкил-N-цитизинилфосфитов6а-е, взаимодействием вышеуказанного алкалоида с диалкилхлорфосфитом в токе сухого аргона в присутствии триэтиламина.
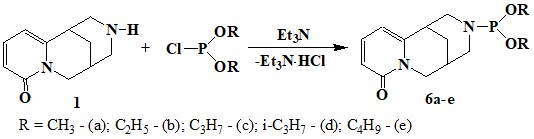
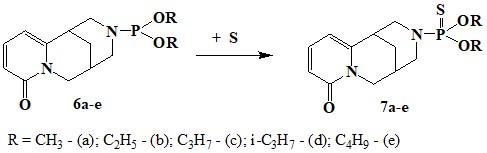
Cоединения трехвалентного фосфора, обладая высокой нуклеофильностью, легко взаимодействует с электрофильным реагентом и при этом увеличивается координационное число атома фосфора. Так, взаимодействием О, О-диалкил-N-цитизинилфосфитов6а-е, с элементной серой получены соответствующие амидотионфосфаты7а-е.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 |



