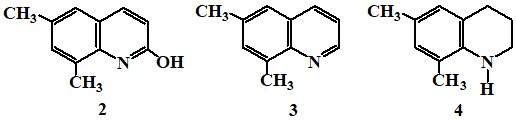
Инг [24] показал, что цитизин содержит ядроα-пиридона и образование производных хинолина связано с некоторыми внутримолекулярными изменениями. Наличие α-пиридона, лактамной группы и сопряженной системы двойных связей в молекуле цитизина доказаны также данными ИК - и УФ-спектров [25]. В ИК-спектре алкалоида имеются полосы поглощения NH-группы (3350 см-1), лактамной группы (1640 см-1) и сопряженной двойной связи (1600-1500 см-1). В УФ-спектре цитизина имеются максимумы (234, 310 нм), характерные для α-пиридона. Исследование ЯМР 1Н-спектра цитизина показало, что расположение сигналов протонов α-пиридинового ядра в более сильных полях, чем расположение сигналов производных пиридина и бензола, обусловлено тем, чтоα-пиридоновый цикл не является полностью ароматическим [25].
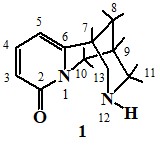
В ЯМР 1Н-спектре цитизина 1, записанного на спектрометре Bruker DRX500 с частотой 500 МГц в растворе DMSO-d6относительно внутреннего стандарта ТМС три группы сигналов низкого поля соответствуют протонам пиридинового ядра. Сигнал в виде двух дублетов при 7,37 м. д. соответствуют H-4 протону с константами спин-спинового взаимодействия J4,3 = 9,03 Гц, J4,5= 6,86 Гц. Дублет при 6,30 м. д. относится к Н-3 протону (J3,4 = 9,02 Гц) и дублет при 6,19 м. д. – Н-5 протону с J5,4 = 6,75 Гц. Следующая группа линий, представляющая собой сложный сигнал в области 3,74-3,96 м. д. (проявляется дублетом при 3,94 м. д. с высокой J = 15,7 Гц и дублет дублетом при 3,77 м. д. с J = 6,92 Гц, J = 15,71 Гц) соответствует Н-10е экваториальному и Н-10а аксиальному протонам. При этом экваториальный протон Н-10е при С10 смещен в более слабое поле по сравнению с аксиальным. Группа линий в области 3,10-3,35 м. д. представляет собой сигналы от пяти протонов Н-11, Н-13 и третичного протона Н-7. Широкий сигнал с центром 2,61 м. д. соответствует третичному протону Н-9. Два третичных протона в положениях С7 и С9 у метиленового мостика не эквивалентны, так как один из них – протон при С7 – находится в α-положении к двойной связи дигидропиридинового кольца и подвержен влиянию анизотропии к ней, вследствие этого смещен в более слабое поле относительно протона при С9. Метиленовые протоны Н-8 проявляются в самой сильной области спектра при 1,86 и 2,01 м. д. двумя уширенными дублетами с J = 13,09 Гц. N-H-протон, вследствие высокой полярности растворителя, проявляется широким синглетом при 9,20 м. д. В структуре цитизина имеется два асимметрических углеродных атома и теоретически для него возможно существование двух пар рацематов. Однако тщательное рассмотрение конфигурации на моделях показывает, что в цитизинемета-метиленовый мостик жестко закреплен в цис-положении, поэтому для него возможно только одна рацемическая пара. Правовращающая форма цитизина в природе не найдена. В [25] приведены результаты квантово-химических расчетов электронного строения алкалоида цитизина, проведенных с использованием метода ССП МО ЛКАО в приближении MINDO/3. Установлено, что молекула цитизина характеризуется большой поляризацией электрических зарядов на атомах в той части молекулы, которая содержит сопряженные двойные связи, что наибольший частичный положительный заряд имеет атом углерода амидной функции. Установлено также, что теплота образования ∆Hf = 245,213 кДж/моль, а полная энергия Еполн = -2243,5502 эВ. Энергия верхней занятой молекулярной орбитали (ВЗМО) определяет потенциал ионизации молекулы цитизина, равной ∆J = 8,6919 эВ. Электронное сродство молекулы цитизина равно – 0,081 эВ, что соответствует энергии низшей свободной молекулярной орбитали.
1.3 Реакционная способность алкалоида цитизина и его производных
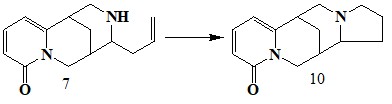
Цитизин несет в своей структуре два асимметрических центра, несколько функциональных групп, и может быть с успехом использован в качестве исходной хиральной матрицы для синтезов более сложных природных объектов. Так в [26], при действии на цитизин хлорной известью образуется N-хлорцитизин 5, который под действием щелочи легко отщепляет хлористый водород и дает 11,12-дегидроцитизин 6. При взаимодействии с аллилмагнийбромидом соединение 7 образует 11-аллилцитизин 8, конденсация которого с формальдегидом приводит к образованию эпибаптифолина, из которого гидрированием получен l-тетрагидробаптифолин 9, являющийся 13-гидроксилупанином.
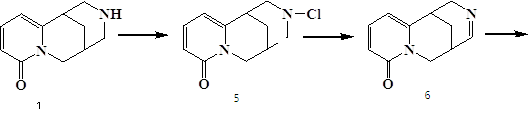
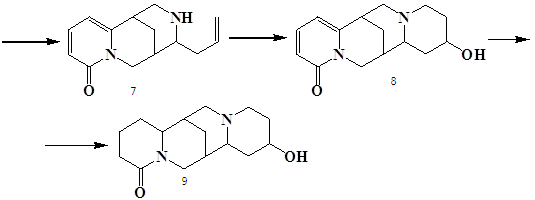
При обработке йодистоводородной кислотой 11-аллилцитизин 7 переходит в леонтидин 10. Его структура подтверждена синтезом из цитизина [27].
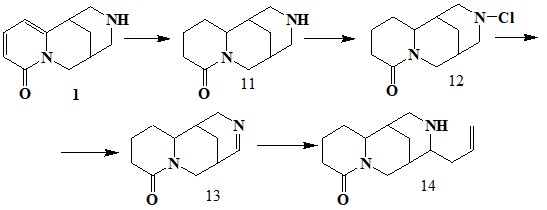
Гидрирование цитизина над никелем Ренея до тетрагидроцитизина 11 с последующей обработкой хлорной известью приводит к N-хлортетрагидроцитизину 12, который превращается в основание 13, конденсация которого с аллилбромидом приводит к получению ангустифолина 14 [2].
Абсолютная конфигурация цитизина и родственных ему алкалоидов была установлена на основании конфигурации l-анагирина 5, которую определяли расщеплением его до (+)-эпилупинина [23,24].
При окислении анагирина 15 марганцевокислым барием был получен анагирамид 16, озонирование которого дает дилактам 17.
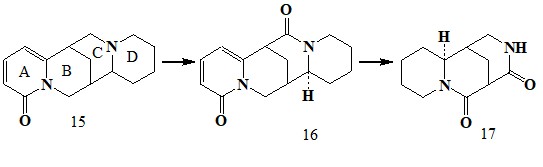
Дилактам 17 имеет тот же скелет, что (-)-цитизин, но у первого кольцо А является насыщенным, пиперидиновым, а у второго - α-пиридиновым. Цитизин в некоторых реакциях проявляет ароматический характер. При бромировании и хлорировании образуется дигалогенпроизводное, причем вторичная аминогруппа остается незатронутой [25-27]. В [28] проведена оценка эффективности методик бромированияцитизина с помощью NBS и молекулярным бромом. Электрофильноебромирование NBS проводят при кипячении, используя в качестве растворителя хлороформ вместо CCl4, из-за низкой растворимости цитизина в последнем. При мольном соотношении исходных реагентов цитизин : NBS = 1:1,5, с общим выходом 65% была получена смесь трех продуктов: 3,5-дибромцитизин 18а, 3-бромцитизин 18б и 5-бромцитизин 18в в соотношении 1:2:2.
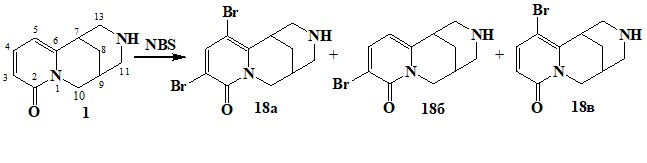
Проведение реакции при фотооблучении (кварцевая лампа ПРК-2) в ацетонитриле привело к изменению соотношения продуктов реакции: были получены все три региоизомера в соотношении 1:1:1 с общим выходом 48%. Бромирование с применением NBS в уксусной кислоте привело к иному соотношению продуктов – соответствующие бромиды образуются с выходом 59% в соотношении 1:5:3. Бромирование цитизина действием четырехкратного избытка молекулярного брома в уксусной кислоте дало единственный продукт – 3,5-дибромцитизин с выходом 92%. Замена растворителя на хлористый метилен, понижение температуры реакции до -5оС и использование соотношения реагентов 1:1,1 позволило получить в качестве основного продукта 3-бромцитизин 18б (соотношение 18а:18б:18в составило 1:6:1).Общий выход продуктов реакции составил 77%. Понижение температуры реакции до -30оС позволило увеличить долю 5-бромцитизина 31в, при выходе 60% соотношение изомерных бромидов составило 1:5:5. [30] и [29] также осуществили реакцию бромирования цитизина и N-метилцитизина и детально изучили ЯМР 1Н-спектры исходных соединений и бромированных продуктов. Показано, что при использовании одного моля брома получаются 3-бромцитизин 18б, а двух молей брома –5-бромцитизин 18в. В соединениях 1 и 18б сигналы протонов Н-8 и частично Н-11 проявились сложными мультиплетами с неразрешенной мультиплетностью. В [15] исследована возможность электрохимической функционализации алкалоида цитизина. Электросинтез проводился в термостатированной ячейке без диафрагмы, с графитовым или платиновым анодом и никелевым катодом при соблюдении соотношения площадей поверхности электродов Sa = 10·Sк. Процесс идет при ia = 0,6 А/дм2 и t = 25oC в метанольном растворе H2SO4 (0,4 М) и NH4Br (0,01 М) в присутствии 0,25-0,3Мцитизина. Результаты препаративного электросинтеза при контролируемом потенциале показали, чтоосновной продукт, идентифицированный как 3,4-диметокси-3,4-дигидроцитизин 19, образуется при ц≥1,0 В. На основании анализа результатов, полученных при проведении электрохимических измерений и спектрального анализа предложена следующая схема образования основного продукта электролиза:
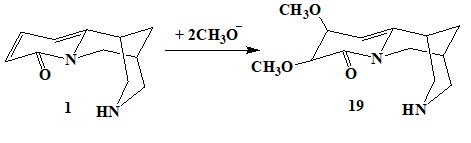
В [30] проведено исследование цитизина на его способность ингибировать радикально-цепное окисление. Показано, что цитизин проявляет свойства ингибитора, обрывающего цепи по реакции с пероксидными радикалами. По эффективности он превосходит 6-метилурацил на два порядка и в два раза активнее ингибиторов пипиридинового ряда [31, 32].

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 |



