В спектрах ИК соединений7а-е имеются интенсивные полосы поглощения, характерные для тиофосфорильной группы (Р=S) в области 750-820 см-1, лактамногокарбонила при 1668-1675 см-1. В спектрах ЯМР 1Н амидотионфосфатахцитизина7а-е имеются характерные сигналы цитизиниевого фрагмента (сигналы протонов Н1-Н8) практически мало отличающиеся от исходных соединений6а-е. Протоны, входящие в тиофосфорильную группу, резонируют в ожидаемых областях поля спектра. Следует отметить, что в соединении О, О-диметил-N-цитизинилтионфосфата 7е наблюдается неэквивалентность двух метоксильных групп (два дублета с δ 3,37 и 3,29 м. д.), обусловленная асимметрией в цитизиниевом фрагменте. Проявление дублетности связано со спин-спиновым взаимодействием с ядром атома фосфора (JНР 12,0 Гц).
Выводы:
- Фосфорилирование–замещение атома в молекуле органического соединения на остаток фосфорной или другой фосфорсодержащей кислоты либо их производного. Фосфорилирование обычно осуществляется по механизму бимолекулярного нуклеофильного замещения (SN2) у атома P. Основные реакции: реакция Тодда–Атертона, реакция Кабачника-Филдса; Реакция Тодда–Атертона и фосфорилирование аминов идет в среде галогенуглеродов или полигалогенирующих углеводородов; Реакция Кабачника-Филдса, метод синтеза a-аминофосфорильных соединении, заключается в одновременном или последовательном действий на NH3, первичные или вторичные амины альдегидов или кетонов и гидрофосфорильных соединений; Получение основных фосфорпроизводных природного алкалоида цитизин по реакциям Тодда–Атертона и Кабачника-Филдса;
3. Экспериментальная часть
3.1 Характеристика объектов исследования
Объектом исследования был выбран алкалоид – цитизин. Предмет исследования: фосфорсодержащие производные алкалоида цитизина.
Цель работы заключается в поиске и разработке синтеза фосфорсодержащих производных алкалоида цитизина, в изучении строения, реакционной способности и механизма их образования, установлении условий протекания реакций, а также проведении исследований антиоксидантной активности синтезируемых соединений. Рассмотрим следующие полученные соединения.
Инструкция перед началом работы:
- очистить предварительно место работы (вытяжка); приготовить и проверить исправность всех используемых оборудований; промыть посуду этиловым спиртом; очистить все используемые растворители (дисстиляция);
3.2 Синтезы аминофосфатов цитизина
Одним из широко известных методов синтеза фосфонметилированных производных азотосодержащих соединений является классическая реакция Кабачника-Филдса. Изучение влияний катализатора на выход продуктов реакции Кабачника-Филдса было проведено на примере N-диалкоксифосфо-рилметильных производных цитизина. С этой целью были поставлены ряд параллельных опытов с использованием каталиатора и без него. Установлено, что применение краун-эфиров позволяет повысить селективность процесса и способствует увеличению выхода целевых продуктов на 20-25%. Действие краун-эфиров можно объяснить их способностью участвовать в образовании водородных связей с гидрофосфорильными соединениями, переводя тем самым последние в реакционноспособную симметричную форму Р-О-Н.
1.Синтез Диметил -2-(-N-цитизинил)-2-пропилфосфоната (1):
Смесь 3,8г (0,02М) цитизина, 1,16г (0,02М) ацетона,2,2г (0,02М) диметилфосфита и каталитического колоичества 15-кр-5 в 100мл бензола кипятят 3 часа с одновременной отгонкой образующейся в ходе реакции воды. После окончания реакции образовавшийся осадок отфильтровывают, промывают несколько раз эфиром и сушат в вакууме. Получают 3,74 (55,0%) соединения Rf=0,60, элюент ацетон:спирт =2:1.
2. Синтез Диметил-2-(-N-цитизинил)-2-изобутилфосфоната (2):
Смесь 3,8г (0,02М) цитизина, 1,44г (0,02М) изомасляного альдегида, 2,2г (0,02М) диметилфосфита и каталитического количества 15-кр-5 в 100мл бензола кипятят 4ч. С одновременной отгонкой образующейся в ходе реакции воды. После окончания реакции растворитель выпаривают на роторном испарителе, остаток промывают несколько раз сухим эфиром и очищают перекрисстализацией из смеси бензола:гексана=2:0,5. Получают 6,15г (87%) соединения Rf=0,62, элюент ацетон:спирт =2:1.
Индивидуальность и строение соединения (1) и (2) подтверждены данными ТСХ, ВЭЖХ и ЯМР1Н-спектроскопии (в разделе 4).
3.3 Синтезы фосфорсодержащих солей цитизина [62]
Взаимодействие цитизина 1 с гидрофосфорильными соединениями в определенных условиях приводит к получению его тио - и дитиофосфатных солей. В продолжение этих исследований и с целью изучения взаимосвязи «структура-активность» в [80] осуществлен синтез моноалкилфосфатных, диалкилтиофосфатных и диалкилдитиофосфатных солей цитизина.
Моноалкилфосфатная соль цитизина2 получена взаимодействием последнего с диметилфосфористой кислотой в водно-спиртовой среде при длительном нагревании [80].
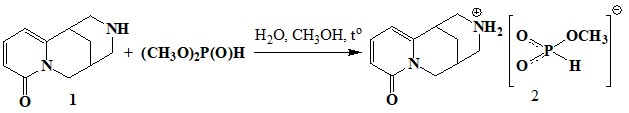
1. ЦитизинийО, О-диалкилтиофосфаты
Цитизиний О, О-диалкилтиофосфаты 3а-е, которые по данным биопрогнозирования должны обладать гипертензивной, кардиостимулирующей и противогрибковой активностью, были синтезированы взаимодействием алкалоида цитизина с фосфитами в присутствии серы в бензоле при нагревании [81].
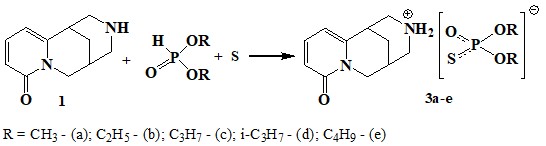
Полученные соединения 3a-e представляют собой белые кристаллические вещества, хорошо растворимые в воде, спирте и ацетоне.
2. Цитизиний О, О-диалкилдитиофосфаты
Биологически активные комплексные диалкилдитиофосфатные соли 4a-e синтезированы взаимодействием цитизина с диалкилдитиофосфористыми кислотами [373].
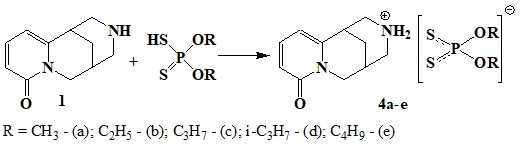
Полученные соединения 4a-e представляют собой белые кристаллические вещества, выходы которых составили 90-95%.
Обнаружена высокая антиоксидантная активность соединения 4e. Цитизиний О, О-дибутилдитиофосфат4e в концентрациях 10-4÷10-5 М обладает антиоксидантной активностью, сравнимой с активностью ионола [82].
Соединение 4а в концентрации 500 мкМ ингибирует захват гамма-аминомасляной кислоты на 30% и ингибирует захват норадреналина на 40%.
Изучена реакция взаимодействия алкалоида цитизина с альдегидами и диизопропилдитиофосфорной кислотой [83]. Установлено, что в результате реакции вместо ожидаемого N-диизопропилтиофосфорилметильного производного цитизина 5 с хорошим выходом был выделен дитиофосфатная соль 5d.
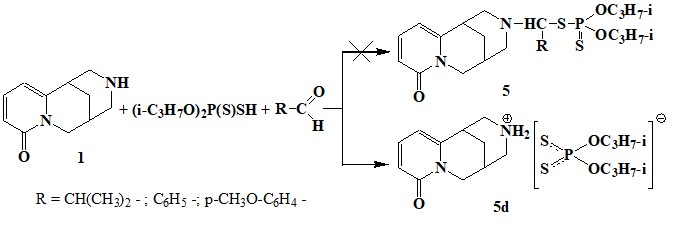
Образование продукта5аминотиофосфонметилирования не было зафиксировано при изучении реакции методами ИК - и ЯМР 1Н-, 31Р-спектроскопии. При длительном нагревании смеси реагентов усиливаются побочные процессы – образование триэфиров дитиофосфорной кислоты.
3.4 Разработка нового отечественного гепатопротекторного средства “Цитафат”
Одним из наиболее практически ценных результатов наших исследований является создание оригинального эффективного гепатопротекторного средства «Цитафат» [63,64].
Цитафат (условное название) представляет собой О, О-диметил-N-цитизинилфосфат (65), не описан в международной фармакопее.
Цитафат обладает выраженным лечебным гепатопротекторным действием на моделях подострого и хронического тетрахлорметанового гепатита: увеличивает выживаемость животных, снижает уровень индикаторов цитолиза и уменьшаются признаки альтерации ткани, препятствует развитию постнекротического цирроза и обеспечивает относительную сохранность биохимических процессов в клетках ткани печени. В механизме гепатопротекторного действия Цитафата присутствует антиоксидантный, мембраностабилизирующий, желчегонный эффект и эффект индукции микросомальных ферментов печени.
Цитафат относится к классу малотоксичных фармакологических соединений и легко растворим в воде.
3.5 Характеристика 0,0-Диметил-N-цитизинилфосфата [65]
Цитафат - 0,0-Диметил-N-цитизинилфосфат.
Препарат содержит не менее 99,5% С13Н19N2О4Р в пересчете на сухое вещество.
Цитафат - белый порошок без запаха, горького вкуса, очень легко растворим в воде, спирте и хлороформе, практически не растворим в эфире.
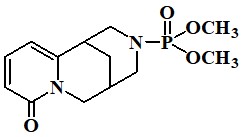
(I)
С13Н19N2О4Р М. м. – 298,0
Цитафат(I) - белый порошок без запаха, горького вкуса, очень легко растворим в воде, спирте и хлороформе, практически не растворим в эфире.
Для идентификации препарата предложен УФ-спектр. Ультафиолетовый спектр 0.01% водного раствора препарата в области от 210 нм до 340 нм имеет максимум поглощения при 305±2 нм и минимум при 231±2 нм. Температура плавления от 155 до 159оС. Удельное вращение 2%-ного водного раствора составляет от –199 до –201о. Растворы прозрачны, бесцветны. рН от 4.0 до 5.0 (2% - ный водный раствор).
Цитафат фасуют по 1 или 1.5 г во флаконы из светозащитного стекла вместимостью 10 мл. рок годности 3 года.
3.6 Методики получения О, О-диметил-N-цитизинилфосфата в классических условиях [66]
Наиболее близким по технической сущности является способ получения О, О-диметил-N-цитизинилфосфата в условиях реакции Тодда-Атертона взаимодействием алкалоида цитизина с диметилфосфитом в среде бензола в присутствии четыреххлористого углерода и триэтиламина [67].
Методика №1
O, O-диметил-N-цитизинилфосфат получают в условиях реакции Тодда-Атертона по следующей схеме:
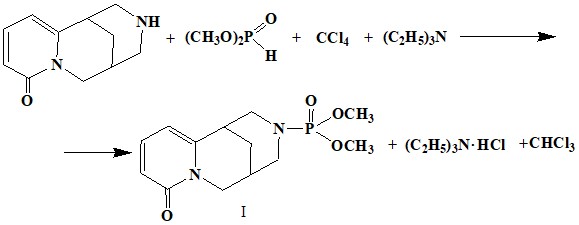

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 |



