В настоящее время на базе полученных 10 тысяч лекарственных субстанций, нескольких сот тысяч готовых лекарственных средств и анализе их структурных формул, физико-химических свойств, данных об основных и побочных видах биологической активности разработаны информационные массивы (банки данных) химических соединений с известными видами физиологической активности [46]. Общее число соединений в массиве свыше 7000 единиц. Основные принципы построения банка данных и его структура приведены в работах [47]. Информационный массив позволяет определить новизну химического соединения, степень сходства с ранее известными биологически активными соединениями, а также дать прогноз о возможном виде активности, которым может обладать данное соединение.
Весьма перспективным являются также электронно-топологический подход к исследованию связи «структура-активность» [48]. Это расчетный метод с применением основ молекулярной механики и квантовой химии. Электронно-топологическая матрица смежности позволяет описать соединения на электронном и конформационном уровне, что дает возможность связать активность соединений с распределением электронной плотности между различными центрами молекулы [36].
В настоящее время в научных центрах по безопасности биологически активных веществ с помощью логико-комбинаторных методов осуществляется биопрогноз по 110 видам активности. В результате прогноза оценивается спектр активностей и соответствующие вероятностные характеристики для каждого вида активности коэффициенты доверия и эффективности.
Выводы:
- Особое место среди многочисленных органических соединений в природе занимают растительные основания – алкалоиды; Производные многих алкалоидов являются важными лекарственных препаратами, особое внимание уделяется алкалоиду хинолизидинового ряда – цитизин; Химическая модификация алкалоида цитизина обладает большими и все еще не раскрытыми потенциальными перспективами и до настоящего времени привлекает усиленное внимание; В настоящее время многие фосфорорганические соединения нашли широкое применение в качестве эффективных лекарственных средств, введение фосфорсодержащего фрагмента в молекулу природного соединения может привести к созданию новых высокоэффективных биологически активных соединений.
2. Реакции фосфорилирования и синтезы алкалоида цитизина
2.1 Фосфорилирование. Реакция Тодда – Атертона и Кабачника–Филдса [49]
Фосфорилирование–замещение атома в молекуле органического соединения на остаток фосфорной или другой фосфорсодержащей кислоты либо их производного, например: в широком смысле фосфорилирование называют замещение любого атома или группы атомов на остаток фосфорсодержащей кислоты или введение остатка такой кислоты в молекулу любыми другими способами [50]. Фосфорилирование реализовывается по механизму бимолекулярного нуклеофильного замещения (SN2) у атома фосфора.
Наибольшие активные фосфорилирующие агенты – соединения, содержащие связь P - X [X = Hal, OH, OR:,OC(O)R: и др.]. Реакция катализируется основаниями, кислотами, ионами металлов. Замещение в молекуле атома H у атомаС на группировку P(O)ClX (X = Cl, Alk, Ar, RO, R2N) осуществляют взаимодействием органического соединения с XPCl2 и O2 (окислительное хлорфосфонирование).
Для избирательного фосфорилирования полифункционального соединения подбирают соответствующий фосфорилирующий агент или условия реакции, например: иногда для избирательного фосфорилирования осуществляют предварительно защиту функциональных групп, не подлежащих фосфорилированию. Фосфорилирование некоторых важных ферментов приводит к их ингибированию (потери ферментативной активности). Так, многие фосфорорганические соединения способны фосфорилировать холинэстеразы, что приводит к блокаде нервно-мышечной передачи импульсов в вегетативной нервной системе. Фундаментальное значение для жизнедеятельности всех живых организмов имеет фосфорилирование, осуществляемое при обмене веществ, которое катализируется ферментами группы фосфотрансфераз. Донорами фосфатной группы обычно служат нуклеотиды, среди которых главную роль играет АТФ. Фосфорирование широко применяют для синтеза пестицидов, пластификаторов, негорючих пропиток, лекарственных средств, экстрагентов. Основные реакции: Абрамова реакция, Арбузова реакция, Кабачника-Филдса реакция, Кирсанова реакция, Клея-Киннера-Перрена реакция, Михаэлиса-Беккера реакция, Перкова реакция, Пищи-муки реакция, Тодда-Атертона реакция, Хорнера реакция [49]. Рассмотрим реакции Тодда–Атертона и Кабачника – Филдса: [50] Реакция Тодда–Атертона и фосфорилирование аминов или NH3 диорганофосфитами в среде галогенуглеродов или полигалогенирующих углеводородов, например: фосфорилирование низкоосновных аминов ведут в присутствии более сильных оснований [например, (C2H5)3N][64]. Она открыта в 1945 Ф. Атертоном, X. Опеншоу и А. Тоддом. В присутствии третичных аминов фосфорилируются также спирты, фенолы и др. Реакцию проводят в среде ССl4, С2Сl5Н или СВrСl3 при комнатной температуре или при нагревании (40-60 °С, 1-2 ч). Cначала в реактор вносят фосфорилирующий агент, а затем при перемешивании прикапывают реагент, подлежащий фосфорилированию, если амин низко основный, то используют эквимолярную смесь этого амина и (C2H5)3N]. Газообразные амины (NH3, CH3NH2 и др.) барботируют в реактор. Также реакцию можно осуществить в условиях межфазного катализа. Выходы 60-95%. Механизм реакции полностью не выяснен. Установлено, что на первой стадии образуется хлорангидрид соответствующего эфира фосфористой кислоты (В-основание): На второй стадии имеет место собственно фосфорилирование амина хлорангидридом. Первая стадия процесса идет лишь в присутствии сильных оснований. В реакцию, схожую с реакцией Тодда-Атертона, вступают практически все соединения типа XYP(О)H (X, Y = Alk, Ar, OR, NR2), а также фосфорноватистая кислота и ее эфиры. В условиях Т.-А. р. некоторые производные тиокислот фосфора типа Х2 Р(S) H образуют соответствующие тиофосфорильные соединения; моноорганоамиды диалкилфосфористых кислот и вторичные амины образуют фосфазосоединения: Т.-А. р. широко используют в препаративной практике. [51] Реакция Кабачника-Филдса, метод синтеза a-аминофосфорильных соединений, заключающийся в одновременном или последовательном действии на NH3, первичные или вторичные амины альдегидов или кетонов и гидрофосфорильных соединений. При использовании тиогидрофосфорильных соединении образуются a-аминотиофосфорильные вещества [52]. Реакция открыта в 1952 и независимо от него несколько позднее Э. Филдсом. Примеры реакции Кабачника-Филдса – взаимодействие диэтилфосфита с ацетоном и NH3, тетраметилдиамида фосфористой кислоты с тетраметиламиналембензальдегида [получают из (CH3)2NH и бензальдегида]. Реакцию Кабачника-Филдса проводят при 80-120 °С в среде полярного растворителя. Побочные процессы - образование a-гидроксифосфорилъных соединений и солей в результате алкилирования аминогрупп фосфоэфирными группами соединения, образующихся на первой стадии реакции. В ряде случаев основная реакция осложняется дезаминированием и другими процессами. Важная разновидность реакции Кабачника-Филдса– взаимодействия фосфористой или фосфорноватистой кислот с аминоарилирующими или аминоалкилирующими агентами, например:
реакцию Кабачника-Филдса используют для получения экстрагентов тяжелых металлов, комплексонов, лекарственных средств, ионообменных смол и др.[52].
2.2 Синтезы фосфорсодержащих производных алкалоида цитизина
Одним из широко известных методов синтеза фосфонметилированных производных азотсодержащих соединений является классическая реакция Кабачника-Филдса. Так, в [53] осуществлен синтез диалкил-2-цитизиноалкил(арил)-фосфонатов 1a-h взаимодействием алкалоида цитизина и диалкилфосфитов с карбонильными соединениями по схеме:
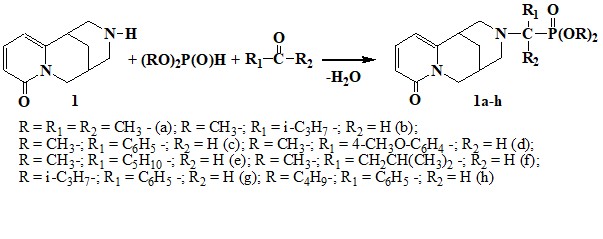 Реакцию проводили в бензоле с азеотропной отгонкой образующейся в ходе реакции воды, выходы целевых продуктов составил от 33,7 до 58,4%. При осуществлении синтеза аминофосфонатов 1a-h с использованием в качестве катализатора различных краун-эфиров (15-Cr-5; 18-Cr-6; ДБ-24-Cr-6) установлено, что их применение позволяет повысить выход целевых продуктов на 20-28%. Действие краун-эфиров можно объяснить их способностью участвовать в образовании водородных связей с диалкилфосфитами переводя тем самым последние в реакционноспособную симметричную форму:>Р-О-Н…О. В ИК-спектрах соединений 1a-h имеются характерные полосы поглощения в областях 1220-1238 см-1 (Р=О) и 1020-1035 см-1 (Р-О-С). Валентные колебания карбонильной группы соединений 1a-h проявляются интенсивной узкой полосой в области 1650-1700 см-1. В спектрах ЯМР 31Р соединений 1a-h наблюдается сигнал в области 18,3-22 м. д., что характерно для соединений аминофосфонатного строения. В спектрах ЯМР 1Н аминофосфонатов 1a-h протоны основного алкалоидного скелета проявляются в характерных областях. Так, при анализе спектра диметил-2-(N-цитизинил)-2-пропилфосфоната 1a три группы сигнала низкого поля соответствуют протонам б-пиридонового ядра. Сигналы при 7,20 м. д. соответствуют Н2 протону с КССВ JН2Н3 = 8,0 Гц. Расщепленный дублет при 5,94 м. д. соответствует Н3 протону, а расщепленный дублет при 6,32 м. д. – Н1 протону с JН1Н2 = 10,0 Гц. Следующая группа линий, представляющая собой сложный мультиплет в области 3,20-4,40 м. д. соответствует аксиальному и экваториальному протонам в положении С7. Сигналы протонов Н8 имеют расщепление в области 2,38 м. д. в виде дублета. Группа линий в области 2,98-3,10 м. д. представляют собой сигналы Н4, Н6 протонов. Метиленовые протоны Н5 проявляются в виде сложного мультиплета в области с центром 1,96 м. д.
Реакцию проводили в бензоле с азеотропной отгонкой образующейся в ходе реакции воды, выходы целевых продуктов составил от 33,7 до 58,4%. При осуществлении синтеза аминофосфонатов 1a-h с использованием в качестве катализатора различных краун-эфиров (15-Cr-5; 18-Cr-6; ДБ-24-Cr-6) установлено, что их применение позволяет повысить выход целевых продуктов на 20-28%. Действие краун-эфиров можно объяснить их способностью участвовать в образовании водородных связей с диалкилфосфитами переводя тем самым последние в реакционноспособную симметричную форму:>Р-О-Н…О. В ИК-спектрах соединений 1a-h имеются характерные полосы поглощения в областях 1220-1238 см-1 (Р=О) и 1020-1035 см-1 (Р-О-С). Валентные колебания карбонильной группы соединений 1a-h проявляются интенсивной узкой полосой в области 1650-1700 см-1. В спектрах ЯМР 31Р соединений 1a-h наблюдается сигнал в области 18,3-22 м. д., что характерно для соединений аминофосфонатного строения. В спектрах ЯМР 1Н аминофосфонатов 1a-h протоны основного алкалоидного скелета проявляются в характерных областях. Так, при анализе спектра диметил-2-(N-цитизинил)-2-пропилфосфоната 1a три группы сигнала низкого поля соответствуют протонам б-пиридонового ядра. Сигналы при 7,20 м. д. соответствуют Н2 протону с КССВ JН2Н3 = 8,0 Гц. Расщепленный дублет при 5,94 м. д. соответствует Н3 протону, а расщепленный дублет при 6,32 м. д. – Н1 протону с JН1Н2 = 10,0 Гц. Следующая группа линий, представляющая собой сложный мультиплет в области 3,20-4,40 м. д. соответствует аксиальному и экваториальному протонам в положении С7. Сигналы протонов Н8 имеют расщепление в области 2,38 м. д. в виде дублета. Группа линий в области 2,98-3,10 м. д. представляют собой сигналы Н4, Н6 протонов. Метиленовые протоны Н5 проявляются в виде сложного мультиплета в области с центром 1,96 м. д.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 |



