УЧРЕЖДЕНИЕ ОБРАЗОВАНИЯ
«БЕЛОРУССКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ»
УДК 616–056.3–036.12:612.751]–053.2–07–08
ПОЧКАЙЛО
Алексей Сергеевич
КОМПЛЕКСНАЯ ОЦЕНКА И КОРРЕКЦИЯ
СОСТОЯНИЯ КОСТНОЙ ТКАНИ У ДЕТЕЙ
С ХРОНИЧЕСКИМИ АЛЛЕРГИЧЕСКИМИ ЗАБОЛЕВАНИЯМИ
Автореферат
диссертации на соискание ученой степени
кандидата медицинских наук
по специальности 14.00.09 – педиатрия
Минск 2009
Работа выполнена в ГУО «Белорусская медицинская академия последипломного образования»
Научный руководитель: , доктор медицинских наук, профессор, заведующий кафедрой поликлинической педиатрии ГУО «Белорусская медицинская академия последипломного образования»
Официальные оппоненты: , доктор медицинских наук, профессор, заслуженный деятель науки Республики Беларусь,
член-корреспондент НАН Беларуси, заведующий 1-й кафедрой детских болезней УО «Белорусский государственный медицинский университет»
, доктор медицинских наук, профессор, заведующий кафедрой педиатрии УО «Витебский государственный ордена Дружбы народов медицинский университет»
Оппонирующая организация: ГУ «Республиканский научно-практический центр «Мать и дитя»
Защита состоится 16 декабря 2009 г. в 12.00 часов на заседании совета по защите диссертаций Д 03.18.01 при УО «Белорусский государственный медицинский университет» ( г. Минск, пр-т Дзержинского, 83,
С диссертацией можно ознакомиться в библиотеке УО «Белорусский государственный медицинский университет».
Автореферат разослан « 14 » ноября 2009 г.
 Ученый секретарь совета
Ученый секретарь совета
по защите диссертаций,
кандидат медицинских наук, доцент
ВВЕДЕНИЕ
Нарушение костного формирования у детей − актуальная
и недостаточно исследованная проблема современной педиатрии в силу значительной распространённости и детерминирующего влияния на риск развития остеопороза и связанных с ним переломов во взрослой популяции [, 2007; и др., 2007; Bianchi L.M., 2007; , 2008]. Достижение детьми пиковой костной массы, своевременное выявление и коррекция его нарушений − перспективный потенциал профилактики остеопороза у взрослых [ и др., 2007]. У детей преобладает вторичная форма нарушений костного формирования, чаще развивающаяся на фоне хронической патологии или приёма лекарств с негативным остеотропным влиянием [
и др., 2006]. Аллергические заболевания по современным представлениям являются значимым этиологическим фактором развития этих нарушений [, 2003].
Широко изучаемой и противоречивой является проблема влияния на костную ткань стероидной терапии у пациентов с бронхиальной астмой [Agertoft L. et al., 1998; Leone F.T. et al., 2003; и др., 2005]. Лишь единичные исследования касаются анализа костного формирования при атопическом дерматите [Konstantynovicz J. et al., 1998; Hidvegi E. et al., 2003; Jensen V.B. et al., 2004]. Сравнение состояния и возрастной динамики костной плотности и метаболизма, частоты их нарушений у пациентов
с бронхиальной астмой и атопическим дерматитом ранее не проводилось.
К важным и не решённым практическим задачам относится установление факторов риска нарушений костного формирования у детей
с хроническими аллергическими заболеваниями, анализ частоты переломов у них и их взаимосвязь с уровнем костной плотности, выявление отклонений в параметрах костного метаболизма, уровнях минералов и гормонов крови, их значимости в диагностике нарушений костного формирования. Недостаточно изучены подходы к коррекции дефицита костной плотности
у детей в целом и при аллергических заболеваниях в частности. Остаются без ответа вопросы, касающиеся показаний к назначению препаратов кальция и витамина Д, длительности их приема, дозирования, влияния
на прирост костной плотности и факторов, прогнозирующих такой прирост
у детей с хроническими аллергическими заболеваниями.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Связь работы с крупными научными программами (проектами)
и темами. Исследование выполнено в рамках задания № 3.30 «Изучение возрастных особенностей макро - и микроэлементного гомеостаза
и гормонального статуса у жителей Беларуси и их роли в патогенезе метаболической костной и почечной патологий» (№ государственной регистрации от 01.01.2001 г., научный руководитель темы − заведующий ЦНИЛ БелМАПО, канд. мед. наук, доцент , сроки выполнения: 2006–2008 гг.) Государственной комплексной программы научных исследований на 2006–2010 гг. «Современные клеточные
и молекулярно-генетические технологии в медицине; новые подходы
к регуляции, коррекции (реабилитации) и профилактике патологических состояний человека (Современные технологии в медицине)». Тема исследования соответствует приоритетным направлениям научно-технической деятельности в Республике Беларусь на 2006–2010 гг., утверждённым Указом Президента Республики Беларусь № 000 от 01.01.2001 г.
Цель и задачи исследования
Цель исследования: установить факторы, связанные со снижением минеральной костной плотности, и факторы, прогнозирующие её прирост при приёме препарата, содержащего кальций и витамин Д, у детей 7−17 лет
с бронхиальной астмой и атопическим дерматитом на основе комплексной оценки минеральной плотности и метаболизма костной ткани, клинических и анамнестических данных.
Задачи исследования:
1. Определить состояние и возрастную динамику минеральной плотности и метаболизма костной ткани по данным рентгеновской остеоденситометрии и оценки биохимических маркёров костного метаболизма у детей школьного возраста с бронхиальной астмой
и атопическим дерматитом.
2. Выявить факторы, связанные с состоянием костной ткани
и формированием дефицита минеральной плотности кости, у школьников
с бронхиальной астмой и атопическим дерматитом.
3. Представить сравнительную характеристику маркёров костного метаболизма (остеокальцин, общая щелочная фосфатаза сыворотки, кальций-креатининовый коэффициент утренней порции мочи), уровней минералов (общий Са, Mg, Р, К, Nа) и гормонов (кальцитонин, паратироидный гормон, свободная фракция тироксина, тиротропный гормон, кортизол, инсулин) сыворотки у детей школьного возраста с бронхиальной астмой и атопическим дерматитом, имеющих различный уровень минеральной плотности костной ткани.
4. Установить динамику изменений и факторы, прогнозирующие прирост минеральной плотности костной ткани, при коррекции её дефицита у школьников с бронхиальной астмой и атопическим дерматитом отечественным витаминно-минеральным комплексом «Кальций-Д3-МИК»
в зависимости от степени приверженности пациентов лечению.
Объект исследования: дети 7–17 лет с аллергической формой бронхиальной астмы и атопическим дерматитом любой степени тяжести, практически здоровые дети 12–17 лет без значимых факторов риска нарушений костного формирования.
Предмет исследования: анамнестические (включая анкетные) данные, параметры физического и полового развития, костного возраста, показатели костной массы, минеральной плотности, метаболизма костной ткани, уровни минералов и гормонов сыворотки крови.
Положения, выносимые на защиту
1. Возрастная динамика минеральной плотности костной ткани у детей с хроническими аллергическими заболеваниями значимо не отличается
от здоровых. У детей 7–17 лет с хроническими аллергическими заболеваниями, как и у здоровых сверстников, происходит возрастное увеличение массы и минеральной плотности кости, а также динамические изменения в уровне остеокальцина и активности общей щелочной фосфатазы крови, характеризующиеся половыми различиями. Денситометрические и метаболические параметры костной ткани, частота дефицита минеральной плотности кости по отношению к половой
и возрастной норме у детей школьного возраста с бронхиальной астмой, атопическим дерматитом и здоровых сверстников не имеют различий.
2. У детей с хроническими аллергическими заболеваниями существует связь между состоянием костной ткани, паспортным и костным возрастом, стадией пубертата, причём период подросткового возраста, соответствующий середине пубертата, является критическим по формированию дефицита минеральной плотности кости. Физическое развитие этих пациентов коррелирует с денситометрическими, а уровень физической активности − с денситометрическими и метаболическими показателями костной ткани.
3. Более высокая активность общей щелочной фосфатазы и уровень остеокальцина у детей с хроническими аллергическими заболеваниями, имеющих дефицит костной плотности, свидетельствуют об активизации костного формирования, в то время как более высокий кальций-креатининовый коэффициент мочи у таких пациентов может быть связан, как с повышенной костной резорбцией, так и с меньшим уровнем креатининурии в сравнении с детьми, имеющими нормальную минеральную плотность кости. Уровни минералов (общий Ca, Mg, P, K, Na) и гормонов (кальцитонин, паратироидный гормон, свободная фракция тироксина, тиротропный гормон, кортизол, инсулин), частота переломов у детей
с дефицитом минеральной плотности кости, страдающих хроническими аллергическими заболеваниями, не различаются в сравнении с пациентами, имеющими нормальную костную плотность.
4. Применение комплекса «Кальций-Д3-МИК» отечественного производства у детей с дефицитом минеральной плотности кости на фоне хронических аллергических заболеваний обеспечивает её бóльший
по сравнению с естественным прирост, причём уровень остеокальцина крови до начала коррекции служит фактором, прогнозирующим величину этого прироста, а шестимесячный срок коррекции недостаточен для восстановления минеральной плотности кости до нормы у большинства пациентов.
Личный вклад соискателя. Соискателем лично проведен патентно-информационный поиск, анализ литературы по теме исследования, разработаны и утверждены анкеты и протокол обследования пациентов, организован и выполнен отбор, анамнестическое исследование (включая анкетирование), клинический осмотр с антропометрией, оценкой физического и полового развития пациентов, заполнение учётной документации. Автор принимал участие в заборе и пробоподготовке биологического материала, освоении методик и выполнении лабораторно-инструментальных исследований по теме диссертации, включая освоение
и проведение денситометрии, самостоятельную интерпретацию денситограмм, иных результатов исследований. Соискателем самостоятельно создана база данных обследованных пациентов на бумажных носителях
и в электронном виде в программах MS Excel и Statistica 6.0., проведена статистическая обработка данных. Научным руководителем оказана консультативная помощь в выборе темы, обсуждении результатов, формулировке выводов. Личный вклад соискателя в подготовку докладов
и публикаций в соавторстве составляет для докладов – до 90 %, для статей
и тезисов − до 80 %, для рационализаторских предложений – до 70 %, для изобретения – до 50 %, для инструкции по применению – до 30 % и отражен в совместных публикациях.
Апробация результатов диссертации. Результаты исследований, включенные в диссертацию, докладывались и обсуждались: на Научных сессиях УО «Белорусский государственный медицинский университет» 30.01.2008 г. и 29.01.2009 г. (г. Минск, Беларусь), Республиканской научно-практической конференции с международным участием «Остеопороз: современные возможности диагностики и перспективы терапии» 20.03.2008 г. (г. Гомель, Беларусь), Минском областном семинаре «Актуальные вопросы аллергологии детского возраста» 26.03.2008 г. (п. Лесной, Беларусь), научно-практической конференции с международным участием «Боль в спине»
15–16.05.2008 г. (г. Полтава, Украина), Республиканской научно-практической конференции «Актуальные вопросы детской аллергологии
и пульмонологии» 17.06.2008 г. (г. Минск, Беларусь), 1-м международном практическом семинаре-выставке «Медицинские достижения
в практическом здравоохранении» 12–13.02.2009 г. (г. Минск, Беларусь).
Опубликованность результатов диссертации. По материалам диссертации в соавторстве и единолично опубликовано 32 печатные работы общим объёмом 7,6 авторских листа, в том числе – 8 статей в научных рецензируемых журналах, рекомендованных ВАК для публикации результатов диссертационных исследований (включая 1 – в моноавторстве), общим объёмом 4,8 авторских листа, а также 3 публикации в рецензируемых сборниках, 21 публикация в сборниках тезисов, научных трудов
и материалах конференций (включая 11 – в моноавторстве) общим объёмом 2,8 авторских листа. В соавторстве подготовлена, утверждена, издана
и внедрена в 2 учреждениях здравоохранения инструкция по применению «Способ комплексной диагностики низкой костной массы и остеопороза
у детей и молодых взрослых» (утверждена Министерством здравоохранения Республики Беларусь 13.02.2009 г., регистрационный № 000–1208).
В соавторстве подготовлены, приняты в ГУО «Белорусская медицинская академия последипломного образования» и внедрены в 4 учреждениях здравоохранения 3 рационализаторских предложения. В соавторстве подготовлена и подана заявка № а от 01.01.2001 г., получено решение Национального центра интеллектуальной собственности Государственного комитета по науке и технологиям Республики Беларусь
о выдаче патента на изобретение «Способ лечения остеопенического синдрома у ребёнка с хроническим аллергическим заболеванием».
Структура и объём диссертации. Диссертация изложена на русском языке на 150 страницах машинописного текста и состоит из введения, общей характеристики работы, обзора литературы, главы описания материалов
и методов исследований, 4 глав результатов собственных исследований, заключения, библиографического списка и приложений. Объем, занимаемый 14 иллюстрациями, 19 таблицами, 17 приложениями, – 34 страницы. Библиографический список состоит из списка использованных источников (190 наименований, включая 82 иностранных источника и 108 – отечественных и стран СНГ), а также списка публикаций соискателя
из 32 печатных работ, занимает 19 страниц. Приложения включают
1 решение о выдаче патента на изобретение, титульный лист 1 инструкции по применению, 12 актов о внедрении рационализаторских предложений,
1 акт практического использования результатов исследования в учебном процессе, 2 акта о внедрении инструкции по применению.
ОСНОВНОЕ СОДЕРЖАНИЕ
Материалы и методы исследований
Для решения задач в исследование включено 178 детей. Основную группу составили 127 мальчиков (Мч) и девочек (Дв), страдающих аллергической формой бронхиальной астмы (БА) или атопическим дерматитом (АД) любой степени тяжести, 7–17 лет (Дв) и 7–15 лет (Мч), госпитализированных в УЗ «Минская областная детская клиническая больница» (УЗ «МОДКБ»). В контрольную группу вошёл 51 ребёнок
I–II групп здоровья, обследованный в УЗ «11-я городская детская поликлиника» г. Минска и ГУ «Республиканский центр медицинской реабилитации и бальнеолечения» (ГУ «РЦМРБ») 12–15 лет (Мч) и 12–17 лет (Дв) в связи с необходимостью их сопоставления со старшей подгруппой пациентов с хроническими аллергическими заболеваниями (ХАЗ). Исключали детей, профессионально занимавшихся спортом,
с анамнестическими и/или клиническими указаниями на наличие иной (кроме ХАЗ) хронической патологии и/или приём в значимых дозах/сроках лекарственных средств, негативно влияющих на костный метаболизм.

Для расчётов детей разделяли на подгруппы в соответствии
с нозологией (АД, БА), возрастом (7–11 и 12–17 лет), полом. Пациентам
с ХАЗ выполняли анамнестическое, физикальное, общеклиническое, аллергологическое, а также специальное обследование. Анамнестическое исследование включало сбор анамнеза аллергической и сопутствующей патологии, выявление наследственной отягощённости по остеопорозу, опрос о наличии в анамнезе у ребёнка переломов и трещин костей. Физическую активность и питание оценивали по разработанным анкетам в виде самоанкетирования. Физикальное обследование начинали с антропометрии и оценки физического и полового развития. Оценку физического развития проводили после измерения длины тела (ДТ), массы тела (МТ), окружности грудной клетки (ОГК) [ с соавт., 1998], расчёта индекса массы тела (ИМТ, частное от деления МТ (кг) на квадрат ДТ (м)). Значение ИМТ интерпретировали в соответствии с критериями ВОЗ. Половое развитие у Дв [J. Tanner, 1969; S. Frasier, 1980] и Мч [J. Tanner, 1980; ,
, 1984] анализировали при осмотре и опросе. Обследование
и верификацию диагноза ХАЗ проводили в соответствии с действующими протоколами. Специальное обследование включало двойную рентгеновскую абсорбциометрию (ДРА), оценку костного возраста, исследование биохимических маркёров костного метаболизма (уровень остеокальцина (ОК), активность общей щелочной фосфатазы (ОЩФ) сыворотки, кальций-креатининовый коэффициент (ККК) первой утренней порции мочи), гормонов (паратироидный гормон (ПТГ), кальцитонин (Кцт), инсулин (Инс), кортизол (Ктз), тиротропный гормон (ТТГ), свободная фракция тироксина (Т4св)) и минералов (общий Са, Mg, неорганический Р, К, Na) сыворотки.
В контрольной группе выполняли анамнестическое, физикальное, специальное обследование (ДРА, оценка костного возраста, анализ ОК, ККК, ПТГ, Кцт, Инс, Ктз, ТТГ, Т4св, Са, Mg, Р).
ДРА L1–L4 позвоночника проводили в ГУ «РЦМРБ» (зав. кабинетом – ) на аппарате Lunar Prodigy GE (Core Version 8.80, США), оснащённом педиатрической программой и референтной базой, с оценкой: площади кости (см²), содержания костного минерала (СКМ, г), минеральной плотности кости (МПК, г/см²). В соответствии с Позицией в педиатрии Международного общества клинической денситометрии при интерпретации результатов анализировали Z–критерий с учётом пола, паспортного, костного возраста, ДТ, МТ, стадии пубертата. Костный возраст определяли
в УЗ «МОДКБ» (зав. кабинетом – ) рентгенографией кисти
с установлением (при наличии) его разницы с паспортным (РКВ). Уровень ОК определяли иммуноэлектрохемилюминесценцией (анализатор «ELECSYS 1010», реагенты «Roche Diagnostics GmbH», Германия), активность ОЩФ – колориметрически по Бессею, Лоури, Броку с измерением в конечной точке (реагенты «Human Gesellschaft fǘr Biochemica und Diagnostica mbH», Германия). Содержание общего Ca, креатинина, неорганического P, Mg сыворотки и Са, креатинина мочи определяли с применением биохимических анализаторов (Dialab Autolyzer, Австрия, ФП-901, Финляндия, наборы «Витал Диагностикс СПб», РФ). Содержание Са анализировали унифицированным колориметрическим методом с о-крезолфталеин-комплексоном, креатинин – псевдокинетическим двухточечным методом (основан на реакции Яффе), P–UV-методом без депротеинизации при восстановлении фосфорномолибденовой кислоты, Mg-колориметрическим методом с ксилидиловым синим без депротеинизации. ККК рассчитывали как отношение Ca первой утренней порции мочи к содержанию креатинина
в этой порции. Содержание K и Na исследовали ионометрически (полуавтоматический калий-натриевый анализатор «ОР 266/1», Венгрия). Содержание гормонов анализировали радиоиммунологическим методом (гамма-счётчик «BERTHOLD» LB 2111, Германия). Содержание Т4св, Ктз, Инс, ТТГ определяли с использованием диагностических наборов УП «ХОП ИБОХ НАН РБ» (РБ), ПТГ – набора «Immunotech» (Франция), Кцт – набора «Diagnostic Systems Laboratories» (США).
После обследования детей с ХАЗ разделяли на подгруппы
в соответствии с результатом ДРА: к подгруппе с дефицитом МПК относили пациентов с Z–критерием, равным или ниже –1 стандартного отклонения (SD), к подгруппе с нормой МПК – со значениями выше –1 SD.
При снижении МПК проводили коррекцию: контроль факторов риска, назначение витаминно-минерального комплекса «Кальций-Д3-МИК» (ПРУП «Минскинтеркапс», РБ), содержащего карбонат Ca (0,1667 г элементарного Ca в 1 капсуле) и витамин Д (66,7 МЕ холекальциферола в 1 капсуле), на
6 месяцев, из расчёта 6 капсул в сутки на 2 приёма для детей 12 лет
и старше, 4 капсулы в сутки на 2 приёма для детей 7−11 лет, во время или после еды. После коррекции выполняли контрольную ДРА с оценкой изменения МПК.
Статистическую обработку результатов проводили в программах MS Excel for Windows 2000 и STATISTICA 6.0 (StatSoft, США). Соответствие распределения признаков закону нормального распределения устанавливали критерием Шапиро–Уилка; при уровне значимости p1<0,05 распределение считали отличающимся от нормального. В зависимости от вида распределения и наличия связи между группами в расчётах использовали параметрические (t-критерий Стьюдента, метод Пирсона)
и непараметрические (U-критерий Манна–Уитни, ранговый анализ вариаций по Краскелу–Уоллису, медианный тест, ранговая корреляция по Спирмену, критерий Вилкоксона) методы. Исследование вида зависимости одного признака от другого с целью прогнозирования значения одного по значению другого выполняли при однофакторном линейном регрессионном анализе. Различия частот в независимых группах анализировали точным критерием Фишера и критерием χ² Пирсона, в связанных группах – критерием χ² МакНемара. Количественные параметры в зависимости от вида распределения представляли в виде среднего значения (М) и среднего квадратического отклонения (s), либо в виде медианы (Me)
и интерквартильного размаха (LQ/UQ). Критическим уровнем значимости при проверке статистических гипотез принимали p2<0,05.
Результаты собственных исследований
У детей с ХАЗ МПК (r=0,76, р2<0,001) и СКМ (r=0,87, р2<0,001) коррелировали с паспортным возрастом, такая же корреляция прослеживалась при разделении по полу. Выявлены отличия (р2<0,001)
в уровнях СКМ и МПК, между возрастными периодами, соответствующими годам жизни, с ростом их значений с возрастом и стабилизацией к 16 годам. Различия (р2<0,001) в СКМ и МПК между возрастными периодами
с увеличением их значений с возрастом прослеживалось как у Мч, так
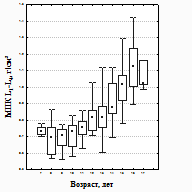
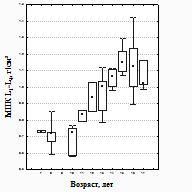
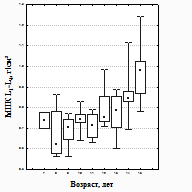
и у Дв: у Дв отмечено нарастание, начиная с 9 лет, со стабилизацией процесса к 16 годам, у Мч − с 12 лет с возрастанием до порогового возраста наблюдения 15 лет (рисунок 1). У здоровых сверстников имела место такая же значимая (р2<0,05) динамика МПК и СКМ с нарастанием их от 12 до
17 лет.
|
|
|
Рисунок 1 – Возрастная динамика МПК у детей (1), Дв (2), Мч (3) с ХАЗ
У пациентов с ХАЗ выявлены возрастные различия в уровне ОК (р2=0,006) и активности ОЩФ (р2=0,013). Установлено, что пиковый уровень ОК приходится на возраст 15 лет, ОЩФ – 13 и 15 лет, ККК – 10 и 17 лет. Выявлены половые различия в содержании ОК: пик концентрации у Дв (р2=0,001) отмечен в 12 лет, а у Мч (р2=0,007) – в 13 и 15 лет (рисунок 2). Максимальная активность ОЩФ в целом совпала с пиками ОК, отмечаясь
в 10–12 лет у Дв (р2=0,002) и в 13–15 лет у Мч (р2=0,144). Уровень ОК коррелировал с активностью ОЩФ (r=0,57, р2<0,001), что может обусловливать сопряжённость их изменений. Значимых динамических различий для ККК в половом и возрастном аспектах не установлено.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |