3. Проверьте работу цепи при разомкнутом и замкнутом ключе.
4. Измерьте ЭДС источника тока (при разомкнутой цепи).
5. Снимите показания амперметра и вольтметра при замкнутом ключе.
6. Переместите движок реостата и снимите показания с приборов ещё раз.
7. Запишите формулу закона Ома для участка цепи.
8. Выразите из неё сопротивление участка.
9. Посчитайте сопротивление участков в обоих случаях и запишите полученные значения в таблицу.
10. Запишите формулу закона Ома для замкнутой цепи для данных случаев (первом и втором)
11. Из формул закона Ома для замкнутой цепи выведете формулу для расчета внутреннего сопротивления источника и вычислите его.
12. Полученное значение запишите в таблицу.
13.Вычислите ЭДС источника тока и запишите его в таблицу
14. Вычислите абсолютную и относительную погрешности измеренного и вычисленного значений ЭДС:
15. Сделайте вывод. В выводе объясните полученные в ходе выполнения работы результаты
Контрольные вопросы.
1. Почему показания вольтметра при разомкнутом и замкнутом ключе различны?
2. Как повысить точность измерения ЭДС источника тока?
Литература:
1. Фирсов для профессий м специальностей технического и естественно - научного профилей: учебник: Рекомендовано ФГУ «ФИРО»/ Под редакцией – М.: «Академия», 2011 – 432с.
2. Янчевская в таблицах и схемах/ . - СПб.: Издательский Дом «Литера», 2008. – 96 с.
3. , Лазаренко по физике. ч.1. :Мозырь Белый ветер, 2006. - 136 с.
Лабораторная работа № 16
Снятие вольтамперной характеристики полупроводникового диода
Цель: снятие вольтамперной характеристики полупроводникового диода
Оборудование: диод полупроводниковый, источник питания на 4 В, миллиамперметр постоянного тока, вольтметр постоянного тока, реостат ползунковый РПШ - 2, провода соединительные, ключ.
Теоретическая часть работы.
Зависимость тока, проходящего через p-n переход, от величины и полярности приложенного к нему напряжения изображают в виде кривой, называемой вольт-амперной характеристикой диода.
По вертикальной оси в верхней части обозначены значения прямого тока Iпр, а в нижней части – обратного тока Iобр.
По горизонтальной оси в правой части обозначены значения прямого напряжения Uпр, а в левой части – обратного напряжения Uобр.
Вольт-амперная характеристика состоит из двух ветвей: прямая ветвь соответствует прямому (пропускному) току через диод, и обратная ветвь, соответствующая обратному (закрытому) току через диод.
![]()
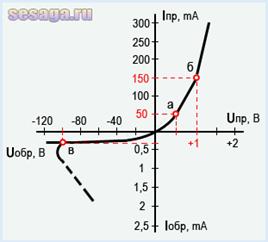
При увеличении прямого напряжения через p-n переход ток вначале возрастает медленно, а затем начинается участок быстрого нарастания тока.
При увеличении обратного напряжения Uобр, приложенного к p-n переходу, ток увеличивается незначительно, о чем говорит обратная ветвь вольтамперной характеристики.
Вопросы для повторения:
1. Для чего применяют диод?
2. Какие типы полупроводников вы знаете?
3. Какой полупроводник называют р-типа, n - типа?
Порядок выполнения работы
1. Повторить устройство полупроводникового диода.
2. Подготовить таблицу.
U (В) | |||||||||||
I (А) |
3. Собрать цепь по схеме:
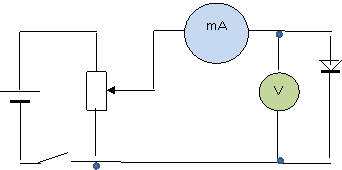 |
Диод включен в пропускном направлении.
4. С помощью резистора изменяйте напряжение и измеряйте силу тока. Результаты занесите в таблицу.
5. Постройте график зависимости силы тока от напряжения
I (mA)
U (В)
6. Исследовать зависимость обратного тока от напряжения. Собрать цепь по схеме:
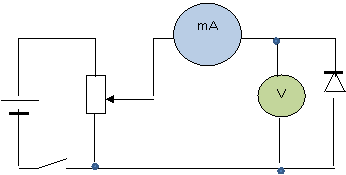
Изменяя напряжение проследить как меняется сила тока.
7. Вывод: как зависит сила тока от напряжения на диоде?
Литература:
1. Фирсов для профессий м специальностей технического и естественно - научного профилей: учебник: Рекомендовано ФГУ «ФИРО»/ Под редакцией – М.: «Академия», 2011 – 432с.
2. Янчевская в таблицах и схемах/ . - СПб.: Издательский Дом «Литера», 2008. – 96 с.
3. , Лазаренко по физике. ч.1. :Мозырь Белый ветер, 2006. - 136 с.
Лабораторная работа № 17
Определение заряда электрона и электрохимического эквивалента меди
Цель: определение экспериментальным путем модуля заряда электрона и электрохимического эквивалента меди и сравнение полученных значений с табличными.
Оборудование: весы с разновесами, амперметр, часы, электрическая плитка, источник питания, реостат, выключатель, соединительные провода, два медных электрода, цилиндрический сосуд, раствор медного купороса, стакан с песком.
Теоретическая часть работы.
Электрохимический эквивалент вещества численно равен массе вещества, выделившегося на электроде при прохождении через электролит заряда, равного 1 Кл. Электрохимический эквивалент вещества выражается в килограммах на кулон (кг/Кл). Закон Фарадея можно записать: m = kIt.
Произведение заряда электрона на постоянную Авогадро — это постоянная Фарадея:F = eNA = 9,65 · 104 Кл/моль. Электрохимический эквивалент меди можно определить, воспользовавшись законом Фарадея для электролиза. Для этого надо измерить массу отложившегося на электроде вещества, силу тока и время его прохождения через электролит.
Заряд электрона может быть определен по формуле е = ![]()
где m1 и m2 -масса катода до и после проведения опыта, М - молярная масса меди, n- валентность меди, NА - постоянная Авогадро, I — сила тока, прошедшего через раствор электролита, ∆t - время прохождения тока.
Вопросы для повторения:
1. Что называется электрохимическим эквивалентом?
2. Чистая вода является диэлектриком. Почему водный раствор соли NaCl является проводником?
Порядок выполнения работы.
1. Уравновесьте весы песком.
2. Положите на одну чашку весов медный электрод, который будет служить катодом.
3. Взвесьте катод.
4.  Соберите цепь, соединив последовательно источник тока, амперметр, реостат, сосуд с раствором медного купороса, в который погружены электроды,
Соберите цепь, соединив последовательно источник тока, амперметр, реостат, сосуд с раствором медного купороса, в который погружены электроды,
ключ.
![]()

![]()

![]()


+ - ![]()
![]()

![]()

![]()
![]()
![]()
![]()
![]()
![]()
 А К А
А К А

5. Замкните ключ, заметив время начала опыта.
6. Поддерживая с помощью реостата силу тока неизменной (около 1 А), следить за тем, что стрелка амперметра совпадала со штрихом шкалы.
7. В течении 20 минут производить электролиз раствора.
8. Выключить ток, вынуть медный электрод, служащий катодом, обсушить его над электроплиткой.
9. Вновь взвесьте электрод, служащий катодом.
10. Результаты измерений занести в таблицу:
№ | М, кг/моль | n | NА, 1/моль 1/моль | m1, кг | m2, кг | I, А | ∆t, с | k, мг/Кл кг/ Кл | е, Кл Кл |
1 |
11. Используя закон Фарадея, определить электрохимический эквивалент меди k= ![]()

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 |



