Выполнение работы
Берут три диска хроматографической бумаги диаметром 12 см. Простым карандашом сверху обозначают фамилию студента и номер диска. В центре каждого диска обводят круг диаметром 0,3-0,4 см. Микропипеткой в центр дисков наносят реактивы, как указано в таблице.
| Iсубстрат | IIcубстрат + фермент | IIIстандарт |
Реактивы | |||
Субстратная смесь (аминокислота + кетокислота) | 2 мкл | 2 мкл | — |
Стандартная смесь (глутамат + аланин) | — | — | 2 мкл |
Раствор АлАТ | — | 2 мкл | — |
Число окрашенных зон и характер окраски | |||
Rf для каждой зоны аминокислоты |
Через 10 минут после нанесения последнего реагента (время инкубации) все три диска подсушивают на воздухе. На каждом диске от края к центру делают ножницами два параллельных разреза (ширина разреза равна диаметру кружочка в центре диска). Вырезанную полоску отгибают перпендикулярно диску так, чтобы линия сгиба проходила через середину зоны нанесения растворов. «Ножку» укорачивают до 2-3 см, и диск помещают между нижней и верхней половинками чашки Петри, содержащей смесь бутанол + уксусная кислота + Н2О в соотношении 5:1:4. Проводят хроматографическое разделение под тягой приблизительно в течение 1 часа. Диски извлекают из хроматографической камеры и обводят фронт растворителя простым карандашом. Высушивают в сушильном шкафу при 100°С, смачивают раствором нингидрина и снова высушивают[§§].
Рассчитывают величину Rf для каждой окрашенной зоны и проводят идентификацию аминокислот. Делают вывод о том, какая аминокислота находилась в субстратной смеси. Затем вырезают сегменты из каждого диска и складывают их вместе рядом, совмещая центральные зоны нанесения вещества.
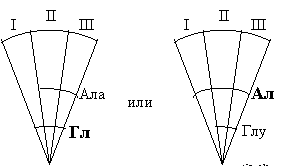
Пояснение к рисунку: Ала – аланин Глу – глутаминовая кислота
Выводы
6.4. Экспресс-метод определения повышенного содержания фенилаланина в плазме крови
Превращение незаменимой аминокислоты фенилаланина в заменимую – тирозин в организме человека осуществляется реакцией гидроксилирования, которую катализирует фермент фенилаланин-4-монооксигеназа (косубстратом служит тетрагидробиоптерин).
Врожденное отсутствие фенилаланин-4-монооксигеназы приводит к развитию тяжелого наследственного заболевания - фенилпировиноградной олигофрении (фенилкетонурии).
При этом, вследствие уменьшения потребления фенилаланина тканями, его концентрация в плазме крови резко возрастает (в норме содержание 0,1 ммоль/л, что соответствует 0,015 г/л).
Одновременно, в результате усиления реакции трансаминирования фенилаланина, в тканях повышается концентрация фенилпирувата – конкурентного ингибитора ферментов, участвующих в метаболизме пирувата. У ребенка наблюдается замедление умственного развития и развивается фенилпировиноградная олигофрения. В связи с этим чрезвычайно важно провести как можно более раннюю диагностику данной патологии (на 1-3 день рождения ребенка) и ввести строгую диету, исключающую фенилаланин из питания. Для раннего выявления отсутствия фенилаланин-4-монооксигеназы проводят определение повышенного содержания фенилаланина в плазме крови, которое довольно просто осуществить методом бумажной хроматографии.
Цель работы
Оценить методом бумажной хроматографии содержание фенилаланина в плазме крови обследуемого ребенка по сравнению с заведомо здоровым.
Принцип метода
Хроматографическое разделение образцов плазмы крови обследуемого ребенка и заведомо здорового в сравнении со стандартом, содержащем предельно допустимое количество фенилаланина (полуколичественное исследование).
Выполнение работы
Берут 3 диска хроматографической бумаги диаметром 12 см.
На I диск наносят 2 мкл плазмы крови обследуемого ребенка. На II диск – 2 мкл плазмы крови заведомо здорового ребенка (концентрация фенилаланина 0,015 г/л). На III диск – 2 мкл стандартного раствора фенилаланина (концентрация 0,06 г/л) и 2 мкл плазмы крови здорового ребенка. Общая концентрация фенилаланина 0,075 г/л.

Нанесение растворов на хроматографические диски, проведение хроматографии и проявление хроматограмм проводят так же, как в предыдущей работе «Доказательство проявления активности АлАТ методом бумажной хроматографии».
Сравнивают полученные хроматограммы по интенсивности окраски фенилаланина на всех трех дисках и делают вывод о содержании фенилаланина в плазме крови обследуемого ребёнка.
Выводы
Тестовые задания по теме: «Обмен аминокислот»
1) Ответить на каждый вопрос однозначно: «да» или «нет»
1. Гистидин в печени способен дезаминироваться по внутримолекулярному типу.
2. Восстановленные коферменты оксидаз аминокислот могут непосредственно окисляться молекулярным кислородом.
3. Дезаминирование глутаминовой кислоты сопровождается промежуточным образованием иминокислоты.
4. Коферментом моноаминоксидаз (МАО) служит ФАД.
5. Декарбоксилирование аминокислот является необратимым процессом.
6. Аммиак образуется при любом типе дезаминирования аминокислот.
7. Обладает ли гистамин сосудосуживающим действием?
8. Является ли дофамин предшественником норадреналина?
9. Возможно ли декарбоксилирование 5-окситриптофана в организме человека?
10. Все ли природные аминокислоты могут "сгорать" в ЦТК?
11. Может ли из аланина образоваться глюкоза в организме человека?
12. Относится ли лейцин к кетогенным аминокислотам?
2) Выбрать один правильный ответ
Коферментом большинства декарбоксилаз аминокислот является: 1. ФАД 2. ФМН 3. ПФ 4. ТПФ 5. НАДФ | Декарбоксилирование аминокислот приводит к образованию: 1. спирта 2. альдегида 3. амина 4. амида 5. кетона |
3) Установить соответствие фермента, участвующего в обмене АМК, и соответствующего кофермента
1. аминотрансферазы 2. глутаматдегидрогеназа 3. моноаминооксидазы 4. сериноксиметилтрансфераза | А. ТГФК Б. ФАД В. НАД + Г. ПФ |
6.5. Количественное определение мочевины в моче ферментативным уреазным/фенол-гипохлоритным методом
Мочевина – основной конечный продукт обмена белков в организме человека. На долю мочевины приходится 80-90% выделяемого с мочой азота.
Биологическая роль синтеза мочевины в печени (орнитиновый цикл мочевинообразования Кребса) заключается в связывании образующегося при дезаминировании аминокислот аммиака в относительно малотоксичную молекулу мочевины, которая затем экскретируется с мочой.
Зная количество экскретируемой за сутки мочевины и количество азота, поступающего с пищей, можно вычислить азотистый баланс, который является важным показателем состояния белкового и аминокислотного обмена. Азотистый баланс может быть:
1) положительным – у детей, у выздоравливающих после тяжелой болезни;
2) отрицательным – при тяжелых заболеваниях, в том числе онкологических, при голодании и в старческом возрасте;
3) равным нулю (азотистое равновесие) – у здоровых взрослых людей (при нормальном питании).
Всякое повышение белкового обмена, процессы интенсивного распада белка (опухоли, гипертиреоз, диабет) сопровождаются усилением мочевинообразования и увеличением количества мочевины, выделяемой с мочой за стуки. Патологические изменения печени, приводящие к ее функциональной недостаточности, а, следовательно, нарушению синтеза мочевины, сопровождаются понижением количества мочевины в крови и моче. Функциональная недостаточность почек ведет к понижению количества мочевины в моче и одновременному повышению ее содержания в крови (уремия). Некоторые формы диабета, характеризующиеся повышенным аппетитом и прогрессирующим исхуданием больного, сопровождаются повышением выделения мочевины с мочой за счет усиленного распада белков.
Цель работы
Определить содержание мочевины в суточной моче и сравнить с нормой.
Принцип метода
Метод – ферментативный, основан на реакции расщепления молекулы мочевины под действием высокоспецифического фермента – уреазы – до аммиака и углекислого газа, которые в водном растворе образуют карбонат аммония.
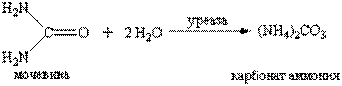
Ионы аммония в присутствии нитропруссида натрия реагируют с фенолом и гипохлоритом натрия. В результате реакции образуется индофенол (синего цвета), интенсивность окрашивания которого пропорциональна концентрации ионов аммония (и, соответственно, мочевины).
Выполнение работы (см. приложение )
Для исследования берут следующие пробы (3 промаркированные пробирки): опыт (разведенная моча), стандарт (стандартный раствор мочевины 0,03 г/л) и контроль (вода). Все реактивы вносят, согласно описанию в таблице:
Реактивы и этапы | Опыт | Стандарт | Контроль |
Моча 1:1000, мл | 0,1 | — | — |
Стандарт 0,03 г/л, мл | — | 0,1 | — |
Вода дистиллированная, мл | — | — | 0,1 |
Раствор уреазы, мл | 0,1 | 0,1 | 0,1 |
Перемешивают. Инкубируют 5 минут при 20°С. | |||
Фенол + нитропруссид натрия, мл | 1,0 | 1,0 | 1,0 |
Щелочной раствор гипохлорита натрия, мл | 1,0 | 1,0 | 1,0 |
Вода дистиллированная (мл) | 1,0 | 1,0 | 1,0 |
Перемешивают. Инкубируют 15 минут при 37°С. | |||
Фотометрируют против Н2О (l = 540 нм, толщина кюветы 0,5 см). D540 | |||
Dоп - Dк | |||
Dст - Dк |
На студенческую группу ставят 2 контроля и 2 стандарта. Остальные студенты делают опытные пробы.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 |



 Диски
Диски