Пояснение:
1. нагревание вызывает денатурацию белка, сопровождающуюся помутнением раствора
2. минеральные и органические кислоты вызывают дегидратацию и перезарядку части белковых молекул, сопровождающуюся их денатурацией
3. тяжелые металлы вызывают денатурацию белка, что обусловлено адсорбцией тяжелых металлов на поверхности белковой молекулы и образованием нерастворимого комплекса
4. органические растворители снимают гидратную оболочку и понижают устойчивость белка в растворе. Но осадок выпадает только в нейтральных и слабо кислых растворах. Длительное действие органического растворителя вызывает денатурацию белка.
Выводы
Тестовые задания по теме: «Аминокислоты и простые белки»
1) Ответить на каждый вопрос однозначно: «да» или «нет»
1. Аспарагин содержит амидную группу.
2. Наличие электрических зарядов стабилизирует белковые молекулы в растворе.
3. Ксантопротеиновая реакция характерна для циклических аминокислот.
4. Смесь свободных аминокислот дает положительную нингидриновую реакцию.
5. Высаливание белков наиболее эффективно в изоэлектрической точке.
6. Аминокислота серин содержит свободную гидроксильную группу.
7. Обладают ли валин, лейцин и изолейцин гидрофобными свойствами?
8. Все ли белки растворимы в воде?
9. Разрываются ли пептидные связи при тепловой денатурации белка?
10. Дает ли смесь свободных аминокислот положительную биуретовую реакцию?
11. Входит ли орнитин в состав природных белков?
12. Можно ли рассматривать метионин как производное масляной кислоты?
2) Выбрать один правильный ответ
К неполярным (гидрофобным) аминокислотам относится: серин треонин лизин валин цистеин | Биуретовая реакция не дает окраски с: простыми белками дипептидами трипептидами желатиной |
3) Найти соответствие:
АМК | Радикал |
Асн Лей Глу Арг | А. гидрофильный с анионной группой Б. гидрофобный В. гидрофильный с незаряженной группой Г. гидрофильный с катионной группой |
1.3. Количественное определение белка биуретовым методом. Построение калибровочных кривых
Определение концентрации белка проводят в научных учреждениях при изучении, выделении и очистке белков; в промышленности в процессе получения ферментов, пищевых белков, белковых лекарственных препаратов; в медицинских биохимических лабораториях для оценки состояния печени и почек.
Существует много разных методов количественного определения белков. Среди них широкое распространение получили колориметрические методы, основанные на способности белков давать окрашенные комплексы с рядом реактивов (цветные реакции). Среди этих методов наиболее распространены биуретовый метод и его модификация (метод Лоури[‡]).
Цель работы
Освоить работу фотоэлектроколориметра (ФЭК). Научиться строить стандартные калибровочные кривые. Определить содержание белка в пробе с неизвестной концентрацией.
Принцип метода
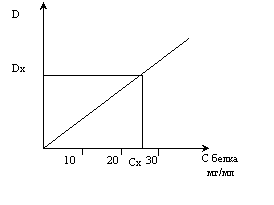
Биуретовый метод основан на образовании окрашенного в фиолетовый цвет комплекса пептидных связей белка с ионами двухвалентной меди в щелочной среде (биуретовая реакция). Интенсивность развивающейся окраски раствора прямо пропорциональна концентрации белка и определяется фотометрически. Для количественного определения белка измеряют интенсивность окраски стандартных растворов белка с известной концентрацией (величину оптической плотности Dст). По полученным данным строят график зависимости оптической плотности окрашенных растворов от концентрации в них белка (стандартную калибровочную кривую). На оси ординат всегда откладывают величину D как функцию от задаваемых значений (см. рисунок).
Измеряют оптическую плотность Dх окрашенного раствора с неизвестной концентрацией белка и по стандартной кривой определяют в нем концентрацию белка. В качестве стандартного белка обычно используют раствор сывороточного альбумина.
Выполнение работы
Реактивы, мл | Контроль | Стандартный белок 10 мг/мл | Стандартный белок 20 мг/мл | Стандартный белок 30 мг/мл | Неизвестный белок Х мг/мл |
Раствор сывороточного альбумина, мл | — | 0,2 | 0,2 | 0,2 | 0,2 |
Н2О, мл | 0,2 | — | — | — | — |
Биуретовый реактив*, мл | 5 | 5 | 5 | 5 | 5 |
Перемешивают и инкубируют 30 минут при комнатной температуре | |||||
Фотометрируют против Н2О (l = 545 нм, толщина кюветы 1 см). D545 | |||||
Dст – Dк; Dх – Dк | |||||
*Биуретовый реактив: исходный концентрат (медь сернокислая – 120 ммоль/л, калий иодистый – 300 ммоль/л, калий-натрий виннокислый – 320 ммоль/л, гидроксид натрия –3 моль/л) разводят перед работой 1:19
 Оформление работы
Оформление работы
В рабочей тетради записать и заполнить таблицу; построить стандартную кривую и определить по ней концентрацию белка в неизвестном растворе.
Выводы
 Тестовые задания по теме: «Аминокислоты и простые белки»
Тестовые задания по теме: «Аминокислоты и простые белки»
1) Ответить на каждый вопрос однозначно: «да» или «нет»
1. Имидазольное кольцо гистидина содержит 1 атом азота.
2. N-концевая аминокислота в дипептиде гистидиллизин - гистидин.
3. С-концевая аминокислота в трипептиде серилпролилглицин - глицин.
4. Альбумины сыворотки крови выполняют транспортную функцию.
5. Пролин содержит имино-группу.
6. Аспарагиновая кислота является производным янтарной кислоты.
7. Все ли пептиды дают положительную биуретовую реакцию?
8. Зависит ли интенсивность окраски вещества в растворе от его концентрации?
9. Можно ли разделить белки методом высаливания, используя сернокислую медь (сульфат меди)?
10. Встречаются ли в организме человека аминокислоты, которые не входят в состав белков?
11. Участвует ли ε-NH2-группа лизина в образовании пептидной связи в белках?
12. Обладают ли радикалы серина и валина гидрофильными свойствами?
2) Выбрать один правильный ответ
Аминокислота с незаряженным радикалом: треонин лизин аргинин гистидин глутаминовая кислота | Для определения оптической плотности синего раствора используют светофильтр: голубой желтый красный зеленый синий |
3) Найти соответствие
АМК | Химическая группа в составе радикалов |
метионин серин аргинин цистеин аспарагин | А. гидроксильная Б. амидная В. тиометильная Г. гуанидиловая Д. сульфгидрильная |
 1.4. Диализ белков. Бумажная хроматография аминокислот
1.4. Диализ белков. Бумажная хроматография аминокислот
I. А. Диализ
Диализом называют процесс разделения высокомолекулярных веществ (например, белков) и низкомолекулярных (например, солей) с помощью полупроницаемых мембран.
Полупроницаемыми называют мембраны, диаметр пор которых позволяет проходить только низкомолекулярным соединениям. Примером естественных полупроницаемых мембран могут быть капсулы Боумена—Шумлянского почек. Широко используют искусственные полупроницаемые мембраны: целлофан, коллодий, на основе которых созданы диализаторы, в том числе «искусственная почка».
Метод диализа используют в научных лабораториях, в промышленности, в клинической практике.
Цель работы
Доказать, что низкомолекулярное соединение NaCl проходит через полупроницаемую мембрану, а высокомолекулярный белок не проходит и остается в диализируемом растворе.
Принцип метода
Метод основан на том, что низкомолекулярные вещества легко диффундируют через полупроницаемые мембраны в чистый растворитель, образуя диализат. Диффузия будет продолжаться, пока не произойдет выравнивание концентраций диффундируемого вещества между диализируемым раствором и диализатом. Процесс возобновится, если диализат заменить чистым растворителем или, если эта смена будет происходить постоянно (проточный диализ).
Выполнение работы
Подготовка диализатора: полупроницаемой мембраной могут быть диализные трубки или целлофановые диализные мешочки. Целлофан (квадрат 10х10 см) смачивают дистиллированной водой, делают в нем углубление и получают диализный мешочек.
Приготовление диализируемого раствора: в диализный мешочек помещают 20 капель разведенного яичного белка в 5 % растворе NaCl (белок одного яйца разводят в 300 мл 5% раствора NaCl) и перемешивают. Края целлофана зажимают между двумя стеклянными палочками, скрепленными между собой резиновыми кольцами.
Диализ. Мешочек с солевым раствором белка помещают в стакан с дистиллированной водой так, чтобы часть мешочка с раствором белка была полностью погружена в воду. Сразу же, на просвет можно заметить струйки солевого раствора, опускающиеся из мешочка на дно стакана, что обусловлено изменением рефракции воды.
Анализ результатов диализа. Через 60 мин после начала диализа проводят качественные пробы на белок (биуретовую реакцию) и на NaCl (с AgNO3) в соответствии с таблицей.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 |



