138. При какой температуре замерзает раствор, содержащий 14,4 г глюкозы 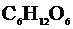 в 200 мл воды. Криоскопическая константа воды
в 200 мл воды. Криоскопическая константа воды ![]()
![]() .
.
139. При какой температуре замерзает раствор, содержащий 3 г мочевины в 200 мл воды. Криоскопическая константа воды ![]()
![]() .
.
140. При какой температуре кипят и замерзают водные растворы неэлектролитов, моляльность которых равна 1 моль/кг. Криоскопическая константа воды ![]()
![]() . Эбуллиоскопическая константа воды
. Эбуллиоскопическая константа воды ![]()
![]() .
.
1.8. Ионно – молекулярные (ионные) реакции обмена
Для решения задач этого раздела рекомендуем воспользоваться литературой 4, 6, 8, 14 и таблицей 7.
Электролиты – вещества, которые в растворенном или расплавленном состоянии проводят электрический ток. При растворении в воде или других полярных растворителях электролиты подвергаются электролитической диссоциации, т. е. в большей или меньшей степени распадаются на положительно и отрицательно заряженные ионы – катионы и анионы.
Уравнения диссоциации обычно записываются следующим образом:
![]() ;
; 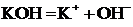
![]()
Нужно иметь ввиду, что эти уравнения только приблизительно отображают подлинный процесс диссоциации, поскольку не показано участие молекул растворителя, без которого сама диссоциация невозможна.
Электролиты практически полностью диссоциирующие на ионы называются сильными электролитами. К ним относятся большинство неорганических солей, гидроксиды щелочных металлов, растворимые гидроксиды щелочноземельных металлов, некоторые минеральные кислоты, например, ![]()
Электролиты, диссоциирующие в растворах не полностью, называются слабыми электролитами. К ним относятся почти все органические кислоты, некоторые минеральные кислоты, например, , многие основания металлов, а также ![]() .
.
В растворах слабых электролитов устанавливается равновесие между недиссоциированными молекулами и продуктами их диссоциации – ионами. В этом случае можно применить законы химического равновесия и записать выражение константы равновесия. Например, в водном растворе уксусной кислоты устанавливается равновесие:
![]() ⇄
⇄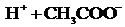
которое характеризуется константой равновесия (константой диссоциации):
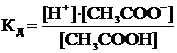 .
.
Величина ![]() зависит от природы электролита и растворителя, от температуры, но не зависит от концентрации раствора. Она характеризует способность данного электролита распадаться на ионы: чем выше
зависит от природы электролита и растворителя, от температуры, но не зависит от концентрации раствора. Она характеризует способность данного электролита распадаться на ионы: чем выше ![]() , тем легче электролит диссоциирует.
, тем легче электролит диссоциирует.
В табл. 4 приведены значения констант диссоциации некоторых слабых электролитов.
Количественно процесс электролитической диссоциации выражают с помощью степени диссоциации (![]() ), т. е. доли молекул, распавшихся на ионы. Степень диссоциации представляют в процентах или в долях единицы:
), т. е. доли молекул, распавшихся на ионы. Степень диссоциации представляют в процентах или в долях единицы:
![]() ,
,
где n – число молекул, распавшихся на ионы, n0 – общее число растворенных молекул.
Ионно-молекулярные, или просто ионные, уравнения реакций обмена отражают состояние электролита в растворе. В этих уравнениях сильные растворимые электролиты, поскольку они полностью диссоциированы, записывают в виде ионов, а слабые электролиты, малорастворимые и газообразные вещества записывают в молекулярной форме.
В ионно-молекулярном уравнении одинаковые ионы из обеих его частей исключаются. При составлении ионно-молекулярных уравнений следует помнить, что сумма электрических зарядов в левой части уравнения должна быть равна сумме электрических зарядов в правой части уравнения.
Пример 1. Написать ионно-молекулярные уравнения реакций взаимодействия между водными растворами следующих веществ: а) ![]() и
и ![]() ; б)
; б) ![]() и
и ![]() ; в)
; в) ![]() и
и  ; г)
; г) 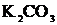 и
и 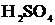 ;
;
д) 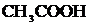 и
и 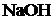 .
.
Решение: запишем уравнения взаимодействия указанных веществ в молекулярном виде:
а) ![]() +
+ 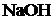 =
= ![]() +
+ ![]()
б) ![]() +
+ ![]() =
= ![]()
![]() +
+ 
в) 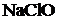 +
+ ![]() =
= 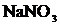 +
+ ![]()
г) 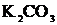 +
+ ![]() =
= ![]() +
+ ![]() ↑ +
↑ + ![]()
д) 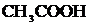 +
+ ![]() ⇄
⇄ 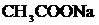 +
+ ![]()
Отметим, что взаимодействие этих веществ возможно, ибо в результате происходит связывание ионов с образованием слабых электролитов (![]() ,
, ![]() ), осадка (
), осадка (![]() ↓), газа (
↓), газа (![]() ↑).
↑).
В реакции (д) имеются два слабых электролита - ![]() и
и ![]() , но так как реакции идут в сторону большего связывания ионов и вода – более слабый электролит, чем уксусная кислота, то равновесие реакции смещено в сторону образования воды. Исключив одинаковые ионы из обеих частей равенства: а)
, но так как реакции идут в сторону большего связывания ионов и вода – более слабый электролит, чем уксусная кислота, то равновесие реакции смещено в сторону образования воды. Исключив одинаковые ионы из обеих частей равенства: а) ![]() и
и ![]() ; б)
; б) ![]() и
и ![]() ; в)
; в) ![]() и NO
и NO![]() ; г) K+ и
; г) K+ и ![]() д)
д) ![]() , получим ионно-молекулярные уравнения реакций, которым соответствуют следующие ионно-молекулярные реакции:
, получим ионно-молекулярные уравнения реакций, которым соответствуют следующие ионно-молекулярные реакции:
а) ![]() +
+ ![]() =
= ![]()
б) ![]() +
+ ![]() =
= ![]()
в) ![]() +
+ ![]() =
= ![]()
г) ![]() + 2
+ 2![]() =
= ![]() +
+ ![]()

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 |



