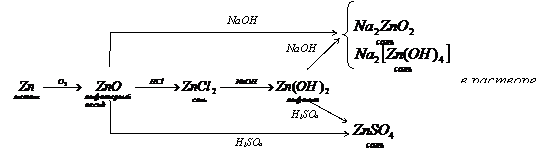Группа | I | II | III | IV | V | VI | VII | VIII |
s-элементы | р-элементы | |||||||
Валентные электроны | s1 | s2 | s2р1 | s2р2 | s2р3 | s2р4 | s2р5 | s2р6 |
Элемент Степени окисления | Li 1 | Be 2 | B 3 | C 4,2 -4 | N 5,3 -3 | O 2 -2 | F - -1 | Ne - - |
Элемент Степени окисления | Na 1 | Mg 2 | Al 3 | Si 4,2 -4 | P 5,3 -3 | S 6,4 -2 | Cl 1,3,5,7 -1 | Ar - - |
Элемент Степени окисления | K 1 | Ca 2 | Ga 3 | Ge 4,2 -4 | As 5,3 -3 | Se 6,4 -2 | Br 1,3,5,7 -1 | Kr 2,4 - |
Элемент Степени окисления | Rb 1 | Sr 2 | In 3 | Sn 4,2 -4 | Sb 5,3 -3 | Te 6,4 -2 | I 1,3,5,7 -1 | Xe 2,4,6,8 - |
Элемент Степени окисления | Cs 1 | Ba 2 | Tl 1,3 | Pb 2,4 -4 | Bi 3,5 -3 | Po 4,6 -2 | At 5,7 -1 | Rn (2,4,6,8) - |
Серым выделены символы неметаллов
Таблица 9. Основные классы неорганических веществ.
Вещества | Классификация | Примеры | |
Простые | Металлы | s–элементы (кроме Н, Не) р–элементы Al, Ga, In, Tl, Ge, Sn, Pb, Sb, Bi d–элементы f–элементы | |
Неметаллы | s–элементы Н, Не р–элементы B, C, Si, N, P, As, O, S, Se, Te галогены (VII A группа) благородные газы (VIII A группа) | ||
Сложные | Бинарные соединения | гидриды карбиды нитриды оксиды сульфиды галиды | LiH, NaH, CaH2, AlH3 Be2C, CaC2, Al4C3 Na3N, Mg3N2, Si3N4 Na2O, CaO, Al2O3, SO3 K2S, ZnS, Fe2S3 NaCl, BaCl2, FeCl3 |
Вещества | Классификация | Примеры | |
Сложные | Гидроксиды | кислоты основания амфолиты (амфотерные) | HNO3, H2SO4, H3PO4 KOH, Ba(OH)2, Ni(OH)3 Э(ОН)n = Н nЭОn Форма основания: Zn(OH)2, Al(OH)3, Be(OH)2 Форма кислоты: H2ZnO2, H3AlO3, H2BeO2 |
Соли | средние кислые основные | NaNO3, Al2(SO4)3, K3PO4, KCl NaHSO4, KH2PO4, Ca(HCO3)2 MgOHCl, (CuOH)2SO4, Fe(OH)2Cl |
Таблица 10. Взаимосвязь простых веществ, оксидов,
оснований и кислот (реакции солеобразования)
металл + кислота → соль + водород |
|
металл + неметалл → соль |
|
металл (1) + соль (1) → соль (2) + металл (1) |
|
основный оксид + кислотный оксид → соль |
|
основный оксид + кислота → соль + вода |
|
основание + кислота → соль + вода (реакция нейтрализации) |
|
основание + кислотный оксид → соль + вода |
|
основание(1)+соль(1)→основание (2) + соль(2) |
|
соль(1) + кислота(1) → соль(2) + кислота(2) |
|
соль(1) + соль(2) → соль(3) + соль(4) |
|
Амфотерные соединения могут проявлять и кислотные и основные свойства в зависимости от того, с чем реагируют:
|
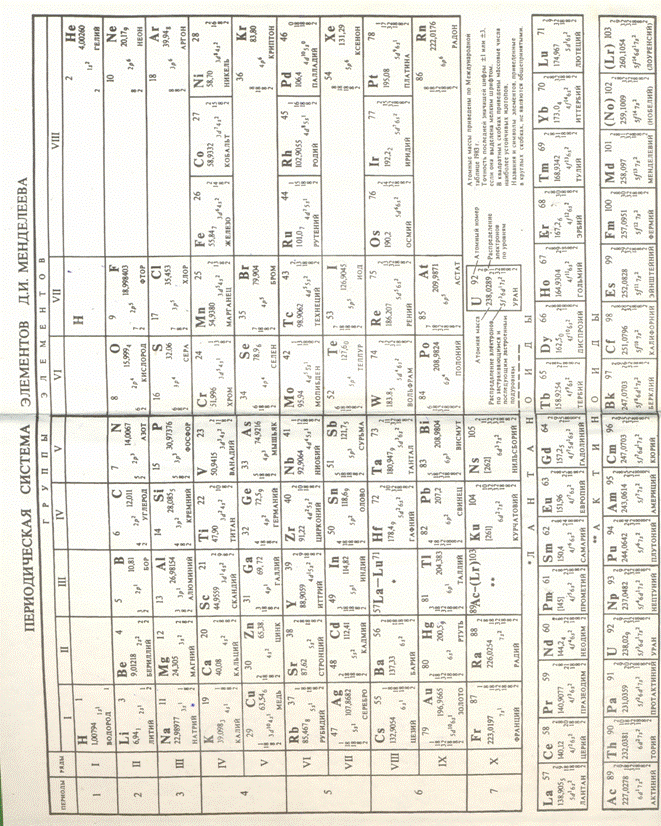
Таблица 11. Периодическая система элементов .

СПИСОК ЛИТЕРАТУРЫ
1. «Органическая химия». – М.: Высшая школа, 2000. – 559с.
2. , , Таперова работы по общей и неорганической химии. – М.: Химия, 1979.
3. Введение в общую химию/Под ред. . – М.: Высшая школа, 1980.
4. , , Юстратов химия.- СПб.: Издательство «Лань», 2003. – 336 с., ил. – (Учебник для вузов)
5. Глинка и упражнения по общей химии. – Л.: Химия, 2000.
6. Глинка химия. – Л.: Химия, 2004.
7. Гольбрайх задач и упражнений по химии. – М.: Высшая школа, 2001.
8. , , Сборник задач по химической термодинамике.-М.: Высшая школа, 1973.
9. Коровин химия: Учеб. для технических направ. и спец. вузов. – М.: Высшая школа, 2005. – 557 с.
10. Краткий справочник физико-химических величин под редакцией А. А , -Л.: Химия, 1986.
11. Курс общей химии/ Под ред. . – М.: Высшая школа, 1981.
12. Курс химии. Ч. 2, специальная для строительных вузов/ Под. Ред. . – М.: Высшая школа, 1974.
13. , Райцин по общей химии. – М.: высшая школа, 1978.
14. Лучинский химии. – М.: Высшая школа, 1985.
15. Павлов основы общей химии. – М.: Высшая школа, 1978.
16. , , Суханова задач и упражнений по общей химии: Учебное пособие для нехим. спец. вузов/ – М.: Высшая школа, 1991.-288 с.
17. Семчиков соединения. – М.: Издательский центр «Академия», 2003. – 368 с.
18. , «Химия и физика полимеров». – М.: Химия, 1989. – 432с.
19. Фролов . – М.: Высшая школа, 1979.
20. , , Харина химии. – М.: Высшая школа, 1983.
21. «Энциклопедия полимеров» гл. ред. . – М.: Советская энциклопедия, 1972. 1-3 том.
СОДЕРЖАНИЕ
КАФЕДРА ОБЩЕЙ И СПЕЦИАЛЬНОЙ ХИМИИ.. 3
ОБЩИЕ МЕТОДИЧЕСКИЕ УКАЗАНИЯ.. 3
ПРОГРАММА.. 5
КОНТРОЛЬНЫЕ ЗАДАНИЯ.. 12
1. Задания к контрольной работе №1. 12
1.1. Моль. Эквиваленты и мольные массы эквивалентов простых и сложных веществ. Закон эквивалентов. 12
1.2. Энергетика химических процессов (термохимические расчеты) 18
1.3. Химическое сродство. 23
1.4. Химическая кинетика. 28
1.5. Химическое равновесие. 33
1.6.Способы выражения концентрации раствора. 39
1.7. Свойства растворов. 46
1.8. Ионно – молекулярные (ионные) реакции обмена. 51
1.9. Гидролиз солей. 57
2. Задания к контрольной работе №2. 64
2.1. Окислительно – восстановительные реакции. 64
2.2. Электродные потенциалы и электродвижущие силы.. 74
2.3. Коррозия металлов. 85
2.4. Электролиз. 90
2.5. Свойства соединений s-, p-, d – элементов. 96
2.6. Жесткость воды и методы её устранения. 103
2.7. Органические соединения. Полимеры. 107
2.8. Дисперсные системы. 112
ТАБЛИЦА ВАРИАНТОВ КОНТРОЛЬНЫХ ЗАДАНИЙ.. 120
ПРИЛОЖЕНИЕ.. 127
СПИСОК ЛИТЕРАТУРЫ... 134

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 |