Все реакции можно разделить на две группы: в одних степень окисления атомов остается постоянной, в других она меняется. К первым относятся обменные реакции, некоторые процессы синтеза и распада веществ. В отличие от них протекание окислительно-восстановительных реакций связано со сдвигом или полным переходом электронов от одних атомов (ионов) к другим – от восстановителя к окислителю.
Об окислительно-восстановительных свойствах элементов и соединений можно судить, руководствуясь периодической системой .
Типичными окислителями являются:
· простые вещества, атомы которых обладают большой электроотрицательностью (элементы VIA и VIIA групп); из них наиболее активен фтор (F);
· ионы с дефицитом электронов: простые катионы с высшей или большей степенью окисления, например: ![]()
![]()
![]()
· растворы кислот.
Растворы кислот – более сильные окислители, чем растворы их солей, причем окислительная активность кислот возрастает с ростом концентрации.
Типичные восстановители:
· элементы, атомы которых обладают наименьшей электроотрицательностью (элементы основных подгрупп I и II группы)
· анионы, как простые, например ![]() , так и сложные, в которых более электроотрицательный элемент не имеет предельной степени окисления, например
, так и сложные, в которых более электроотрицательный элемент не имеет предельной степени окисления, например ![]() .
.
· катионы, у которых степень окисления может возрасти, например ![]()
· некоторые вещества при высоких температурах, например С, СО, ![]() .
.
В качестве восстановителей применяют также нагретые магний (Mg), алюминий (Al), цинк (Zn), железо (Fe) и некоторые другие металлы. Восстановительная активность металла тем больше, чем меньше их потенциал ионизации.
Вещества, содержащие элементы в максимальной и минимальной степенях окисления, могут быть соответственно только окислителями или только восстановителями. Вещества, содержащие вещества в промежуточной степени окисления, могут быть как окислителями (под влиянием более активного, чем они восстановителя), так и восстановителями (под влиянием более энергичного, чем они, окислителя).
Степень окисления – это тот условный заряд, который приобрёл бы атом элемента, если предположить, что он принял или отдал то или иное число электронов.
Пример 1.
Исходя из степени окисления (n) азота, серы и марганца в соединениях 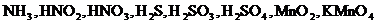 , определите, какие из них могут быть только восстановителями, только окислителями и какие проявляют как окислительные, так и восстановительные свойства.
, определите, какие из них могут быть только восстановителями, только окислителями и какие проявляют как окислительные, так и восстановительные свойства.
Решение: степень окисления (n) азота (N) в указанных соединениях соответственно равна: ![]() (низшая),
(низшая), ![]() промежуточная),
промежуточная), ![]() (высшая); степень окисления серы (S) соответственно равна:
(высшая); степень окисления серы (S) соответственно равна: ![]() (низшая),
(низшая), ![]() (промежуточная),
(промежуточная), ![]() (высшая); степень окисления марганца (Mn) соответственно равна:
(высшая); степень окисления марганца (Mn) соответственно равна: ![]() (промежуточная),
(промежуточная), ![]() (высшая). Из этого следует, что
(высшая). Из этого следует, что 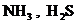 – только восстановители;
– только восстановители; ![]() – только окислители;
– только окислители; 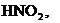
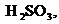
 – окислители и восстановители.
– окислители и восстановители.
Пример 2.
Могут ли происходить окислительно-восстановительные реакции (ОВР) между следующими веществами: а) ![]() и
и ![]() ; б)
; б) ![]() и
и ![]() ; в)
; в) ![]() и
и ![]() ?
?
Решение: а) степень окисления в ![]()
![]() ; в
; в ![]()
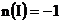 . Так как и сера и иод находятся в своей низшей степени окисления, то оба взятые вещества могут проявлять только восстановительные свойства и взаимодействовать друг с другом не могут; б) в
. Так как и сера и иод находятся в своей низшей степени окисления, то оба взятые вещества могут проявлять только восстановительные свойства и взаимодействовать друг с другом не могут; б) в 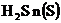
![]() (низшая); в
(низшая); в 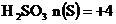 (промежуточная). Следовательно, взаимодействие этих веществ возможно, причём
(промежуточная). Следовательно, взаимодействие этих веществ возможно, причём ![]() является окислителем; в) в
является окислителем; в) в ![]() (промежуточная); в
(промежуточная); в ![]() (высшая). Взятые вещества могут взаимодействовать,
(высшая). Взятые вещества могут взаимодействовать, ![]() в этом случае будет проявлять восстановительные свойства.
в этом случае будет проявлять восстановительные свойства.
Рассмотрим составление ОВР на конкретных примерах.
1. Восстановление перманганата калия в кислой среде.
![]()
Ионная схема реакции:
![]()
Из составленной схемы видим, что ион ![]() окисляется в ион
окисляется в ион ![]() ,а ион
,а ион ![]() восстанавливается до иона
восстанавливается до иона ![]() . Причем степень окисления в первом случае возросла с
. Причем степень окисления в первом случае возросла с ![]() до
до ![]() , а во втором уменьшилась от
, а во втором уменьшилась от ![]() до
до ![]() . Таким образом, ион железа (
. Таким образом, ион железа (![]() ) будет окисляться, являясь при этом восстановителем, а
) будет окисляться, являясь при этом восстановителем, а ![]() будет восстанавливаться, являясь окислителем.
будет восстанавливаться, являясь окислителем.
Частичное уравнение окисления будет выглядеть следующим образом:
![]()
При написании частичного уравнения восстановления необходимо учесть наличие атомов кислорода в ионе ![]() . Для связывания их в молекулу воды нужно добавить ионы водорода из кислой среды и завершить баланс добавлением 5 электронов:
. Для связывания их в молекулу воды нужно добавить ионы водорода из кислой среды и завершить баланс добавлением 5 электронов:
![]()
При выводе общего уравнения реакции частичные уравнения надо умножить на такие множители, чтобы число потерянных и приобретенных электронов было одинаково.
![]() │
│![]() окисление (восстановитель)
окисление (восстановитель)
![]() │
│![]() восстановление (окислитель)
восстановление (окислитель)
После умножения каждого уравнения на коэффициенты и суммирования получим ионное уравнение ОВР:
![]()
В молекулярном виде:
![]()
2. Восстановление перманганата калия в щелочной среде
![]()
Ионное уравнение имеет вид:
![]()
Степени окисления меняются у марганца и серы.
Составим частичные уравнения окисления и восстановления:
![]() │
│ 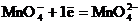 восстановление (окислитель)
восстановление (окислитель)
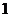 │
│ 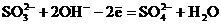 окисление (восстановитель)
окисление (восстановитель)
Чтобы восполнить недостаток атомов кислорода в левой части уравнения окисления, добавляют гидроксильные группы ![]() , тогда в правой части уравнения появляются молекулы
, тогда в правой части уравнения появляются молекулы ![]() .
.
Суммируем полученные уравнения:
![]()
Молекулярное уравнение:
![]()

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 |



