Химическая кинетика изучает скорость химических реакций (υ), которая определяется как изменение концентрации реагирующих веществ или продуктов реакции в единицу времени в постоянном реакционном пространстве.
В общем случае υ ![]() ,
,
где ∆C – изменение концентрации; τ – время протекания реакции в секундах.
Скорость реакции зависит от:
1. концентрации реагирующих веществ;
2. природы реагирующих веществ;
3. температуры реакционной смеси;
4. наличия катализатора в системе.
Зависимость скорости химической реакции от концентрации определяется законом действующих масс: скорость химической реакции пропорциональна произведению концентраций реагирующих веществ в степенях, равных их стехиометрическим коэффициентам.
Математическое выражение закона действующих масс для системы аА + bB = cC + dD выглядит следующим образом:
![]() ,
,
где k – коэффициент пропорциональности или константа скорости, которая не зависит от концентрации, но зависит от природы реагирующих веществ, температуры и катализатора;
[А] и [В] – концентрации веществ А и В;
a, b – стехиометрические коэффициенты.
Влияние температуры на скорость химической реакции определяется правилом Вант-Гоффа: при изменении температуры на каждые 10 градусов скорость реакции изменяется в 2-4 раза.
![]() ,
,
где υ2 и υ1 – скорости реакций при температурах Т2 и Т1 соответственно;
γ – температурный коэффициент Вант-Гоффа, который может принимать значения от 2 до 4;
∆Т = Т2 –Т1.
Если один из реагентов находится в твердой фазе (гетерогенная система), то скорость химической реакции зависит от общей поверхности твердого вещества или от степени его дисперсности. Однако в общем случае изучение скорости реакции проводят в условиях не изменяющейся поверхности. Тогда в выражение скорости реакции входит только концентрация жидкого или газообразного компонента и не входит площадь поверхности. Например, скорость реакции между поверхностью раскаленного угля и парами воды 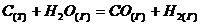 зависит только от концентрации водяного пара
зависит только от концентрации водяного пара
![]() .
.
В системах, где одно или несколько веществ являются газами, скорость химической реакции зависит также от внешнего давления. В этом случае в выражение скорости может быть введено значение парциального давления.
Пример 1. Во сколько раз изменится скорость прямой и обратной реакций в системе ![]() ⇄
⇄ 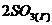 , если объем газовой смеси уменьшить в три раза?
, если объем газовой смеси уменьшить в три раза?
Решение: Обозначим концентрации реагирующих веществ: [SO2] = а; [O2] = b; [SO3] = с. Согласно закону действия масс скорости прямой и обратной реакции до изменения объема имеют следующие выражения:
![]()
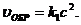
После уменьшения объема гомогенной системы в три раза концентрация каждого из реагирующих веществ увеличится в три раза, т. е. [SO2] = 3а; [O2] = 3b; [SO3] = 3с. Тогда при новых концентрациях скорости прямой и обратной реакций можно записать следующим образом:
![]() = k (3a)2 3b = 27 k a2 b;
= k (3a)2 3b = 27 k a2 b; ![]() = k1(3c)2 = 9 k c2
= k1(3c)2 = 9 k c2
Отсюда ![]() = 27 k a2 b/ k a2 b = 27;
= 27 k a2 b/ k a2 b = 27;
![]() = 9 k c2/ k1 c2 = 9.
= 9 k c2/ k1 c2 = 9.
Следовательно, скорость прямой реакции увеличится в 27 раз, а обратной – только в 9 раз.
Пример 2. Вычислить, во сколько раз увеличится скорость реакции, протекающей в газовой фазе, при повышении температуры от 30 до 70 °С.
Решение: Зависимость скорости химической реакции от температуры определяется эмпирическим правилом Вант-Гоффа по формуле:
υ2 = υ1∙γ∆T/10 = υ1∙270-30/10 = υ1∙24 = 16∙υ1
Следовательно, скорость реакции при температуре 70°С больше скорости реакции при температуре 30°С в 16 раз.
Контрольные вопросы
61. Напишите выражение для скорости химической реакции, протекающей в гомогенной системе по уравнению А + 2В = АВ2 и определите, во сколько раз увеличится скорость этой реакции, если: а) концентрация вещества А увеличится в 2 раза; б) концентрация вещества В увеличится в 2 раза; в) концентрация обоих веществ увеличится в 2 раза.
62. Во сколько раз следует увеличить концентрацию оксида углерода (II) в системе ![]() , чтобы скорость реакции увеличилась в 4 раза?
, чтобы скорость реакции увеличилась в 4 раза?
63. Во сколько раз следует увеличить давление, чтобы скорость образования NO2 по реакции ![]() ⇄
⇄ 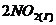 , возросла в 1000 раз?
, возросла в 1000 раз?
64. Напишите выражение для скорости реакции 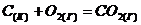 и определите, во сколько раз увеличится скорость реакции при увеличении концентрации кислорода в 3 раза.
и определите, во сколько раз увеличится скорость реакции при увеличении концентрации кислорода в 3 раза.
65. Реакция между оксидом азота (II) и хлором протекает по уравнению ![]() ⇄
⇄ 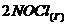 . Как изменится скорость реакции при увеличении: а) концентрации оксида азота в 2 раза; б) концентрации хлора в 2 раза; в) концентрации обоих веществ в 2 раза?
. Как изменится скорость реакции при увеличении: а) концентрации оксида азота в 2 раза; б) концентрации хлора в 2 раза; в) концентрации обоих веществ в 2 раза?
66. Во сколько раз увеличится константа скорости химической реакции при повышении температуры на 40°С, если γ = 3,2?
67. На сколько градусов следует повысить температуру системы, чтобы скорость протекающей в ней реакции возросла в 30 раз (γ = 2,5)?
68. При повышении температуры на 50°С скорость реакции возросла в 1200 раз. Вычислите температурный коэффициент реакции.
69. Вычислите температурный коэффициент реакции, если константа скорости ее при 120°С равна 6,7·10-2.
70. Реакция между веществами А и В выражается уравнением
А + 2В = С. Начальные концентрации соответственно равны 0,3 и 0,5 моль/л. Константа скорости равна 0,4 л2/(моль2∙с). Вычислите скорость реакции в начальный момент и в тот момент, когда концентрация вещества А уменьшилась на 0,1 моль/л.
71. Температурный коэффициент реакции равен 3. Вычислите, во сколько раз увеличится скорость реакции при увеличении температуры с 22 до 62°С?
72. Напишите математические выражения для определения скоростей следующих химических реакций, протекающих в гомогенной системе: a) ![]() ⇄
⇄ ![]() ;
;
б) ![]() ⇄
⇄ ![]() ;
;
в) ![]() ⇄
⇄ ![]() .
.
73. Напишите математические выражения для определения скоростей следующих химических реакций, протекающих в гетерогенной системе: а) ![]() ⇄
⇄ ![]() ;
;
б) ![]() ⇄
⇄ ![]() ;
;
в) ![]() ⇄
⇄ 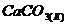 .
.
74. Определите, как изменится скорость прямой реакции
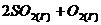 ⇄
⇄ 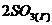 , если давление в системе увеличить в 5 раз?
, если давление в системе увеличить в 5 раз?
75. Как изменится скорость прямой реакции
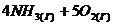 ⇄
⇄ 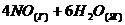 , если объем газовой смеси уменьшить в 2 раза?
, если объем газовой смеси уменьшить в 2 раза?
76. При повышении температуры на 30°С скорость химической реакции увеличилась в 64 раза. Вычислите, во сколько раз увеличится скорость этой реакции при повышении температуры на каждые 10°С.
77. Рассчитайте температурный коэффициент реакции, если при нагревании системы от 40°С до 80°С скорость возросла в 64 раза.
78. Температурный коэффициент реакции равен 3. При какой температуре следует проводить эту реакцию, чтобы скорость реакции, идущей при 100°С, уменьшилась в 27 раз?
79. Как изменится скорость прямой и обратной реакции, если объем газовой смеси ![]() ⇄
⇄ 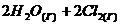 увеличить в 2 раза?
увеличить в 2 раза?
80. Во сколько раз следует увеличить давление в системе
![]() ⇄
⇄ ![]() , чтобы скорость образования HI возросла в 100 раз?
, чтобы скорость образования HI возросла в 100 раз?
1.5. Химическое равновесие
Для решения задач этого раздела рекомендуем воспользоваться литературой 6, 7, 9 и таблицей 1 ᾽᾽Стандартные энтальпии образования веществ᾽᾽.
Химические реакции бывают обратимыми и необратимыми. Для обратимых реакций характерно состояние химического равновесия.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 |



