305. Сополимеры. Классификация сополимеров. Примеры.
306. Процесс полимеризации. Механизм, способы инициирования, примеры реакции. Важнейшие полимеры, получаемые реакцией полимеризации.
307. Процесс поликонденсации. Раскройте механизм поликонденсации на примере получения фенол - формальдегидных смол.
308. Отличия процессов полимеризации и поликонденсации.
309. Классификация полимеров по строению макромолекулы.
310. Особенности химических реакций полимеров. Классификация химических процессов в полимерах, примеры.
311. Реакции сшивания полимеров (отверждение, вулканизация). Механизм и регулирование процесса, изменение физико – химических свойств в ходе реакции сшивания.
312. Три физических состояния аморфных полимеров. Температурные интервалы перехода из одного состояния в другое; изменение физико – химических свойств при этом.
313. Диффузия в полимерах. Растворимость полимеров. Процесс набухания. Структура растворов полимеров.
314. Механические свойства полимеров. Деформационные свойства полимеров. Упругая и неупругая деформации. Релаксационные процессы.
315. Деструкция полимеров. Основные виды деструкции. Стабилизация полимеров.
316. Полиэтилен. Способы получения, уравнение процесса. Физико – химические свойства, области применения в строительных материалах.
317. Акрилаты. Классификация. Физико – химические свойства, области применения в строительных материалах. Полиметилметакрилат: получение, уравнение процесса.
318. Поливинилхлорид и поливинилацетат. Получение. Физико – химические свойства, области применения в строительных материалах.
319. Полиуретаны. Получение. Физико – химические свойства, области применения в строительных материалах.
320. Полистирол. Получение. Физико – химические свойства, области применения в строительных материалах.
2.8. Дисперсные системы.
Для ответов на контрольные вопросы рекомендуем воспользоваться литературой 4, 9, 12, 16
Дисперсная система (ДС) – это система, в которой хотя бы одно вещество находится в раздробленном состоянии. Степень измельчения вещества характеризуется степенью дисперсности - величина обратная размеру частиц.
По степени дисперсности все ДС располагаются в непрерывный ряд:
Название | r, см > 10-3 10-4 ¸ 10-5 10-5 ¸ 10-7 <10-7 |
Гетерогенные cистемы Гомогенные системы | 1.Грубодисперсные 2.Микрогетерогенные 3.Высокодисперсные (коллоиды, золи) 4. Молекулярнодисперсные (истинные растворы) |
В гетерогенных ДС между дисперсной фазой (раздробленные частицы) и дисперсионной средой (сплошная среда) имеется поверхность раздела. Чем больше дисперсность, тем больше площадь этой поверхности.
Пример 1. Вычислить дисперсность, удельную и общую площадь поверхности частиц золя, полученного при дроблении 0,5 г вещества на частицы шарообразной формы диаметром 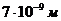 . Плотность вещества 19320 кг/м3.
. Плотность вещества 19320 кг/м3.
Решение: Степень дисперсности - величина обратная размеру частиц. ![]()
Удельная поверхность Sуд равна отношению площади поверхности раздробленных частиц S к объему дисперсной фазы V или ее массы m.
Для сферических частиц с радиусом r:
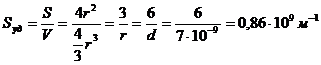
Находим объем вещества: ![]()
Находим общую площадь поверхности:
![]()
И удельную площадь, отнесенную к массе:
![]()
ДС классифицируют по агрегатному состоянию дисперсной фазы и среды: суспензии, лиозоли (Т-Ж), эмульсии (Ж-Ж), пены (Г-Ж), гели (Ж-Т), сплавы, солеозоли (Т-Т), твердые пены (Г-Т), и две разновидности аэрозолей (Т-Г и Ж-Г), где Т, Ж, Г - твердое, жидкое и газообразное тела.
Существуют лиофильные системы, в которых частицы имеют тесную связь с растворителем, и лиофобные, в которых частицы практически не растворяются в растворителе. Лиофильные системы являются термодинамически устойчивыми и образуются самопроизвольно. Лиофобные золи получают путем дробления частиц, исходя из грубодисперсных систем – диспергирование, или же путем агрегации из более мелких частиц - конденсация. В обоих случаях получаемая лиофобная ДС должна быть стабилизирована. Это достигается адсорбцией на поверхности частиц дисперсной фазы ПАВ (коллоидная защита) или ионов электролита-стабилизатора. Стабилизатор создает механический или электростатический барьер на поверхности частиц, препятствующий их слипанию.
Пример 2. Золь иодида серебра получен при добавлении к 30 мл 0,006 М раствора ![]() 40 мл 0,004 М раствора
40 мл 0,004 М раствора ![]() . Определить заряд частиц полученного золя и написать формулу его мицеллы. Какой электролит является стабилизатором для данного золя?
. Определить заряд частиц полученного золя и написать формулу его мицеллы. Какой электролит является стабилизатором для данного золя?
Решение: Золь получен методом конденсации по реакции обмена:
![]()
Нерастворимые молекулы хлорида серебра образуют ядро коллоидной частицы ![]() . Для того чтобы вместо осадка
. Для того чтобы вместо осадка ![]() образовался коллоидный раствор, необходимо условие: один из реагентов должен быть в избытке. Рассчитаем число молей нитрата серебра и иодида калия:
образовался коллоидный раствор, необходимо условие: один из реагентов должен быть в избытке. Рассчитаем число молей нитрата серебра и иодида калия:
![]()
![]()
т. к. ![]() >
> ![]() следовательно,
следовательно, ![]() взят в избытке и является стабилизатором.
взят в избытке и является стабилизатором.
Согласно правилу избирательной адсорбции Пескова – Фаянса, на поверхности ядра будут адсорбироваться ионы ![]() и частицы золя приобретают отрицательный заряд. Противоионами являются катионы
и частицы золя приобретают отрицательный заряд. Противоионами являются катионы ![]() . В целом мицелла нейтральна. Мицелла имеет строение:
. В целом мицелла нейтральна. Мицелла имеет строение:
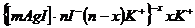 ,
,
где ![]() - ядро;
- ядро; ![]()
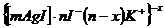 - гранула;
- гранула; ![]() - потенциалопределяющие (зарядообразующие) ионы, каким будет заряд этих ионов, таким будет и заряд гранулы;
- потенциалопределяющие (зарядообразующие) ионы, каким будет заряд этих ионов, таким будет и заряд гранулы; ![]() - адсорбционный слой – неподвижный;
- адсорбционный слой – неподвижный; ![]() - диффузный слой, подвижный.
- диффузный слой, подвижный.
Заряд коллоидных частиц можно установить экспериментально. Под действием постоянного электрического поля наблюдается перемещение гранул к противоположно заряженному электроду, диффузный слой передвигается в обратном направлении, увлекая за собой среду. Это явление называется электрофорез. Таким образом, приведенная в примере 2 гранула ![]() имеет отрицательный заряд и при электрофорезе движется к аноду, а среда – к катоду.
имеет отрицательный заряд и при электрофорезе движется к аноду, а среда – к катоду.
В случае неподвижных частиц, передвигается только диффузный слой, это явление называется электроосмос.
Если заряд коллоидной частицы уменьшить до некоторого минимума, то устойчивость коллоидного раствора нарушится, произойдет слипание и соединение частиц в более крупные агрегаты – коагуляция (коалесценция) и их осаждение - седиментация. Коагуляция золя происходит при добавлении электролита, добавлении противоположно заряженного золя, изменении температуры и др.
Коагуляция электролитами происходит по определенным правилам:
1. Коагуляция начинается при определенной концентрации электролита. Минимальная концентрация электролита, вызывающая в системе коагуляцию, называется порогом коагуляции .Иногда вместо порога коагуляции используют величину γ, называемую коагулирующей способностью: ![]() .
.
2. Коагуляцию вызывают ионы - коагулянты, противоположные по знаку потенциалопределяющим ионам и заряду гранулы.
3. Порог коагуляции обратно пропорционален шестой степени заряда коагулирующего иона. По правилу Шульце-Гарди пороги коагуляции одно-, двух-, трех-, четырехзарядных ионов соотносятся как:
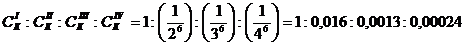
Соответственно коагулирующая способность подчиняется следующему соотношению: ![]()
Пример 3. Пороги коагуляции некоторого золя электролитами ![]()
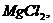
![]() равны соответственно 50,0; 0,8; 49,0 ммоль/л. Как относятся между собой величины коагулирующих способностей этих веществ? Укажите коагулирующие ионы. Каков знак заряда коллоидной частицы?
равны соответственно 50,0; 0,8; 49,0 ммоль/л. Как относятся между собой величины коагулирующих способностей этих веществ? Укажите коагулирующие ионы. Каков знак заряда коллоидной частицы?

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 |



