Химическое равновесие – это такое состояние системы, при котором скорости прямой и обратной реакций равны между собой, т. е.
![]() υпр = υобр
υпр = υобр
Равновесное состояние системы характеризуется константой химического равновесия. Так, например, для обратимой реакции
![]() ⇄
⇄ 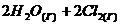
константа химического равновесия выражается следующим образом 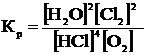
В общем случае в обратимых химических реакциях равновесие устанавливается в тот момент, когда отношение произведения концентраций продуктов реакции, возведенных в степени, равные стехиометрическим коэффициентам, к произведению концентраций исходных веществ, также возведенных в соответствующие степени, равно постоянной величине, называемой константой равновесия.
Константа равновесия зависит от природы реагирующих веществ и от температуры.
Концентрации, при которых устанавливается равновесие, называются равновесными. Изменение внешних условий, таких как температура, концентрация, давление, приводят к нарушению равновесия в системе и переходу ее в новое равновесное состояние.
Направление смещения равновесия определяется принципом Ле Шателье: если на систему, находящуюся в равновесии, производить какое-либо внешнее воздействие, то в этой системе самопроизвольно происходят процессы, ослабляющие оказанное воздействие.
Пример 1. Куда будет смещаться равновесие при изменении температуры для системы 2NO2 ⇄ N2O4; ∆H= -57 кДж/моль?
Решение: В ходе реакции наблюдается выделение теплоты, реакция является экзотермической. В соответствии с принципом Ле Шателье равновесие для данной системы будет смещаться в сторону ослабления оказанных воздействий. Значит, при повышении температуры равновесие смещается в сторону эндотермической реакции, т. е. влево. Если же температуру системы понижать, то равновесие сместится вправо, т. е. в сторону прямой реакции.
Пример 2. В какую сторону сместится равновесие в системе:
![]() ⇄
⇄ ![]() при уменьшении концентрации иода?
при уменьшении концентрации иода?
Решение: По принципу Ле Шателье изменение концентрации одного из исходных веществ приводит к определенным изменениям в равновесном состоянии системы. В конкретном случае при уменьшении концентрации иода равновесие сместится в сторону его воспроизведения, т. е. в сторону обратной реакции, в результате которой из иодоводорода и будет получаться дополнительное количество иода.
Пример 3. Как сместится равновесие в системе:
![]() ⇄
⇄ 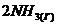 , если увеличить давление?
, если увеличить давление?
Решение: В соответствии с принципом Ле Шателье увеличение внешнего давления вызовет такие изменения, которые приведут к уменьшению давления в системе. Так как из 4 моль газа (из четырех объемов) образуется 2 моль (два объема) аммиака, то равновесие сместится вправо, т. е. в сторону меньшего объема.
Пример 4. Константа равновесия гомогенной системы:
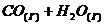 ⇄
⇄ 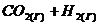 при 850°С равна 1. Вычислите концентрации всех веществ при равновесии, если исходные концентрации:
при 850°С равна 1. Вычислите концентрации всех веществ при равновесии, если исходные концентрации:
[СО]исх = 3 моль/л, [Н2О]исх = 2 моль/л.
Решение: При равновесии скорость прямой и обратной реакции равны, а отношение констант этих скоростей постоянно и называется константой равновесия данной системы:
υпр = k1[СО][Н2О]; υобр = k2[СО2][Н2];
![]()
В условии задачи даны исходные концентрации, тогда как в выражение ![]() входят только равновесные концентрации всех веществ системы. Предположим, что к моменту равновесия концентрация
входят только равновесные концентрации всех веществ системы. Предположим, что к моменту равновесия концентрация ![]() х моль/л. Согласно уравнению системы число молей образовавшегося водорода при этом будет также х моль/л. По столько же молей (х моль/л) СО и Н2О расходуется для образования СО2 и Н2. Следовательно, равновесные концентрации всех четырех веществ составляют:
х моль/л. Согласно уравнению системы число молей образовавшегося водорода при этом будет также х моль/л. По столько же молей (х моль/л) СО и Н2О расходуется для образования СО2 и Н2. Следовательно, равновесные концентрации всех четырех веществ составляют:
![]() ;
;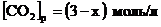 ;
;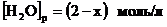 .
.
Зная константу равновесия, находим значение х, затем исходные концентрации всех веществ:
![]() ;
; ![]() ;
; 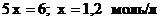 .
.
Таким образом, искомые равновесные концентрации:
[СО2]р = 1,2 моль/л; [Н2]р = 1,2 моль/л; [СО]р = 3-1,2 = 1,8 моль/л; [Н2О]р = 2-1,2 = 0,8 моль/л.
Контрольные вопросы
81. Напишите выражение для константы равновесия следующих обратимых процессов: а) ![]() ⇄
⇄ ![]()
б) ![]() ⇄
⇄ 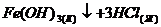
82. При синтезе аммиака равновесие установилось при следующих равновесных концентрациях веществ: [N2] = 2,5; [H2] = 1,8; [NH3] = 3,6 моль/л. Рассчитайте значение константы равновесия и исходные концентрации.
83. Как повлияет повышение давления и температуры на равновесие следующих обратимых реакций:
а) ![]() ⇄
⇄ 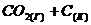 , ∆Н < 0
, ∆Н < 0
б) ![]() ⇄
⇄ ![]() , ∆H < 0
, ∆H < 0
в) 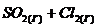 ⇄
⇄ 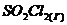 , ∆H > 0
, ∆H > 0
84. Используя справочные данные (табл. 1), определите, в какую сторону произойдет смещение равновесия гомогенных реакций:
![]() ⇄
⇄ 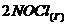 и
и 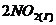 ⇄
⇄![]()
при следующих воздействиях:
а) охлаждение системы;
б) увеличение давления.
85. Константа равновесия для реакции 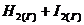 ⇄
⇄ ![]() равна 36, а начальные концентрации водорода и иода равны по 0,02 моль/л. Вычислить равновесные концентрации водорода, иода и иодоводорода.
равна 36, а начальные концентрации водорода и иода равны по 0,02 моль/л. Вычислить равновесные концентрации водорода, иода и иодоводорода.
86. Исходные концентрации ![]() и
и ![]() в гомогенной системе
в гомогенной системе 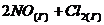 ⇄
⇄ 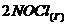 составляют соответственно 0,5 и 0,2 моль/л. Вычислите константу равновесия, если к моменту наступления равновесия прореагировало 20% NO.
составляют соответственно 0,5 и 0,2 моль/л. Вычислите константу равновесия, если к моменту наступления равновесия прореагировало 20% NO.
87. Почему при изменении давления смещается равновесие системы ![]() ⇄
⇄ 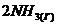 и не смещается равновесие системы
и не смещается равновесие системы ![]() ⇄
⇄ ![]() ? Мотивируйте ответ, используя расчет скоростей прямой и обратной реакций до и после изменения давления. Составьте уравнения для констант равновесия обеих систем.
? Мотивируйте ответ, используя расчет скоростей прямой и обратной реакций до и после изменения давления. Составьте уравнения для констант равновесия обеих систем.
88. При некоторой температуре равновесие в гомогенной системе ![]() ⇄
⇄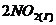 установилось при следующих концентрациях реагирующих веществ
установилось при следующих концентрациях реагирующих веществ ![]()
![]()
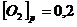
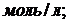
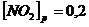
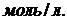 Вычислите константу равновесия и исходную концентрацию оксида азота и кислорода.
Вычислите константу равновесия и исходную концентрацию оксида азота и кислорода.
89. Константа равновесия гомогенной системы ![]() ⇄
⇄ 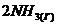 при некоторой температуре равна 0,2. Равновесные концентрации водорода и аммиака соответственно равны 0,4 и 0,15 моль/л. Вычислите исходную и равновесную концентрации азота.
при некоторой температуре равна 0,2. Равновесные концентрации водорода и аммиака соответственно равны 0,4 и 0,15 моль/л. Вычислите исходную и равновесную концентрации азота.
90. Константа равновесия системы при постоянной температуре ![]() ⇄
⇄ 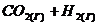 равна 1. Вычислите равновесные концентрации всех реагентов, если исходные концентрации составляют:
равна 1. Вычислите равновесные концентрации всех реагентов, если исходные концентрации составляют: ![]()
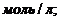
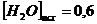


|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 |



