Вещество |
| Вещество |
|
С2Н2 (г) | + 226,75 | Н2О (г) | - 241,83 |
С2Н4 (г) | + 52,28 | Н2О (ж) | - 285,84 |
С2Н6 (г) | - 84,67 | Fe2O3 (к) | - 822,10 |
С2Н5ОН (г) | - 235,31 | Аl2О3 (к) | - 1669,80 |
СН4 (г) | - 74,85 | Са(ОН)2 (к) | - 986,50 |
NО (г) | + 90,37 | СаС2 (к) | - 59,83 |
N2O (г) | + 82.01 | НСl (г) | - 92,31 |
NH3 (г) | - 46,19 | NН4Сl (к) | - 315,39 |
СО2 (г) | - 393,51 | С2Н5ОН (ж) | -276,98 |
СО(г) | -110,53 | Н2О2 (ж) | -187,86 |
SO2 (г) | -296,90 | SO3 (г) | 395,85 |
Таблица 2. Стандартные абсолютные энтропии S0298 некоторых веществ
Вещество | S0298, Дж/моль · К | Вещество | S0298, Дж/моль · К |
С (графит) | 5,69 | СО (г) | 197,91 |
Мg (к) | 32,68 | С2Н2 (г) | 200.82 |
Na (к) | 51,21 | О2 (г) | 205,03 |
S (к, ромб) | 31,90 | Н2S (г) | 205,64 |
ВаО (к) | 213,80 | NO (г) | 210,20 |
СаО (к) | 38,07 | СО2 (г) | 213,65 |
МgO (к) | 61,50 | Сl2 (г) | 222,95 |
Н2О (ж) | 69,94 | NO2 (г) | 240,46 |
Вещество | S0298, Дж/моль · К | Вещество | S0298, Дж/моль · К |
Н2О (г) | 188,72 | SO2 (г) | 248,07 |
Н2 (г) | 130,59 | SO3 (г) | 256,69 |
Fe3O4 (к) | 146,19 | FeO (к) | 60,75 |
СН4 (г) | 186,19 | NaCl (к) | 72,13 |
НСl (г) | 186,68 | ВаСО3 (к) | 112,13 |
N2 (г) | 191,49 | СаСО3 (к) | 91,71 |
NH3 (г) | 192,50 | МgCO3 (к) | 65,10 |
Таблица 3. Стандартные энергии Гиббса образования ![]() G0298 некоторых веществ
G0298 некоторых веществ
Вещество |
| Вещество |
|
Fe (к) | 0 | N2 (г) | 0 |
S (к, ромб) | 0 | СО2 (г) | -394,38 |
Аl (к) | 0 | СО (г) | -137,27 |
Al2O3 (к) | -1582,27 | СН4 (г) | -50,79 |
ВаО (к) | -528,40 | С2Н2 (г) | +209,20 |
FeO (к) | -243,30 | NO (г) | +86, 69 |
Fe2O3 (к) | -740,34 | NH3 (г) | -16,48 |
Fe3O4 (к) | -1014.20 | Н2S (г) | -51,42 |
СаО (к) | -604,20 | Н2О (г) | -228,59 |
СuO (к) | -134,26 | Н2О (ж) | -237,19 |
МnO (к) | -363,34 | Н2О2 (ж) | -120,52 |
PbO (к) | -188,20 | ВаСО3 (к) | -1138,80 |
O2 (г) | 0 | СаСО3 (к) | -1128,75 |
Н2 (г) | 0 | MgCO3 (к) | -1012,15 |
MgO (к) | -569,27 |
Таблица 4. Константы диссоциации некоторых слабых электролитов
Электролит | КД |
Сернистая кислота H2SO3 | K1 = 1,3∙10-2 |
Угольная кислота H2CO3 | K1 = 4,45∙10-7 |
Cepoвoдородная кислота H2S | КД = 8,9∙10-8 |
Фосфорная кислота H3PO4 | КД = 7,11∙10-3 |
Таблица 5. Произведение растворимости малорастворимых гидроксидов в воде при 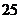
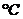 .
.
Электролит | ПР |
Al(OH)3 | 1,9∙10-33 |
Fe(OH)3 | 3,8∙10-38 |
Zn(OH)2 | 1,0∙10-17 |
Cd(OH)2 | 2,0∙10-14 |
Таблица 6. Стандартные электродные потенциалы (![]()
![]() )
)
некоторых металлов (ряд напряжений)
Уравнение электродного процесса | Стандартный потенциал ( | Уравнение электродного процесса | Стандартный потенциал ( |
Li++e-=Li | -3,045 | Co2++2e-=Co | -0,277 |
Rb++e-=Rb | -2,925 | Ni2++2e-=Ni | -0,250 |
K++e-=K | -2,925 | Sn2++2e-=Sn | -0,136 |
Cs++e-=Rb | -2,923 | Pb2++2e-=Pb | -0,126 |
Ca2++e-=Ca | -2,866 | Fe3++3e-=Fe | -0,036 |
Na++e-=Na | -2,714 | 2H++2e-=H2 | 0 |
Mg2++2e-=Mg | -2,363 | Bi3++3e-=Bi | 0,215 |
Al3++3e-=Al | -1,662 | Cu2++2e-=Cu | 0,337 |
Ti2++2e-=Ti | -1,628 | Cu++e-=Cu | 0,521 |
Mn2++2e-=Mn | -1,180 | Hg22++2e-=2Hg | 0,788 |
Cr2++2e-=Cr | -0,913 | Ag++e-=Ag | 0,799 |
Zn2++2e-=Zn | -0,763 | Hg2++2e-=Hg | 0,854 |
Уравнение электродного процесса | Стандартный потенциал ( | Уравнение электродного процесса | Стандартный потенциал ( |
Cr3++3e-=Cr | -0,744 | Pt2++2e-=Pt | 1,2 |
Fe2++2e-=Fe | -0,440 | Au3++3e-=Au | 1,498 |
Cd2++2e-=Cd | -0,403 | Au++e-=Au | 1,691 |
Таблица 7. Растворимость кислот, солей, оснований в воде.
Ионы | OH | NO | F | Cl | Br | I | S | SO | SO | CO | SiO | PO | CH |
H | P | P | P | P | P | P | P | P | P | H | P | P | |
NH | P | P | P | P | P | P | P | P | P | P | - | P | P |
Li | P | P | P | P | P | P | P | P | P | P | P | H | P |
K | P | P | P | P | P | P | P | P | P | P | P | P | P |
Na | P | P | P | P | P | P | P | P | P | P | P | P | P |
Ag | - | P | P | H | H | H | H | M | M | H | H | H | P |
Ba | P | P | M | P | P | P | - | M | H | H | H | H | P |
Ca | M | P | H | P | P | P | - | M | M | H | H | H | P |
Ni | H | P | P | P | P | P | H | H | P | - | H | H | P |
Sn | H | P | P | P | P | P | H | - | P | - | - | H | P |
Pb | H | P | M | M | M | H | H | H | H | H | H | H | P |
Cu | H | P | P | P | P | - | H | - | P | - | - | H | P |
Hg | - | P | - | P | M | H | H | - | P | - | - | H | P |
Hg | - | - | M | H | H | H | H | - | M | H | - | H | M |
Fe | H | P | M | P | P | P | H | M | P | H | H | H | P |
Fe | H | P | H | P | P | - | H | - | P | - | - | H | P |
Al | H | P | M | P | P | P | - | - | P | - | - | H | P |
Cr | H | P | M | P | P | P | - | - | P | - | - | H | P |
Mg | M | P | M | P | P | P | - | M | P | H | H | H | P |
Zn2+ | H | P | M | P | P | P | H | M | P | H | H | H | P |
Таблица 8. Степени окисления s- и р - элементов.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 |



