d-Элементы имеют большое количество вакантных орбиталей и поэтому являются хорошими комплексообразователями, соответственно входят в состав комплексных соединений. Например:
![]() – гексацианоферрат (III) калия;
– гексацианоферрат (III) калия;
![]() – тетрагидроксоцинкат (II) натрия;
– тетрагидроксоцинкат (II) натрия;
![]() – хлорид диамминсеребра(I);
– хлорид диамминсеребра(I);
![]() – трихлоротриамминкобальт.
– трихлоротриамминкобальт.
Контрольные вопросы
261. Опишите лабораторные и промышленные способы получения водорода. Какую степень окисления может проявлять водород в своих соединениях? Почему? Приведите примеры реакций, в которых газообразный водород играет роль а) окислителя; б) восстановителя.
262. Какие соединения магния и кальция применяются в качестве вяжущих строительных материалов? Чем обусловлены их вяжущие свойства?
263. Какие соединения называют негашеной и гашеной известью? Составьте уравнения реакций их получения. Какое соединение образуется при прокаливании негашеной извести с углем? Что является окислителем и восстановителем в последней реакции? Составьте электронные и молекулярные уравнения.
264. Напишите химические формулы следующих веществ: каустическая сода, кристаллическая сода, кальцинированная сода, поташ. Объясните, почему водные растворы всех этих веществ можно применять как обезжиривающие средства.
265. Написать уравнение гидролиза пероксида натрия. Как называют раствор пероксида натрия в технике? Сохранит ли раствор свои свойства, если его прокипятить? Почему? Написать соответствующее уравнение реакции в электронном и молекулярном виде.
266. На каких свойствах алюминия основано его применение а) в качестве конструкционного материала; б) для получения газобетона; в) в составе термитов при холодной сварке. Записать уравнения реакций.
267. В чем проявляется агрессивность природной и технической воды по отношению к алюминию и глиноземистому цементу? Составить соответствующие уравнения реакций.
268. Какие соединения называют карбидами? На какие группы их делят? Напишите уравнения реакций взаимодействия карбидов кальция и алюминия с водой, где они находят применение?
269. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
![]()
Что такое агрессивная углекислота?
270. Почему в технике олово растворяют в соляной кислоте, а свинец в азотной? Написать соответствующие уравнения реакций в электронном и в молекулярном виде.
271. Составьте уравнения реакций, которые надо провести для осуществления превращений:
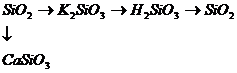
Где применяются данные вещества в технике?
272. Составьте молекулярные и электронные уравнения реакций взаимодействия аммиака и гидразина с кислородом, где применяются эти реакции?
273. Какие свойства проявляет в окислительно-восстановительных реакциях серная кислота? Напишите в молекулярном и электронном виде уравнения следующих взаимодействий: а) разбавленной серной кислоты с магнием; б) концентрированной серной кислоты с медью; в) концентрированной серной кислоты с углем.
274. Для удаления диоксида серы из дымовых газов можно применить следующие методы: а) адсорбцию твердым оксидом магния; б) превращение в сульфат кальция реакцией с карбонатом кальция в присутствии кислорода; в) превращение в свободную серу. Какие химические свойства проявляет диоксид серы в этих реакциях? Напишите соответствующие уравнения. Где можно использовать полученные продукты?
275. Какими особыми свойствами обладает плавиковая кислота? Составьте уравнения реакций, которые надо провести для осуществления превращений:
![]()
Дайте название веществам. Где используются данные превращения?
276. При действии хлора на гашеную известь образуется хлорная известь. Напишите уравнение реакции, укажите окислитель, восстановитель. Дайте химическое название полученному продукту, напишите его структурную формулу. Где используется хлорная известь?
277. Рассмотрите особенности d-элементов на примере марганца и его соединений. Ответ подтвердите уравнениями реакций. Для окислительно- восстановительных реакций составьте электронный баланс, укажите окислитель и восстановитель.
278. Какое основание более сильное ![]() или
или ![]() ? Почему? Какие свойства проявляет
? Почему? Какие свойства проявляет ![]() при сплавлении со щелочными и основными оксидами? Напишите несколько примеров получения таких соединений. Как называются образующиеся продукты?
при сплавлении со щелочными и основными оксидами? Напишите несколько примеров получения таких соединений. Как называются образующиеся продукты?
279. Какие соли железа находят наибольшее практическое применение, где и для чего они используются? Ответ подтвердите уравнениями реакций.
280. Дайте названия веществам, составьте уравнения реакций, которые надо провести для осуществления превращений:
![]()
для окислительно-восстановительных реакций составьте электронные уравнения, укажите окислитель, восстановитель. Какую среду необходимо поддерживать при осаждении гидроксида хрома(III)? Почему?
2.6. Жесткость воды и методы её устранения
Для ответов на контрольные вопросы рекомендуем воспользоваться литературой 5, 6, 7, 9, 11, 14, 15.
Жесткость воды обусловлена присутствием в воде растворимых солей кальция и магния.
Карбонатная жесткость зависит от содержания в воде гидрокарбонатов кальция и магния. Она почти полностью устраняется кипячением, при котором гидрокарбонаты разлагаются:
Поэтому карбонатную жесткость называют также устранимой или временной.
Некарбонатная жесткость вызывается присутствием в воде сульфатов (а также хлоридов) кальция и магния. Кипячением она не устраняется и поэтому называется постоянной.
Сумма карбонатной и некарбонатной жесткости дает общую жесткость воды.
Принято жесткость выражать молярной концентрацией эквивалентов кальция и магния (z = 2) в моль на 1 л воды или (ммоль/л). Практически при этом указывают молярную концентрацию эквивалентов раствора солей, умноженную на 1000.
Зная, что мольные массы эквивалентов кальция и магния (Z=2) равны 20,04 и 12,16 соответственно, можно рассчитать жесткость по солевым концентрациям этих ионов 
![]() и
и ![]()
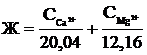 , ммоль/л
, ммоль/л
Так же жесткость можно определить, зная массу соли, обуславливающей жесткость воды или вещества, применяемого для устранения жесткости воды по формуле:
![]() , ммоль/л
, ммоль/л
где ![]() - масса вещества, обуславливающего жесткость воды или применяемого для устранения жесткости воды, мг;
- масса вещества, обуславливающего жесткость воды или применяемого для устранения жесткости воды, мг; ![]() - молярная масса эквивалента вещества;
- молярная масса эквивалента вещества; ![]() - объем воды, л.
- объем воды, л.
Пример 1. Сколько граммов ![]() содержится в 1000 л воды, если жесткость, обусловленная присутствием этой соли, равна 4 ммоль/л?
содержится в 1000 л воды, если жесткость, обусловленная присутствием этой соли, равна 4 ммоль/л?
Решение: Из формулы ![]() выразим массу вещества, обуславливающего жесткость воды:
выразим массу вещества, обуславливающего жесткость воды: ![]() , мольная масса
, мольная масса ![]() 136,14 г/моль, тогда молярная масса эквивалента 136,14 : 2 = 68,07 г/моль, найдем массу сульфата кальция m (
136,14 г/моль, тогда молярная масса эквивалента 136,14 : 2 = 68,07 г/моль, найдем массу сульфата кальция m (![]() ) =4 × 68,07 × 1000 = 272,28 г.
) =4 × 68,07 × 1000 = 272,28 г.
Пример 2. Вычислите карбонатную жесткость воды, зная, что на титрование 100 см3 этой воды, содержащей гидрокарбонат кальция, потребовалось 6,25 см3 раствора ![]() с молярной концентрацией эквивалента 0,08 моль/л.
с молярной концентрацией эквивалента 0,08 моль/л.
Решение: Жесткость воды рассчитывают по формуле 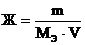 , количество вещества
, количество вещества ![]() можно рассчитать из формулы
можно рассчитать из формулы 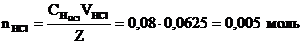 , тогда количество вещества
, тогда количество вещества ![]() в соответствии с реакцией:
в соответствии с реакцией:
будет в два раза меньше, чем у ![]()
![]() = 0,0025 моль, тогда масса : m( ) = M( ) · 0,0025 = 100 · 0,0025 = 0,25 г. Теперь рассчитываем жесткость:
= 0,0025 моль, тогда масса : m( ) = M( ) · 0,0025 = 100 · 0,0025 = 0,25 г. Теперь рассчитываем жесткость: 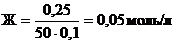 .
.
Контрольные вопросы
281. Присутствие каких солей в природной воде обуславливает её жесткость? Какие химические реакции происходят при добавлении к жесткой воде: а) ; б) |
282. К 500 л жесткой воды прибавили 132,5 г карбоната натрия. Насколько понизилась жесткость? |
283. Сколько граммов необходимо прибавить гидроксида кальция к 100 л воды, чтобы удалить временную жесткость равную 4,29 ммоль/л? |
284. Вычислить временную жесткость воды, зная, что на реакцию с гидрокарбонатом, содержащимся в 100 мл этой воды, потребовалось 5 мл раствора |
285. Чему равна временная жесткость воды, в 1 л которой содержится 0,185 г гидрокарбоната магния? |
286. Жесткость воды содержащей только гидрокарбонат кальция, равна 2,50 ммоль/л. Определить массу гидрокарбоната в 1 л воды. |
287. Какую массу карбоната натрия надо прибавить к 100 л воды, чтобы устранить её жесткость, равную 5,00 ммоль/л? |
288. Сколько карбоната натрия надо добавить к 100 л воды, чтобы устранить общую жесткость, равную 6,90 ммоль/л? |
289. В 1 л воды содержится 24 мг ионов |
290. При кипячении 250 мл воды, содержащей гидрокарбонат кальция, выпал осадок массой 7 мг. Чему равна жесткость воды? |
291. В чем заключается ионообменный способ устранения жесткости воды? Сколько граммов необходимо прибавить |
292. Какие соли обуславливают жесткость природной воды? Какую жесткость называют карбонатной и некарбонатной? Какую массу |
293. Как можно устранить карбонатную, некарбонатную жесткость? Напишите уравнения соответствующих реакций. Чему равна жесткость воды, в 1000 л которой содержится 81 г гидрокарбоната кальция? |
294. В 5 м3 воды воды содержится 120 г сульфата магния и 272 г сульфата кальция. Вычислите жесткость этой воды. |
295. Вода, содержащая только гидрокарбонат кальция, имеет жесткость 4,00 ммоль/л. Какая масса гидрокарбоната кальция содержится в 200 л этой воды? |
296. Какие ионы надо удалить из природной воды, чтобы сделать её мягкой? Введением каких ионов можно умягчить воду? Составьте уравнения соответствующих реакций. Чему равна жесткость воды, в 100 л которой содержится 16,2 г гидрокарбоната кальция? |
297. Вода, содержащая только гидрокарбонат магния, имеет жесткость 5,3 ммоль/л. Какова масса гидрокарбоната магния содержащегося 1 м3 этой воды. |
298. Жесткость воды, в которой растворен только гидрокарбонат магния, равна 2 ммоль/л. Какой объем раствора |
299. В 10 л воды содержится 36 мг ионов магния и 100 мг ионов кальция. Чему равна жесткость этой воды? |
300. Чему равна карбонатная жесткость воды, если в 1 л её содержится 0,146 г гидрокарбоната магния и 0,324 г гидрокарбоната кальция? |
2.7. Органические соединения. Полимеры.
Для ответов на контрольные вопросы рекомендуем воспользоваться литературой 1, 17, 18, 21.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 |



