31. Реакция горения этилового спирта выражается термохимическим уравнением:
![]() ;
; ![]() Н
Н
Вычислить тепловой эффект реакции, если известно, что мольная теплота парообразования ![]() равна ( + 42,36 кДж) и известны теплоты образования:
равна ( + 42,36 кДж) и известны теплоты образования: ![]() ,
, ![]() ,
, ![]() .
.
32. Значения энтальпии растворения в воде 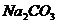 и
и 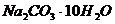 составляют соответственно (-25,10 и + 66,94 кДж). Вычислите энтальпию гидратации
составляют соответственно (-25,10 и + 66,94 кДж). Вычислите энтальпию гидратации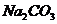 .
.
33. Найдите теплоту сгорания алмаза, если стандартная теплота сгорания графита составляет -393,51 кДж, а теплота фазового перехода 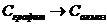 равна + 1,88 кДж.
равна + 1,88 кДж.
34. Вычислите, какое количество теплоты выделится при восстановлении ![]() металлическим алюминием, если было получено 335,1 г железа.
металлическим алюминием, если было получено 335,1 г железа.
35. Теплота растворения ![]() равна +8.66 кДж/моль, а теплота гидратации этой соли при переходе в
равна +8.66 кДж/моль, а теплота гидратации этой соли при переходе в ![]() составляет +29,16 кДж/моль. Какова теплота растворения
составляет +29,16 кДж/моль. Какова теплота растворения ![]() ?
?
36. Вычислите ![]() хлорида аммония, если для реакции
хлорида аммония, если для реакции
![]() = -176,93 кДж/моль.
= -176,93 кДж/моль.
37. При растворении 16 г ![]() в воде выделяется 31,3 кДж теплоты. Определите стандартную теплоту образования
в воде выделяется 31,3 кДж теплоты. Определите стандартную теплоту образования ![]() .
.
38. Какое количество теплоты выделяется при превращении 1 кг красного фосфора в черный, если ![]() = -18,41 кДж/моль;
= -18,41 кДж/моль;
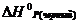 = -43,20 кДж/моль?
= -43,20 кДж/моль?
39. При сгорании 9,3 г фосфора выделяется 229,5 кДж теплоты. Рассчитайте ![]() оксида фосфора (V).
оксида фосфора (V).
40. Сколько теплоты выделится при разложении 54 г глюкозы по реакции: 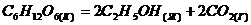 ,
,
если![]()
 = -1273,0 кДж/моль;
= -1273,0 кДж/моль; 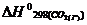 = -393,5 кДж/моль.
= -393,5 кДж/моль.
1.3. Химическое сродство
Для решения задач этого раздела рекомендуем воспользоваться литературой 6, 8, 10, 16 и таблицами 2, 3.
Первый закон термодинамики не позволяет определить, в каком направлении процесс может протекать самопроизвольно.
Критерием самопроизвольного протекания реакции в изолированной системе служит функция состояния S, названная Р. Клаузиусом энтропией. Самопроизвольные процессы могут идти только с увеличением энтропии и будут идти до тех пор, пока система не перейдет в равновесное состояние и энтропия не достигнет максимального для данных условий значения. На основе постулата Планка рассчитано абсолютное значение энтропии многих простых веществ, химических соединений и приведено в справочной литературе (при стандартных условиях). С помощью справочных данных можно рассчитать изменение энтропии, происходящее при химической реакции по следствию из закона Гесса:
![]() ;
;
где ![]() – стандартная энтропия вещества, n – cтехиометрические коэффициенты в уравнении реакции.
– стандартная энтропия вещества, n – cтехиометрические коэффициенты в уравнении реакции.
Пример 1. Определите возможность протекания реакции:
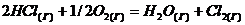 в изолированной системе.
в изолированной системе.
Решение: Используя значения стандартных энтропий веществ (табл. 2) рассчитаем стандартную энтропию реакции:
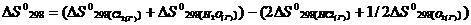
![]() = 223,0 + 188,74 – (2 · 186,7 + 0,5 · 205,03) = - 64,175Дж
= 223,0 + 188,74 – (2 · 186,7 + 0,5 · 205,03) = - 64,175Дж
В результате реакции энтропия уменьшилась и, следовательно, процесс в изолированной системе самопроизвольно протекать не может.
В природе и технике большинство химических процессов протекают в неизолированных системах, то есть в условиях теплообмена с окружающей средой. В этих системах критерием направленности процесса служит изменение термодинамических потенциалов G, F.
G – энергия Гиббса для условий p = соnst и Т = const;
F – энергия Гельмгольца для условий V = const и Т = const.
Изменение энергии Гиббса (![]() G) характеризует максимально полезную работу процесса и указывает на возможное самопроизвольное его протекание. Самопроизвольным является всякий процесс, в результате которого, энергия системы уменьшается (
G) характеризует максимально полезную работу процесса и указывает на возможное самопроизвольное его протекание. Самопроизвольным является всякий процесс, в результате которого, энергия системы уменьшается (![]() G < 0). Когда система достигает положения равновесия, G принимает минимальное значение, а
G < 0). Когда система достигает положения равновесия, G принимает минимальное значение, а ![]() G становится равным нулю. Изменение энергии Гиббса включает в себя как энтальпийный (
G становится равным нулю. Изменение энергии Гиббса включает в себя как энтальпийный (![]() ), так и энтропийный (
), так и энтропийный (![]() ) факторы. Для расчета используется соотношение:
) факторы. Для расчета используется соотношение:
![]() ;
; ![]()
Термодинамические потенциалы G и F можно также рассчитать с помощью следствия из закона Гесса с использованием стандартных величин 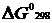 и
и ![]() (табл. 2).
(табл. 2).
![]()
Пример 2. Определите возможность протекания реакции:
![]()
в системе при стандартных условиях и при температуре 1000 К. Установить температуру, при которой система будет находиться в равновесии.
Решение: 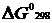 =
= 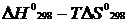
Воспользуемся результатами решения предыдущих примеров:
![]() -57240 - 298 · (-64,175) = -38115Дж
-57240 - 298 · (-64,175) = -38115Дж
Для приближенных расчетов ![]() можно принять:
можно принять:
![]()
![]() = -57240 – 1000 · (-64,175) = 6935 Дж
= -57240 – 1000 · (-64,175) = 6935 Дж
При равновесии:
![]() G = 0 ;
G = 0 ; 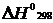 = - 57240 Дж;
= - 57240 Дж; ![]() = -64,175 Дж
= -64,175 Дж
T = ![]() =
=![]()
Таким образом, при стандартных условиях реакция возможна, так как ![]() G < 0; при температуре 1000 К реакция самопроизвольно протекать не может
G < 0; при температуре 1000 К реакция самопроизвольно протекать не может ![]() G > 0; реакция протекает при Т = 892 К.
G > 0; реакция протекает при Т = 892 К.
Контрольные вопросы
41. Вычислите изменение энтропии в результате реакции образования аммиака из азота и водорода. При расчете можно исходить из 42. Определите
Вычисления сделайте на основании стандартных теплот образования и стандартных энтропий соответствующих веществ. Возможна ли эта реакция при стандартных условиях. | |
43. Эндотермическая реакция взаимодействия метана с диоксидом углерода протекает по уравнению:
При какой температуре начнется реакция? |
|
44. Вычислите стандартные значения
и определите, какой из карбонатов обладает большей термической устойчивостью? |
|
45. Вычислите возможность протекания при стандартных условиях реакции:
|
|
46. Вычислите изменение энергии Гиббса при
|
|
47. В каком направлении нижеприведенная реакция будет протекать самопроизвольно:
Необходимые для расчета |
|
48. Определите, при какой температуре начнется реакция восстановления: |
|
49. Образование сероводорода из простых веществ протекает по уравнению
Исходя из значений
|
|
50. Вычислите возможность протекания при стандартных условиях реакции:
|
|
51. Вычислите изменение энергии Гиббса при
зная |
|
52. Вычислите значения
и составьте ряд термической стабильности карбонатов |
|
53. Какие из приведенных реакций протекают самопроизвольно и являются экзотермическими:
|
|
54. Укажите, какая из двух реакций будет протекать самопроизвольно:
|
|
55. В каком направлении ниже приведенная реакция будет протекать самопроизвольно:
Рассчитать с использованием |
|
56. На основании значений
Укажите, в каком направлении эти реакции будут протекать, приближаясь к равновесию. |
|
57. Определить стандартное изменение энтропии при
Сделать вывод о возможности самопроизвольного протекания реакций. |
|
58. Для каких оксидов |
|
59. Пользуясь значениями
Сделать вывод о возможности самопроизвольного протекания реакции. |
|
60. Реакция горения ацетилена протекает по уравнению:
Вычислите |
|
1.4. Химическая кинетика
Для решения задач этого раздела рекомендуем воспользоваться литературой 6, 7, 9.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 |



