91. Равновесие гомогенной системы при Т=const
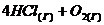 ⇄
⇄ 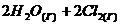 установилось при следующих концентрациях:
установилось при следующих концентрациях:![]()
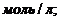
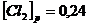
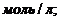
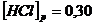
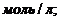
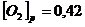
 Вычислите исходные концентрации хлороводорода и кислорода.
Вычислите исходные концентрации хлороводорода и кислорода.
92. Напишите выражение для константы равновесия гетерогенной системы ![]() ⇄
⇄ ![]() . Как следует изменить давление и концентрацию веществ, чтобы сместить равновесие в сторону прямой реакции?
. Как следует изменить давление и концентрацию веществ, чтобы сместить равновесие в сторону прямой реакции?
93. Напишите выражение для константы равновесия гетерогенной системы ![]() ⇄
⇄ ![]() . Что необходимо предпринять для повышения выхода оксида углерода? Как изменится скорость прямой реакции, если концентрацию диоксида углерода увеличить в 3 раза?
. Что необходимо предпринять для повышения выхода оксида углерода? Как изменится скорость прямой реакции, если концентрацию диоксида углерода увеличить в 3 раза?
94. Составьте выражение для константы равновесия реакции, протекающей в закрытой системе при постоянной температуре:
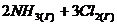 ⇄
⇄ ![]() . Укажите, во сколько раз изменится значение константы равновесия, если: а) концентрацию хлора увеличить в 2 раза; б) концентрацию хлороводорода увеличить в 6 раз.
. Укажите, во сколько раз изменится значение константы равновесия, если: а) концентрацию хлора увеличить в 2 раза; б) концентрацию хлороводорода увеличить в 6 раз.
95. Установите, во сколько раз уменьшится или увеличится равновесная концентрация оксида углерода в реакции: ![]() ⇄
⇄ ![]() при увеличении значения равновесной концентрации диоксида углерода в 3 раза.
при увеличении значения равновесной концентрации диоксида углерода в 3 раза.
96. Как увеличить выход продуктов реакций
![]() ⇄
⇄![]() ,
, 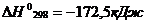
![]() ⇄
⇄ 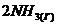 ,
, ![]()
за счет изменения концентрации реагентов, давления, температуры?
97. Вычислите константу равновесия для следующей реакции 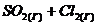 ⇄
⇄ 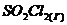 , если при некоторой температуре образовалось 2,3 моль
, если при некоторой температуре образовалось 2,3 моль ![]() , а исходные концентрации двуокиси серы и хлора соответственно составляли 6,2 моль/л и 5,5 моль/л.
, а исходные концентрации двуокиси серы и хлора соответственно составляли 6,2 моль/л и 5,5 моль/л.
98. Вычислите константу равновесия реакции ![]() ⇄
⇄ 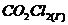 , если исходные концентрации оксида углерода и хлора составляли соответственно 6 и 8 моль/л, а равновесие установилось, когда образовалось 3 моль
, если исходные концентрации оксида углерода и хлора составляли соответственно 6 и 8 моль/л, а равновесие установилось, когда образовалось 3 моль ![]() .
.
99. Константа равновесия системы ![]() ⇄ равна 0,35. Определите равновесные концентрации
⇄ равна 0,35. Определите равновесные концентрации ![]() и
и ![]() , если исходная концентрация йодоводорода равна 2 моль/л.
, если исходная концентрация йодоводорода равна 2 моль/л.
100. Вычислите равновесные концентрации веществ в реакции ![]() ⇄
⇄ 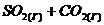 , если константа равновесия реакции равна 1,89, а исходная концентрация
, если константа равновесия реакции равна 1,89, а исходная концентрация ![]()
![]()
1.6.Способы выражения концентрации раствора
Для решения задач этого раздела рекомендуем воспользоваться литературой 6, 8, 10, 16
Молекулярные или истинные растворы состоят из перемешанных друг с другом молекул растворенного вещества и среды. Растворы образуются при самопроизвольном распределении одного вещества в другом в результате диффузии. Но рассматривать раствор как смесь молекул различных веществ нельзя, так как свойства растворенного вещества и растворителя в общей системе раствора изменяются. Например, объем раствора никогда не равен сумме объемов растворителя и растворенного вещества. Полученная система однородна, так как за счет диффузии концентрация во всех микрообъемах выравнивается.
Раствором называется термодинамически устойчивая однофазная конденсированная система переменного состава, состоящая из двух или более компонентов, связанных между собой силами физического и химического взаимодействия.
Основным признаком, характеризующим раствор, является его гомогенность (однородность). Раствор может состоять только из одной фазы: жидкой или твердой.
Количественный состав раствора определяется концентрацией, т. е. относительным содержанием каждого из компонентов, составляющих раствор.
Концентрацией называется содержание растворенного вещества в единице массы или объема раствора или растворителя.
Существуют различные способы численного выражения состава растворов: массовые, объемные и безразмерные.
Массовые концентрации.
Массовая доля ![]() растворенного вещества – это отношение массы компонента, содержащегося в массе раствора.
растворенного вещества – это отношение массы компонента, содержащегося в массе раствора.
![]() или
или ![]() ,
,
где ![]() - массовая доля;
- массовая доля;
![]() - масса растворенного вещества, г;
- масса растворенного вещества, г;
![]() - масса раствора, г;
- масса раствора, г;
![]() - объем раствора, мл;
- объем раствора, мл;
![]() - плотность раствора, г/мл.
- плотность раствора, г/мл.
Пример 1. Кристаллогидрат нитрата железа (III) 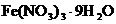 массой 60,6 г растворили в воде массой 250 г. Определите массовую долю нитрата железа (III) в полученном растворе.
массой 60,6 г растворили в воде массой 250 г. Определите массовую долю нитрата железа (III) в полученном растворе.
Решение: Масса полученного раствора составляет
![]() ;
;
![]() = 60,6+250= 310,6 г
= 60,6+250= 310,6 г
определяем количество вещества кристаллогидрата, растворенного в воде:
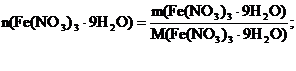
![]() 60,6/404=0,15 моль.
60,6/404=0,15 моль.
Из формулы кристаллогидрата следует:
![]()
![]() 0,15 моль.
0,15 моль.
Находим массу нитрата железа (III), которая содержится в растворе:
![]()
![]() = 0,15 . 242=36,3 г.
= 0,15 . 242=36,3 г.
Рассчитываем массовую долю нитрата железа (III) в растворе:
![]()
![]() 36,3/310,6 = 0,117 или 11,7%.
36,3/310,6 = 0,117 или 11,7%.
Моляльность (![]() ) – число молей растворенного вещества в 1 кг растворителя.
) – число молей растворенного вещества в 1 кг растворителя.
![]() , моль/кг,
, моль/кг,
где ![]() - число молей растворенного вещества;
- число молей растворенного вещества;
![]() - масса растворителя, кг.
- масса растворителя, кг.
Пример 2. Раствор содержит 10 г ![]() и 100 г воды. Вычислить моляльную концентрацию раствора.
и 100 г воды. Вычислить моляльную концентрацию раствора.
Решение: Определим число молей растворенного вещества:
![]() ;
; 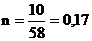 моль,
моль,
где ![]() - молярная масса
- молярная масса ![]() равная 58 г/моль
равная 58 г/моль
Моляльность раствора рассчитаем по формуле: ![]()
![]()
Объемные концентрации.
Молярная концентрация ![]() - число молей растворенного вещества в 1 л раствора.
- число молей растворенного вещества в 1 л раствора.
![]() , моль/л
, моль/л

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 |



