17. При пропускании сероводорода через раствор, содержащий 2,98 г хлорида некоторого одновалентного металла, образуется 2,2 г его сульфида. Вычислите молярную массу эквивалентов металла.
18. При сгорании трехвалентного металла массой 11,2 г образовался оксид массой 16 г. Какой был взят металл?
19. Сколько литров ![]() (при н. у.) надо пропустить через раствор
(при н. у.) надо пропустить через раствор 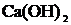 , чтобы получить: а) 7 молей эквивалентов карбоната кальция; б) 7 молей карбоната кальция;
, чтобы получить: а) 7 молей эквивалентов карбоната кальция; б) 7 молей карбоната кальция;
в) 100 г карбоната кальция?
20. Сколько молей эквивалентов оксида цинка получится при взаимодействии цинка с кислородом объемом 5,6 л (н. у.).
1.2. Энергетика химических процессов (термохимические расчеты)
Для решения задач этого раздела рекомендуем воспользоваться литературой 6, 8, 10, 16 и таблицей 1.
Предметом химической термодинамики является применение законов классической термодинамики к физико-химическим явлениям. Она рассматривает тепловые эффекты химических реакций, фазовые переходы и химические равновесия. Термодинамический метод помогает, не прибегая к опыту, решать вопрос о возможности протекания реакции, ее направлении, пределе протекания, выборе оптимального режима.
Раздел химической термодинамики, изучающий тепловые эффекты химических реакций, называют термохимией. Под тепловым эффектом химической реакции понимают количество теплоты, которое выделяется или поглощается в необратимом процессе при постоянном объеме или давлении и при условии равенства температур исходных веществ и продуктов реакции в расчете на 1 моль продукта реакции.
Теплота при р = соnst и Т = const приобретает свойство функции состояния, не зависит от пути, по которому протекает процесс. Теплоту реакции в изобарно-изотермическом процессе принято называть энтальпией системы, а ее изменение ![]() .
.
Термохимические расчеты основаны на законе Гесса (1840 г.): тепловой эффект реакции зависит только от природы и физического состояния исходных веществ и конечных продуктов, но не зависит от пути перехода (промежуточных стадий реакции). Часто в термохимических расчетах применяют следствие из закона Гесса: тепловой эффект реакции (стандартная энтальпия ![]() Н0), равен сумме стандартных энтальпий образования продуктов реакции за вычетом суммы стандартных энтальпий образования исходных веществ с учетом их стехиометрических коэффициентов. Под стандартной энтальпией образования вещества
Н0), равен сумме стандартных энтальпий образования продуктов реакции за вычетом суммы стандартных энтальпий образования исходных веществ с учетом их стехиометрических коэффициентов. Под стандартной энтальпией образования вещества ![]() понимают энтальпию образования одного моля вещества при стандартных условиях (Т = 298 К,
понимают энтальпию образования одного моля вещества при стандартных условиях (Т = 298 К, ![]() ) из простых веществ (табл.1) :
) из простых веществ (табл.1) :
![]() , где
, где
n-стехиометрические коэффициенты в уравнении реакции.
Кроме того, тепловой эффект реакции можно рассчитать, используя теплоты сгорания исходных веществ и продуктов реакции:
![]()
![]()
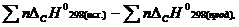
где ![]() - стандартная энтальпия сгорания вещества, равная энтальпии сгорания одного моля вещества при стандартных условиях до
- стандартная энтальпия сгорания вещества, равная энтальпии сгорания одного моля вещества при стандартных условиях до ![]() и
и ![]() .
.
Этим способом чаще пользуются при расчетах тепловых эффектов органических реакций.
Пример 1. Реакция выражается термохимическим уравнением:
![]() +
+ ![]() =
= 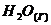 +
+ ![]() ;
; ![]() Н =?
Н =?
Рассчитайте тепловой эффект реакции при стандартных условиях. Сколько теплоты выделится при образовании 44, 8 л Cl2?
Решение: В таблице 1 находим теплоты образования всех участников реакции. Обратим внимание на то, что теплоты образования для простых веществ и элементов в стандартном состоянии приняты равными нулю. Рассчитываем по следствию из закона Гесса:
![]()
![]() = -241,84 – 2 · (-92,30) = -57,24 кДж
= -241,84 – 2 · (-92,30) = -57,24 кДж
Исходя из определения теплового эффекта реакции при образовании 1 моля ![]() выделяется 57,24 кДж теплоты. Рассчитаем – сколько молей составляют 44,8 л
выделяется 57,24 кДж теплоты. Рассчитаем – сколько молей составляют 44,8 л ![]() . Так как, 1 моль любого газа при нормальных условиях занимает объем, равный 22,4 л, то 44,8 л составят 2 моля. Таким образом, при образовании двух молей
. Так как, 1 моль любого газа при нормальных условиях занимает объем, равный 22,4 л, то 44,8 л составят 2 моля. Таким образом, при образовании двух молей ![]() выделится 57,2 · 2 = 11,48 кДж теплоты.
выделится 57,2 · 2 = 11,48 кДж теплоты.
Пример 2. Теплота растворения безводного ![]() равна (- 47,70 кДж), а теплота растворения кристаллогидрата
равна (- 47,70 кДж), а теплота растворения кристаллогидрата ![]() равна (+ 30,96 кДж). Вычислите теплоту гидратации
равна (+ 30,96 кДж). Вычислите теплоту гидратации ![]() .
.
Решение: Процесс растворения ![]() протекает через посредство двух промежуточных стадий в соответствии с химической теорией растворов :
протекает через посредство двух промежуточных стадий в соответствии с химической теорией растворов :
![]() + aq =
+ aq =![]() · aq;
· aq; ![]() Н, реакция растворения
Н, реакция растворения
1.![]() , реакция гидратации
, реакция гидратации
2. ![]() , реакция растворения кристаллогидрата
, реакция растворения кристаллогидрата
По закону Гесса: ![]() Н =
Н = ![]() ,
,
т. о. 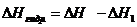 = - 47,70 - 30,96 = -78,66 кДж.
= - 47,70 - 30,96 = -78,66 кДж.
Контрольные вопросы
21. Вычислите тепловой эффект и напишите термохимическое уравнение реакции горения 1 моля метана, в результате которой образуются пары воды и диоксид углерода.
22. Вычислите тепловой эффект реакции восстановления одного моля ![]() металлическим алюминием.
металлическим алюминием.
23. При взаимодействии трех молей оксида азота ![]() с аммиаком образуются азот и пары воды. Тепловой эффект реакции равен (+877,76 кДж) Напишите термохимическое уравнение этой реакции и вычислите теплоту образования
с аммиаком образуются азот и пары воды. Тепловой эффект реакции равен (+877,76 кДж) Напишите термохимическое уравнение этой реакции и вычислите теплоту образования ![]() .
.
24. При сгорании газообразного аммиака образуются пары воды и монооксид азота ![]() . Напишите термохимическое уравнение этой реакции, вычислив ее тепловой эффект в расчете на один моль
. Напишите термохимическое уравнение этой реакции, вычислив ее тепловой эффект в расчете на один моль ![]() .
.
25. Напишите термохимическое уравнение горения 1 моля этилового спирта, в результате которой образуются пары воды и диоксид углерода. Вычислите теплоту образования ![]() , если известно, что при сгорании 11,5 г его выделилось 308,71 кДж теплоты.
, если известно, что при сгорании 11,5 г его выделилось 308,71 кДж теплоты.
26. Газообразный этиловый спирт можно получить при взаимодействии этилена ![]() и водяных паров. Напишите термохимическое уравнение этой реакции, вычислите ее тепловой эффект. Сколько теплоты выделится, если в реакцию вступило 10 л
и водяных паров. Напишите термохимическое уравнение этой реакции, вычислите ее тепловой эффект. Сколько теплоты выделится, если в реакцию вступило 10 л ![]() при нормальных условиях?
при нормальных условиях?
27. Напишите термохимическое уравнение реакции горения одного моля этана ![]() , в результате которой образуются пары воды и диоксид углерода. Сколько теплоты выделится при сгорании 1 м3 этана в пересчете на нормальные условия?
, в результате которой образуются пары воды и диоксид углерода. Сколько теплоты выделится при сгорании 1 м3 этана в пересчете на нормальные условия?
28. Теплота растворения безводного хлорида стронция ![]() равна ( - 47,70 кДж), а теплота растворения кристаллогидрата
равна ( - 47,70 кДж), а теплота растворения кристаллогидрата ![]() равна (+30,96 кДж). Вычислите теплоту гидратации
равна (+30,96 кДж). Вычислите теплоту гидратации ![]() .
.
29. Теплоты растворения сульфата меди ![]() и кристаллогидрата
и кристаллогидрата ![]() соответственно равны ( - 66,11 кДж) и ( + 11,72 кДж). Вычислите теплоту гидратации
соответственно равны ( - 66,11 кДж) и ( + 11,72 кДж). Вычислите теплоту гидратации ![]() .
.
30. Реакция горения этана выражается термохимическим уравнением:
![]()
![]() Н = -1559,87 кДж
Н = -1559,87 кДж
Вычислить теплоту образования этана, если известны теплоты образования ![]() и
и ![]() .
.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 |



