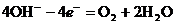
В кислой и нейтральной средах вода окисляется по уравнению:
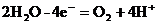
2. при электролизе водных растворов бескислородных кислот и их солей (кроме фтороводорода и фторидов) происходит окисление анионов.
Если анод металлический, происходит: электрохимическое окисление воды, окисление аниона, окисление металла анода. При этом если значение стандартного потенциала металла анода меньше, чем у предыдущих двух систем, то будет происходить анодное растворение металла.
Пример 1. Написать уравнения процессов, происходящих при электролизе водного раствора нитрата калия с инертным анодом.
Решение: Стандартный электродный потенциал системы 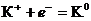
(Е0 = - 2,925 В) значительно отрицательнее потенциала водородного электрода в нейтральной водной среде (- 0,41 В). Поэтому на катоде будет происходить электрохимическое восстановление воды по уравнению:
![]()
а ионы К+, приходящие к катоду, будут накапливаться в прилегающей к нему части раствора.
На аноде будет происходить электрохимическое окисление воды по уравнению:
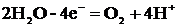
а нитрат-ионы будут накапливаться в анодном пространстве.
Умножая уравнение катодного процесса на два и складывая его с уравнением анодного процесса, получаем суммарное уравнение процесса электролиза:
![]()
Учитывая, что одновременно происходит накопление ионов К+ в катодном пространстве и ионов ![]() в анодном пространстве, суммарное уравнение процесса можно записать в следующей форме:
в анодном пространстве, суммарное уравнение процесса можно записать в следующей форме:
![]()
Т. о., одновременно с выделением водорода и кислорода образуется гидроксид калия (в катодном пространстве) и азотная кислота (в анодном пространстве).
Количественной характеристикой электролиза являются законы Фарадея:
1. Массы разрядившихся или образовавшихся на электродах ионов, т. е. массы выделившихся или перешедших в электролит веществ, пропорциональны количеству электричества, прошедшего через раствор или расплав электролита, и не зависят от других условий.
2. При прохождении через различные электролиты одинаковых количеств электричества на электродах выделяются массы веществ, пропорциональные их химическим эквивалентам.
![]() (1)
(1)
где m – масса вещества, окисленного или восстановленного на электроде; Мэ– молярная масса эквивалента; I – сила тока, А; t – продолжительность электролиза, сек.; F – постоянная Фарадея, численно равна 96500 Кл/моль.
Пример 2. Какая масса меди выделится на катоде при электролизе раствора CuSO4 в течение 1 ч при силе тока 4 А?
Решение: Согласно законам Фарадея ![]()
Молярная масса эквивалентов меди в CuSO4 равна 63,54/2 = 31,77 г/моль. Подставив в формулу (1) значения
Мэ = 31,77 г/моль,
I = 4 А,
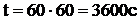 ,
,
получим
![]()
![]() .
.![]()
Пример 3. Вычислите молярную массу эквивалента металла, зная, что при электролизе раствора хлорида этого металла затрачено 3880 Кл электричества и на катоде выделяется 11,742 г металла.
Решение: Из формулы (1)
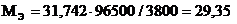
![]()
где m = 11,742 г;
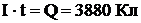
Пример 4. Чему равна сила тока при электролизе раствора в течение 1 ч 40 мин 25 с, если на катоде выделилось 1,4 л водорода (нормальные условия)?
Решение: Из формулы (1)
![]()
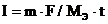
Так как дан объём водорода, то отношение m / Мэ заменяем отношением ![]() , где
, где ![]() - объём водорода, л;
- объём водорода, л; ![]() - эквивалентный объём водорода, л. Тогда
- эквивалентный объём водорода, л. Тогда
![]()
Эквивалентный объём водорода при нормальных условиях равен половине молярного объёма 22,4/2 = 11,2 л. Подставив в приведённую формулу значения ![]() = 1,4 л,
= 1,4 л, ![]() = 11,2 л, t = 6025 с (1 ч 40 мин 25 с = 6025 с), находим
= 11,2 л, t = 6025 с (1 ч 40 мин 25 с = 6025 с), находим
![]()
![]()
Контрольные вопросы:
241. При электролизе водного раствора сульфата калия значение, рН раствора в при электродном пространстве возросло. К какому полюсу источника тока присоединён электрод: а) к аноду; б) к катоду? Ответ подтвердите расчетами.
242. При электролизе раствора хлорида меди (II) масса катода увеличилась на 3,2 г, что произошло при этом на медном аноде: а) выделилось 0,112 л Cl2; б) выделилось 0,56 л О2; в) перешло в раствор 0,1 моля Cu2+; г) перешло в раствор 0,05 моля Cu2+? Ответ подтвердите расчетами.
243. При электролизе водного раствора SnCl2 на аноде выделилось 4,48 л хлора (условия нормальные). Составьте электронные уравнения процессов, происходящих на электродах. Найти массу выделившегося на катоде олова.
244. В какой последовательности будут выделяться металлы при электролизе раствора, содержащего в одинаковой концентрации сульфаты никеля, серебра, меди? Ответ подтвердить расчетами.
245. Какая масса серебра выделилась при пропускании тока силой 6 А через раствор нитрата серебра в течение 30 мин?
246. При прохождении через раствор соли трехвалентного металла тока силой 1,5 А в течение 30 мин на катоде выделилось 1,071 г металла. Определить атомную массу металла.
247. Составьте электронные уравнения процессов, происходящих на графитовых электродах при электролизе водного раствора КОН. Какой объем кислорода выделится (нормальные условия) при пропускании тока силой 6А в течение 30 мин через раствор?
248. Чему равна молярная масса эквивалента кадмия, если для выделения 1г кадмия из раствора его соли надо пропустить через раствор 1717 Кл электричества?
249. При электролизе водного раствора Cr2(SO4)3 током силой 2А масса катода увеличилась на 8г. В течение, какого времени проводили электролиз? Составить электронные уравнения процессов, происходящих на электродах.
250. Электролиз раствора сульфата некоторого металла проводили при силе тока 6А в течение 45 мин, в результате чего на катоде выделилось 5,49 г металла. Вычислите молярную массу эквивалента металла.
251. За 10 мин из раствора платиновой соли ток силой 5А выделил 1,517 г Pt. Определить молярную массу эквивалента платины.
252. Через водный раствор H2SO4 пропускали ток силой в 3А в течение 1 часа. Составить электронные уравнения процессов, происходящих на электродах. Какой объём водорода (условия нормальные) при этом выделится?
253. Какое количество электричества потребуется для выделения из раствора: а) 2 г водорода; б) 2 г кислорода?
254. Как электролитически получить LiOH из соли лития? Какое количество электричества необходимо для получения 1 т LiOH? Составить схемы электродных процессов.
255. Составьте электронные уравнения процессов, происходящих на электродах при электролизе воды. Сколько потребуется времени для полного разложения 2 молей воды током силой 2 А?
256. Электролиз раствора нитрата серебра проводили при силе тока 2А в течение 4 ч. Составьте электронные уравнения процессов, происходящих на электродах. Какая масса серебра выделилась на катоде, и каков объём газа (нормальные условия), выделившегося на аноде?
257. При электролизе раствора хлорида двухвалентного металла на аноде выделилось 560 мл газа (условия нормальные), а на катоде за это же время – 1,6 г металла. Какой это металл? Ответ подтвердите расчетами.
258. Ток силой 5 А пропускали через водный раствор серной кислоты в течение 1,5 ч. Вычислите массу разложившейся воды и объём выделившихся водорода и кислорода (условия нормальные).
259. Ток силой 2,7 А, проходя через раствор электролита, за 30 мин выделяет из раствора 2,94 г металла. Найти молярную массу эквивалента металла.
260. При электролизе водного раствора NaOH на аноде выделилось 2,8 л кислорода (условия нормальные). Составить электронные уравнения процессов, происходящих на электродах. Сколько водорода выделилось на катоде?
2.5. Свойства соединений s-, p-, d – элементов
Для ответов на контрольные вопросы рекомендуем воспользоваться литературой 6, 9, 12 и таблицами 8 – 11.
s-, р-Элементы расположены в главных подгруппах периодической системы (подгруппа А). Каждый период начинается двумя s - элементами, а шесть последних (кроме первого периода) – это р - элементы. У s - и р - элементов валентными являются электроны и орбитали внешнего слоя атома. Число внешних электронов равно номеру группы (кроме ![]() и
и ![]() ). При участии в образовании связей всех валентных электронов элемент проявляет высшую степень окисления, которая численно равна номеру группы. Энергетически более стабильны соединения, в которых элементы нечетных групп проявляют нечетные степени окисления, а элементы четных групп – четные степени окисления (табл. 8).
). При участии в образовании связей всех валентных электронов элемент проявляет высшую степень окисления, которая численно равна номеру группы. Энергетически более стабильны соединения, в которых элементы нечетных групп проявляют нечетные степени окисления, а элементы четных групп – четные степени окисления (табл. 8).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 |



