Поскольку цепь замкнута, избыточные электроны будут перетекать на медную пластину и т. д. До тех пор, пока цепь будет замкнута, цинковая пластина будет растворяться, на медной будет осаждаться металлическая медь. Равновесие на электродах не установится, в цепи будет протекать ток. Просуммируем процессы, протекающие на электродах в замкнутом гальваническом элементе:
![]()
или 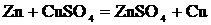
Суммарная электрохимическая реакция называется токообразующей. Рассмотренный гальванический элемент называется элементом Даниэля - Якоби. В прошлом веке он широко использовался в качестве источника постоянного тока. Сокращенное обозначение элемента Даниэля-Якоби: А (-) 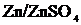 //
//![]() (+) К
(+) К
Подобным образом обозначают любые гальванические элементы. При этом следует помнить, что слева принято указывать электрод с более отрицательным потенциалом.
Гальванический элемент – это система, в которой происходит самопроизвольная окислительно-восстановительная реакция ( < 0), энергия которой превращается в электрическую энергию.
Гальванический элемент является химическим источником электрического тока.
Основной характеристикой гальванического элемента является его электродвижущая сила (ЭДС) или ![]() , которая представляет собой разность электродных потенциалов в исходный момент работы элемента. ЭДС всегда является величиной положительной.
, которая представляет собой разность электродных потенциалов в исходный момент работы элемента. ЭДС всегда является величиной положительной.
Чтобы рассчитать величину ЭДС, необходимо вычесть из более положительного электродного потенциала величину более отрицательного потенциала. В нашем примере при концентрации ионов цинка и меди в растворах равных 1 моль/л:
![]()
Гальванический элемент может быть составлен не только из электродов, состоящих из разных металлов, но и из электродов одного металла, погруженных в растворы одного и того же электролита, но с различной концентрацией ионов. Такой гальванический элемент называется концентрационным. Поскольку ЭДС обусловлена только разностью концентраций ионов металла в растворах.
Составим гальванический элемент из двух серебряных пластинок, погруженных в растворы нитрата серебра разных концентраций ![]() и
и ![]() .
.
А (-)![]() /
/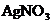 //
//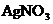 /
/![]() (+) К
(+) К
![]() <
< ![]()
ЭДС такого элемента может быть определена по формуле:
![]()
При работе этого элемента протекают следующие процессы:
А (-)![]() окисление
окисление
К (+)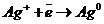 восстановление
восстановление
Таким образом, концентрация первого раствора ![]() будет постепенно увеличиваться, а второго раствора
будет постепенно увеличиваться, а второго раствора ![]() уменьшаться, следовательно ЭДС будет уменьшаться. Через некоторое время концентрации
уменьшаться, следовательно ЭДС будет уменьшаться. Через некоторое время концентрации ![]() и
и ![]() станут одинаковыми, а ЭДС - равной нулю.
станут одинаковыми, а ЭДС - равной нулю.
Пример 1. Стандартный электродный потенциал никеля больше, чем кобальта (табл. 6). Изменится ли это соотношение, если измерить потенциал никеля в растворе его ионов с концентрацией 0,1 моль/л?
Решение: Электродный потенциал металла (Е) зависит от концентрации в растворе. Эта зависимость выражается уравнением Нернста:
где ![]() - стандартный электродный потенциал; n – число электронов, принимающих участие в процессе; С – концентрация (при точных вычислениях – активность) гидратированных ионов металла в растворе, моль/n;
- стандартный электродный потенциал; n – число электронов, принимающих участие в процессе; С – концентрация (при точных вычислениях – активность) гидратированных ионов металла в растворе, моль/n; ![]() для никеля и кобальта соответственно равны - 0,25 и - 0,277 В. Определим электродные потенциалы этих металлов при данных в условии концентрациях:
для никеля и кобальта соответственно равны - 0,25 и - 0,277 В. Определим электродные потенциалы этих металлов при данных в условии концентрациях: ![]()
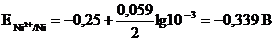
![]()
Таким образом, при изменившейся концентрации потенциал кобальта стал больше потенциала никеля.
Пример 2. Магниевую пластинку опустили в раствор его соли. При этом электродный потенциал магния оказался равен -2,41 В. Вычислите концентрацию ионов магния (в моль/л).
Решение: Подобные задачи так же решаются на основании уравнения Нернста (см. пример 1):
![]()
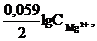
![]()
![]()
![]()
Пример 3. Составьте схему гальванического элемента, в котором электродами являются магниевая и цинковая пластинки, опущенные в растворы их ионов с активной концентрацией 1 моль/л. Какой металл является анодом, какой катодом? Напишите уравнение Окислительно-восстановительной реакции, протекающий в этом гальваническом элементе, и вычислите его ЭДС.
Решение: Схема данного гальванического элемента
(-)![]() //
//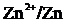 (+)
(+)
Наклонная линия обозначает поверхность между металлом и раствором, а две наклонные линии – границу раздела двух жидких фаз – пористую перегородку (или соединительную трубку, заполненную раствором электролита). Магний имеет меньший потенциал (-2,37 B) и является анодом, на котором протекает окислительный процесс:
![]()
Цинк, потенциал которого (– 0,763 В) - катод, т. е. электрод, на котором протекает восстановительный процесс:
![]()
Для определения ЭДС гальванического элемента из потенциала катода следует вычесть потенциал анода. Так как концентрация ионов в растворе равна 1 моль/л, то ЭДС элемента равна разности стандартных потенциалов двух его электродов:
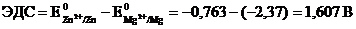
Контрольные вопросы
201. Составить схемы двух гальванических элементов, в одном из которых медь служила бы катодом, а в другом – анодом. Написать уравнения реакций, происходящих при работе этих элементов, и вычислить значения стандартных ЭДС. |
202. Кобальтовая и медная пластины соединены внешним проводником и погружены в раствор соляной кислоты. Составьте схему данного гальванического элемента и напишите электронные уравнения процессов происходящих на аноде и катоде. |
203. При каком условии будет работать гальванический элемент, электроды которого сделаны из одного и того же металла? Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, состоящего из медных электродов, опущенных: первый в 0,1 М, а второй 1 М растворы сульфата меди. |
204. В каком направлении будут перемещаться электроны во внешней цепи следующих гальванических элементов: а) |
205. При какой концентрации ионов |
206. Гальванический элемент состоит из серебряного электрода, погруженного в 1 М |
207. Увеличится, уменьшится или останется без изменений масса кобальтовой пластинки при взаимодействии её с растворами: а) |
208. ЭДС гальванического элемента, состоящего из стандартного водородного электрода и свинцового электрода, погруженного в 1 М раствор соли свинца, равна 0,126 В. При замыкании элемента электроны во внешней цепи перемещаются от свинцового к водородному электроду. Чему равен потенциал свинцового электрода? Составить схему элемента. Какие процессы протекают на его электродах? |
209. Гальванический элемент составлен из стандартного цинкового электрода и железного электрода, погруженного в раствор, содержащий ионы |
210. Рассчитать электродные потенциалы магния в растворе его соли при концентрациях иона |
211. Кадмиевая и никелевая пластины соединены внешним проводником и погружены в раствор серной кислоты. Составьте схему данного гальванического элемента и напишите электронные уравнения процессов происходящих на аноде и катоде. |
212. Увеличится, уменьшится или останется без изменений масса цинковой пластинки при взаимодействии её с растворами: а) |
213. ЭДС элемента состоящего из медного и свинцового электродов, погруженных в 1 М растворы солей этих металлов, равна 0,47 В. Изменится ли ЭДС если взять 0,01 М растворы? Ответ обосновать. |
214. Гальванический элемент составлен из стандартного цинкового электрода и хромового электрода, погруженного в раствор, содержащий ионы |
215. Потенциал cеребряного электрода составляет 80 % от значения его стандартного электродного потенциала. Чему равна концентрация ионов |
216. Какие процессы происходят на электродах гальванического элемента |
217. Составить схемы двух гальванических элементов, в одном из которых свинец служил бы катодом, а в другом – анодом. Написать уравнения реакций, происходящих при работе этих элементов, и вычислить значения стандартных ЭДС. |
218. Железная и никелевая пластины соединены внешним проводником и погружены в раствор серной кислоты. Составьте схему данного гальванического элемента и напишите электронные уравнения процессов происходящих на аноде и катоде. |
219. Составьте схему гальванического элемента, в основе которого лежит реакция, протекающая по уравнению:
Напишите электронные уравнения анодного и катодного процессов. Вычислите ЭДС этого элемента, если [ |
220. При какой концентрации ионов |
2.3. Коррозия металлов
Для ответов на контрольные вопросы рекомендуем воспользоваться литературой 5, 6, 7 и таблицей 6.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 |



