Для решения задач этого раздела рекомендуем воспользоваться литературой 4, 6, 8, 14 и таблицами 4,5.
Вода является очень слабым электролитом, степень ее диссоциации равна ![]() . Полярные молекулы воды в очень небольшой степени диссоциируют на ионы:
. Полярные молекулы воды в очень небольшой степени диссоциируют на ионы:
![]() =
= ![]() +
+ ![]() ,
,
или с учетом гидратации:
2![]() =
= ![]() +
+ ![]()
На основании законов химического равновесия получим выражение константы диссоциации воды:
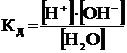 ,
,
отсюда
![]()
По данным измерения электропроводности при температуре ![]()
![]()
![]() , а молярная концентрация чистой воды
, а молярная концентрация чистой воды ![]() . Получаем значение
. Получаем значение ![]()
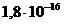
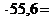
![]() Произведение
Произведение ![]() называется ионным произведением воды.
называется ионным произведением воды.
Если ![]() , то концентрация каждого из ионов воды равна
, то концентрация каждого из ионов воды равна ![]() =10-7 моль/л. Ионы водорода являются носителем кислотных свойств, а гидроксид-ионы – щелочных, следовательно, при равенстве их концентраций реакция среды раствора является нейтральной.
=10-7 моль/л. Ионы водорода являются носителем кислотных свойств, а гидроксид-ионы – щелочных, следовательно, при равенстве их концентраций реакция среды раствора является нейтральной.
При ![]() моль/л реакция среды будет кислой, а при
моль/л реакция среды будет кислой, а при ![]() - щелочной. Таким образом, концентрация ионов водорода является мерой его кислотности или щелочности.
- щелочной. Таким образом, концентрация ионов водорода является мерой его кислотности или щелочности.
Более удобен способ выражения реакции среды с помощью отрицательного десятичного логарифма концентрации водородных ионов, именуемого водородным показателем рН:
![]()
В нейтральной среде рН = 7; в кислой – рН < 7; в щелочной – рН > 7.
Растворение различных веществ в воде часто сопровождается химическим взаимодействием обменного характера. Процессы подобного типа объединяют под общим названием гидролиза. Гидролиз – это химический процесс обменного разложения вещества с водой. Гидролиз солей – частный случай взаимодействия растворенных солей с водой, где их составные части соединяются с составными частями воды с образованием соответствующего слабого электролита.
Реакцию гидролиза соли можно представить общим уравнением:
МА + НОН ⇄ МОН + НА,
соль вода основание кислота
где М – металл, А – остаток кислоты (анион).
Соли, образованные сильными кислотами и сильными основаниями (например, ![]() ,
,  и др.), гидролизу не подвергаются. Гидролиз характерен для солей, образованных: 1) слабой кислотой и сильным основанием, 2) сильной кислотой и слабым основанием, 3) слабой кислотой и слабым основанием. Приведем примеры.
и др.), гидролизу не подвергаются. Гидролиз характерен для солей, образованных: 1) слабой кислотой и сильным основанием, 2) сильной кислотой и слабым основанием, 3) слабой кислотой и слабым основанием. Приведем примеры.
Пример 1. Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей: а) ![]() ; б)
; б) 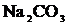 ; в)
; в) 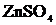 . Определите реакцию среды растворов этих солей.
. Определите реакцию среды растворов этих солей.
Решение: а) Цианид калия ![]() – соль слабой одноосновной кислоты
– соль слабой одноосновной кислоты ![]() и сильного основания
и сильного основания ![]() . При растворении в воде молекулы
. При растворении в воде молекулы ![]() полностью диссоциируют на катионы
полностью диссоциируют на катионы ![]() и анионы
и анионы ![]() . Катионы
. Катионы ![]() не будут связывать ионы
не будут связывать ионы ![]() воды, так как
воды, так как ![]() – сильный электролит, анионы же
– сильный электролит, анионы же ![]() связывают ионы
связывают ионы ![]() воды, образуя молекулы слабого электролита
воды, образуя молекулы слабого электролита ![]() . Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза
. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза
![]() +
+ ![]() ⇄
⇄ ![]() +
+ ![]()
или в молекулярной форме
![]() +
+ ![]() ⇄
⇄ ![]() +
+ ![]()
В результате гидролиза в растворе появляется некоторый избыток ионов ![]() , поэтому раствор
, поэтому раствор ![]() имеет щелочную реакцию (pH>7).
имеет щелочную реакцию (pH>7).
б) Карбонат натрия ![]() – соль слабой многоосновной кислоты
– соль слабой многоосновной кислоты 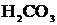 и сильного основания
и сильного основания ![]() . В этом случае анионы соли
. В этом случае анионы соли ![]() , связывая водородные ионы воды, образуют анионы кислой соли
, связывая водородные ионы воды, образуют анионы кислой соли 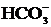 , а не молекулы
, а не молекулы ![]() . В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза
. В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза
![]() +
+ ![]() ⇄
⇄ 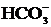 +
+ ![]()
или в молекулярной форме
![]() +
+ ![]() ⇄
⇄ ![]() +
+ 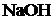
В растворе появляется избыток ионов OH![]() , поэтому раствор
, поэтому раствор ![]() имеет щелочную реакцию (pH>7).
имеет щелочную реакцию (pH>7).
в) Сульфат цинка ![]() – соль слабого многокислотного основания
– соль слабого многокислотного основания 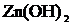 и сильной кислоты
и сильной кислоты ![]() . В этом случае катионы
. В этом случае катионы ![]() связывают гидроксильные ионы воды, образуя катионы основной соли
связывают гидроксильные ионы воды, образуя катионы основной соли ![]() . Образование молекул
. Образование молекул ![]() не происходит, так как ионы
не происходит, так как ионы ![]() диссоциируют гораздо труднее, чем молекулы
диссоциируют гораздо труднее, чем молекулы 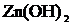 . В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза
. В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза
![]() +
+ ![]()
![]() ⇄
⇄ 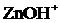 +
+ ![]()
или в молекулярной форме
2![]() + 2
+ 2![]() ⇄
⇄ 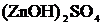 +
+ ![]()
В растворе появляется избыток ионов водорода, поэтому раствор 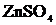 имеет кислую реакцию (pH< 7).
имеет кислую реакцию (pH< 7).
Пример 2. Какие продукты образуются при смешивании растворов ![]() и
и ![]() ? Составьте ионно-молекулярное и молекулярное уравнение реакции.
? Составьте ионно-молекулярное и молекулярное уравнение реакции.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 |



