где n - число молей растворенного вещества, моль;
![]() - масса растворенного вещества, г;
- масса растворенного вещества, г;
![]() - молярная масса растворенного вещества г/моль;
- молярная масса растворенного вещества г/моль;
![]() - объем раствора, л
- объем раствора, л
Пример 3. Определите молярную концентрацию раствора, полученную при растворении сульфата натрия массой 21,3 г в воде массой 150 г, если плотность полученного раствора равна 1,12 г/мл.
Решение: Определяем массу полученного раствора:
![]() ;
;
![]() = 21,3 + 150 = 171,3 г.
= 21,3 + 150 = 171,3 г.
Вычисляем объем раствора:
![]() ;
; ![]() = 153 мл = 0,153 л.
= 153 мл = 0,153 л.
Количество вещества растворенного сульфата натрия равно
![]() ;
; ![]() = 0,15 моль.
= 0,15 моль.
Рассчитываем молярную концентрацию раствора:
![]() , моль/л
, моль/л
![]() моль/л.
моль/л.
Молярная концентрация эквивалента ![]() (нормальная концентрация) – количество вещества эквивалента, содержащегося в 1 л раствора.
(нормальная концентрация) – количество вещества эквивалента, содержащегося в 1 л раствора.
![]() , моль/л
, моль/л
где МЭ =![]() (см. раздел 1.1).
(см. раздел 1.1).
Пример 4. Какой объем 96%-ной кислоты плотностью 1,84 г/см3 потребуется для приготовления 5 л раствора с молярной концентрацией эквивалента равной 0,3 моль/л?
Решение: Молярная масса эквивалента серной кислоты определяется по формуле:
![]() г/моль
г/моль
Находим массу серной кислоты для приготовления 3 л раствора с молярной концентрацией эквивалента 0,3 моль/л, если
![]() , выразим из этого выражения массу вещества (
, выразим из этого выражения массу вещества (![]() )
)
![]() .
.
Масса 1 см3 96%-ной кислоты 1,84 г. В этом растворе содержится
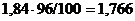 г серной кислоты.
г серной кислоты.
Следовательно, для приготовления 5 л раствора с молярной концентрацией эквивалента 0,3 моль/л надо взять 73,5:1,76=41,76 см3 кислоты.
Пример 5. На нейтрализацию 50 см3 раствора кислоты израсходовано 25 см3 раствора щелочи с молярной концентрацией эквивалента 0,5 моль/л. Чему равна молярная концентрация эквивалента кислоты?
Решение: Так как вещества взаимодействуют между собой в эквивалентных соотношениях, то растворы с равными концентрациями эквивалента реагируют в равных объемах. При разных концентрациях объемы растворов реагирующих веществ обратно пропорциональны их концентрациям, т. е.
![]() или
или ![]()
Подставим в последнее выражение известные данные:
![]() , откуда
, откуда ![]() = 25 . 0,5/50 = 0,25 моль/л.
= 25 . 0,5/50 = 0,25 моль/л.
Безразмерные концентрации.
Мольная доля (![]() ) – отношение числа молей растворенного вещества к сумме числа молей всех компонентов раствора.
) – отношение числа молей растворенного вещества к сумме числа молей всех компонентов раствора.
![]()
где ![]() - число молей растворенного вещества.
- число молей растворенного вещества.
Титр (![]() ) - масса вещества, содержащегося в 1 мл или в 1 см3 раствора.
) - масса вещества, содержащегося в 1 мл или в 1 см3 раствора.
![]() , г/мл.
, г/мл.
Титр связан с молярной концентрацией эквивалента соотношением:
![]()
Контрольные вопросы
101. Из 15 кг 18%-ного раствора при охлаждении выделилось 380 г соли. Чему равна массовая доля охлажденного раствора?
102. Чему равна молярная концентрация эквивалента 25%-ного раствора NaOH плотностью 1,328 г/см3? К 1 л этого раствора прибавили 6 л воды. Вычислите массовую долю полученного раствора.
103. Из 650 г 55%-ной серной кислоты выпариванием удалили 180 г воды. Чему равна массовая доля оставшегося раствора?
104. Вычислите молярную концентрацию эквивалента и молярную концентрацию 20,8%-ного раствора НNO3 плотностью 1,12 г/см3. Сколько граммов кислоты содержится в 7 л этого раствора?
105. Вычислите молярную, молярную концентрацию эквивалента и моляльную концентрации 26%-ного раствора хлорида алюминия плотностью 1,149 г/см3.
106. Смешали 400 г 20%-ного раствора и 600 г 40%-ного раствора NaCl. Чему равна массовая доля полученного раствора?
107. Для осаждения в виде AgCl всего серебра, содержащегося в 100 см3 раствора AgNO3, потребовалось 75 см3 раствора НСl с молярной концентрацией эквивалента 0,3 моль/л. Какова молярная концентрация эквивалента раствора AgNO3? Какая масса AgCl выпала в осадок?
108. Какая масса НNO3 содержалась в растворе, если на нейтрализацию его потребовалось 50 см3 раствора NaOH с молярной концентрацией эквивалента 0,3 моль/л? Каков титр раствора NaOH?
109. Смешали 30 см3 10%-ного раствора HNO3 (пл. 1,056 г/см3) и 150 см3 30%-ного раствора НNO3 (пл. 1,184 г/см3). Вычислите массовую долю полученного раствора.
110. Какой объем 45%-ного раствора КОН (пл. 1,538 г/см3) требуется для приготовления 3л 4%-ного раствора (пл. 1,048 г/см3)?
111. Какую массу NaNO3 нужно растворить в 300 г воды, чтобы приготовить 20%-ный раствор?
112. На нейтрализацию 26 см3 раствора щелочи с молярной концентрацией эквивалента 0,15 моль/л требуется 167 см3 раствора Н2SO4. Чему равны молярная концентрация эквивалента и титр раствора Н2SO4?
113. Какой объем раствора кислоты с молярной концентрацией эквивалента 0,35 моль/л требуется для нейтрализации раствора, содержащего 0,42 г NaOH в 40 см3?
114. На нейтрализацию 1 л раствора, содержащего 1,25 г КОН, требуется 50 см3 раствора кислоты. Вычислите молярную концентрацию эквивалента кислоты.
115. Какой объем 18,01%-ного раствора HCl (пл. 1,100 г/см3) требуется для приготовления 1 л 8,17%-ного раствора (пл. 1,050 г/см3) ?
116. Какой объем 18%-ного раствора карбоната натрия (пл. 1,105 г/см3) требуется для приготовления 5 л 4%-ного раствора (пл. 1,02 г/см3)?
117. Сколько и какого вещества останется в избытке, если к 75 см3 раствора Н2SO4 с молярной концентрацией эквивалента 0,5 моль/л прибавить 125 см3 раствора КОН с молярной концентрацией эквивалента 0,3 моль/л?
118. Смешали 278 г 62%-ного и 132 г 18%-ного раствора серной кислоты. Какова массовая доля полученного раствора?
119. К 4 л 10%-ного раствора НNO3 плотностью 1,054 г/см3 прибавили 3 л 2%-ного раствора той же кислоты плотностью 1,009 г/см3. Вычислите массовую долю и молярную концентрацию полученного раствора, объем которого равен 7 л.
120. Вычислите молярную концентрацию и молярную концентрацию эквивалента 28%-ного раствора хлорида кальция плотностью 1,178 г/см3.
1.7. Свойства растворов
Для решения задач этого раздела рекомендуем воспользоваться литературой 6, 8, 10, 16.
Важной физико-химической характеристикой твердых и жидких тел является давление пара, определяющее состояние равновесия между конденсированной и газообразной фазами. Чем выше давление пара, тем больше равновесие смещается в сторону процессов сублимации и испарения. Поэтому давление насыщенного пара над раствором используется для объяснения его поведения и свойств.
Понижение давления пара над раствором приводит к изменению температур кипения и замерзания по отношению к чистым растворителям. Известно, что жидкость кипит или кристаллизуется, когда давление ее насыщенного пара становится равным внешнему давлению или давлению насыщенного пара над твердой фазой, в которую она переходит. Раствор вследствие пониженного давления его паров труднее достигает точки кипения или точки кристаллизации. В связи с этим растворы кипят при более высоких и кристаллизуются при более низких температурах, чем чистые растворители. По закону Рауля: повышение температуры кипения или понижение температуры кристаллизации раствора прямо пропорционально моляльной концентрации растворенного вещества:
![]() и
и ![]()
где 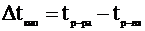
![]()
![]() - моляльная концентрация, моль/г
- моляльная концентрация, моль/г
![]() - эбуллиоскопическая константа
- эбуллиоскопическая константа
![]() - криоскопическая константа.
- криоскопическая константа.
Закон Рауля имеет практическое значение - по изменению температуры кипения и кристаллизации определяют молекулярные веса неизвестных веществ. Преобразуем математические уравнения закона Рауля. Зная, что

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 |



