Генетические факторы играют ключевую роль в запуске патогенеза целиакии, у 10-15% ближайших родственников больных выявляются морфологические признаки целиакии. В среднем, 14% родителей пациентов сами страдают целиакией в скрытой форме [67,160]. Механизм наследования относится к аутосомно-доминантному типу с неполной пенетрантностью. Следовательно, в патогенезе участвуют несколько генов. Конкордантность по заболеваемости обнаружена у монозиготных близнецов 70-100% [87,132,178]. Заболеваемость среди братьев и сестер (сибсов) выше, чем у родственников пробандов, что характерно для полигенных заболеваний. Исследования различных генетических маркеров дали основание полагать, что гены, ответственные за непереносимость глютена локализованы в хромосомах 6 и 14 [12,87].
1.3 Этиология и патогенез целиакии.
В этиологии целиакии ведущую роль играет глютен.
Глютен (пшеничная клейковина) - запасный протеин эндосперма зерна злаковых культур пшеницы, ржи, ячменя, овса. Слово «глютеин» происходит от английского glue - клей. Белки злаков имеют в составе 4 фракции: альбумины, глобулины, проламины и глютенины. Две последние фракции носит название «глютен». Глютен представляет собой нерастворимый в воде комплекс белков с низким содержанием сахаров и липидов. Глютен пшеницы придает хлебу из пшеничной муки его особые свойства - «эластичность» и пышность. Именно глютен пшеницы является главной и наиболее частой причиной развития пищевой аллергии. Ячмень, рожь и овес имеют меньше содержание глютена, чем пшеница. Токсичными для больных целиакией являются проламины (спирторастворимые протеины, богатые глютамином и пролином). Антигенной фракцией пшеницы является глиадин, ржи - секалин, ячменя – гордеин, овса – авенин, кукрузы - зеин, риса – орезин, в пшене - каферин. Токсическими фракциями этих проламинов считается последовательность аминокислот Про-Сер-Глю-Глю и Глю-Глю-Глю-Про [12,59,148,163,224].
В настоящее время получило широкое распространение мнение, что овес не является токсичным, по крайней мере, для взрослых больных целиакией, и может употребляться в составе аглиадиновой диеты [222]. Вопрос о токсичности овса для больных целиакией нуждается в дальнейшем изучении, так как реакция на овес у больных неоднозначна [158,184,186,222].
Глиадиновый белок, устойчивый к воздействию пищеварительных ферментов, беспрепятственно достигает просвета тонкой кишки. В норме плотные межклеточные контакты ограничивают пассаж макромолекулярных соединений, в том числе глютена, через эпителиальный барьер. Глютен вызывает нарушение регуляции зонулина - белка, участвующего в организации межклеточных контактов, что приводит к увеличению межклеточной проницаемости и обеспечивает всасывание и проникновение глиадинового белка в собственную пластинку.
Кроме того, глиадиновый белок имеет высокую аффинность к тканевой трансглютаминазе (tTG) - кальций-зависимому ферменту, который экспрессируется на субэпителиальном слое и дезаминирует глиадиновный белок. При этом положительно заряженный глютамин трансформируется в глютаминовую кислоту с отрицательным зарядом, которая вступает в контакт с имеющими положительный заряд карманами полостей молекул HLA DQ2 или DQ8. Таким образом, дезаминированные глиадиновые белки образуют комплексы с молекулами HLA-системы, захватываются антигенпрезентирующими клетками, происходит распознавание этих антигенов и инициируется иммунный ответ, результатом которого является формирование Т-хелперов 1-го и 2-го типа. Т-хелперы 1-го порядка определяют клеточную иммунорегуляцию с активизацией цитотоксических Т-лимфоцитов, выработкой интерферона-гамма, стимуляцией воспаления. Т-хелперы 2-го порядка запускают выработку антител В-клетками. В итоге развивается воспаление и атрофия ворсинок, в процесс активно вовлекается лимфоидная ткань кишки. При прогрессировании процесса запускается аутоиммунный механизм, результатом которого является выработка аутоантител, в том числе к тканевой трансглутаминазе, антиретикулиновые, энтиэндомизийные. В результате повреждения гликокаликса, а также щеточной каемки энтероцитов с мембранными ферментами, к которым относятся лактаза, сахараза, мальтаза, изомальтаза и др. развивается непереносимость соответствующих пищевых веществ [6,12,18,64,164].
При нарушении ферментативной активности тонкой кишки некоторое количество пищи попадает в ее дистальные отделы в нерасщепленном состоянии. Вследствие нарушения проницаемости слизистой оболочки во внутреннюю среду попадает большое количество нерасщепленных белков. Изменяется нормальный состав микрофлоры тонкой и толстой кишок, что приводит к нарушению метаболизма холестерина, желчных кислот, снижению
синтеза витамина К и группы В.
Существует гипотеза о роли вирусов в патогенезе целиакии. Несколько наблюдений свидетельствуют о том, что слизистая оболочка тонкой кишки может оставаться интактной в течение нескольких лет употребления глютена, после чего развитие атрофии происходит под влиянием некоего провоцирующего фактора. Обсуждается значение рота - и энтеровирусов в патогенезе целиакии [194].
Было обнаружено, что белок-аденовируса-12 обладает определенной гомологией с глиадином, что могло бы приводить к перекрестной реактивности иммунной системы. Однако целиакия развевается далеко не всегда, когда в крови обнаруживаются антитела к антигенам этого вируса. Но, скорее всего, вирусы играют вторичную роль в патогенезе целиакии, так как уровень антител к аденовирусам в крови снижается на фоне аглиадиновой диеты без какого–либо специфического противовирусного лечения [2,164].
Высказано подобное предположения и в отношении Candida albicans. Имеются наблюдение, что дети рожденные летом, имеют больший риск раннего дебюта целиакии, поскольку введение прикорма у них совпадает с началом эпидемического подъема заболеваемости кишечными инфекциями. А это косвенно говорит о роли инфекционного процесса, как пускового механизма развития целиакии [154,211].
Согласно генетической теории, глютен связывается со специфическими рецепторами энтероцитов, экспрессия которых детерминирована генами системы HLA и генами, определяющими чувствительность к глютену. В результате образуются специфические иммунные продукты, которые повреждают энтероциты ворсинок. По данным популяционных исследований в Европе, высокая частота выявлений аллелей DQ2/DQ8 у больных целиакией и по мнению ряда авторов, развитие заболевания практически невозможно при отсутствии в генотипе данных гетеродимеров [164,230].
1.4 Клиническая картина целиакии.
Проводятся попытки систематизировать клиническую симптоматику целиакии с выделением типичных и атипичных проявлений [40,70,130]. Предложено деление клинических симптомов на основные и дополнительные [46], на гастроинтестинальные и эктсраинтестинальные [95,129,202]. Разделение клинических проявлений целиакии представляется условным.
Считается, что для детской целиакии более характерна классическая манифестная форма, которая протекает с поражением в основном ЖКТ, нервной системы и снижением массы тела. У детей старшего возраста присоединяются поражения других органов и систем, что максимально приближает к проявлениям взрослой целиакии [105,129].
Максимальная частота дебюта целиакии приходится на возраст от 6 месяцев до 2 лет [2,26,115]. Предположение о внутриутробной сенсибилизации плода злаковыми белками в настоящее время подтверждения не нашло [47]. Сроки манифестации целиакии зависят от времени введения в питание ребенка глютенсодержащих продуктов, происходит воздействие на генетически предрасположенную слизистую оболочку кишечника. Очень часто манную кашу начинают давать в возрасте 4-6 месяцев [3,45], поэтому в классическом случае первые проявления заболевания выявляются на 6-8 месяце жизни. Чем раньше введены глютенсодержащие продукты в рацион питания ребенка, тем раньше происходит манифестация симптомов целиакии [4,28,45,114].
Проведенные в Эстонии исследования показали, что раннее отнятие младенца от груди приводит к ранней и тяжелой манифестации целиакии, а ротавирусная инфекция существенно увеличивает риск развития ее аутоиммуногенности [207].
В ряде случаев манифестация целиакии происходит несколько позже, порой через 5-6 месяцев и более после введение глиадинсолержащих продуктов, или после воздействия факторов способствующих реализации генетических дефектов - перенесенного вирусного заболевания, кишечной инфекции, стрессовые ситуации. Инфекционный процесс, в данном случае, является не причиной, а провоцирующим фактором [115].
Нередко клиническая манифестация целиакии происходит без видимой
причины. Если у детей заболевание обычно развивается после введения глютена - впервые 2 года жизни, то у взрослых она чаще всего проявляется после 30 лет [58,143]. По некоторым данным лица в возрасте 60 лет и старше составляют 4-7 % больных целиакией [15].
Клинические проявления целиакии развиваются, как правило, постепенно. Дети становятся раздражительными, нередко появляется озлобленность, капризность, боязливость, дети теряют навыки, приобретенные ранее [46,48,53]. На эти симптомы родители часто не обращают внимания и связывают их обычно с прорезыванием зубов. Появление жидкого или кашицеобразного стула с увеличением количества каловых масс, увеличения живота, отсутствие аппетита, отсутствием прибавки массы тела, или потеря массы, снижением двигательной активности ребенка, нарушение моторного развития заставляют родителей, обратится к врачу. Эти симптомы могут проявляться одновременно или в любой последовательности, что затрудняет своевременную диагностику целиакии. В этот период примерно у половины детей диагностируют кишечные инфекции, как правило, лабораторно неподтвержденные. Такие дети получают массивные курсы антибиотиков, что еще более усугубляет течение заболевания, и способствуют развитию кишечного дисбиоза. В связи с выше указанным, целиакию следует исключать в ходе дифференциальной диагностики во всех случаях синдрома мальабсорбции неясного происхождения [17,46,114].
При классическом (типичном) варианте течения заболевания отмечается
значительное снижение массы тела ребенка (нередко гипотрофия II-III степени) [53,64], а так же отставание в росте. Однако около 30% больных нелеченной целиакией имеют избыточный вес. Характерен учащенный, водянистый, кашицеобразный, пенистый, ахоличный, зловонный, плохо смывающийся с горшка светло-коричневый или серый стул [39,46,115]. Стул может быть обильным до 10 раз в день [30]. Для классической целиакии характерна полифекалия, даже при небольшой частоте дефекации. Количество каловых масс превышает 5% массы съеденной пищи [4,46,116]. Однако у части детей отмечаются запоры, а иногда полифекалия без нарушения частоты стула [58].
В фазе разгара отмечается резкое снижение аппетита. Часто возникает рвота и срыгивания, которая усиливает электролитные нарушения, возникающие на фоне диареи [6,115]. Характерен внешний вид больных напоминающий «паука»: увеличен в размерах живот, за счет скопления жидкого химуса в атонически расширенных петлях кишечника в сочетании с тонкими конечностями и несчастным выражением лица [46,116].
Проявления синдрома мальабсорбции представлены на рисунке 1.1
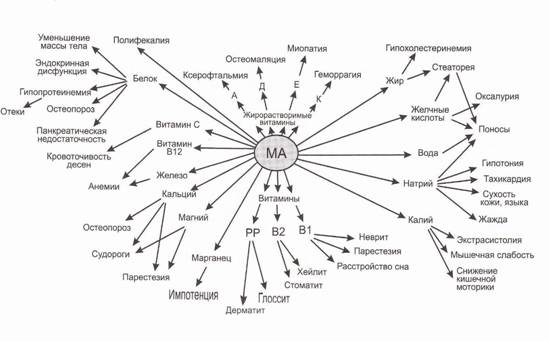
Рисунок 1.1 Симптоматика синдрома мальабсорбции [35]
При целиакии страдают все виды обмена, в первую очередь белковый. С одной стороны, мальабсорбция сама по себе может привести к значительной белковой недостаточности, с другой стороны, повреждение слизистой оболочки тонкой кишки нередко приводит к развитию вторичной экссудативной энтеропатии с дополнительной потерей белка. Выраженные гипопротеинемия и гипоальбуминемия, приводят к безбелковым отекам, вплоть до анасарки [27,54,60,103,201].
Со временем симптомы (в процессе роста и без лечения) целиакии претерпевают изменения, в процесс вовлекаются другие органы и системы, усиливая многообразие проявлений и еще более затрудняя диагностику заболевания.
Доминирующей в клинической картине является патология желудочно-кишечного тракта, который в той или иной степени поражается на всем протяжении. Частыми клиническими проявлениями являются парадонтит, гингивит, глоссит, стоматит [187,188,220]. Так же характерны стеноз луковицы двенадцатиперстной кишки и постбульбарное дуоденальное образование язв, лимфоцитарный гастрит [37,170,231], колит [147].
У взрослых довольно часто отмечаются аноректальные осложнения: проктит или парапроктит с болями, тенезмами, анальным зудом, трещинами ануса. Боли в животе имеют непостоянный «тупой» характер, локализуется преимущественно в околопупочной области, проходят после дефекации или самостоятельно. Однако существует мнение, что боли в животе у взрослых больных с неосложненной глютеновой энтеропатией встречаются редко [116].
При целиакии в активной стадии заболевания поражение поджелудочной железы наблюдается у 88% больных, в стадии ремиссии у 79%. Повышение в крови активности трипсина, говорящее о деструктивном процессе в поджелудочной железе, скорее всего, обострении хронического панкреатита, наблюдается у 37% детей в активной стадии целиакии и у 12% больных в стадии ремиссии [37].
 Целиакия характеризуется развитием атрофии слизистой оболочки тонкой кишки, которая является причиной мальабсорбции. Данная атрофия носит гиперрегенераторный характер, что проявляется значительным углублением крипт и повышением митотической активности в них. Вместе с увеличением числа собственно энтероцитов, в криптах увеличивается также число некоторых энтероэндокринных клеток. Характерно повышение числа соматостатин-продуцирующих D-клеток в слизистой оболочке тонкой кишки в активную стадию целиакии и нормализацию их числа в стадию ремиссии [12,31,39,50]. Гиперплазия D-клеток сопровождается стимуляцией их активности и увеличением продукции соматостатина который в свою очередь играет роль в задержке роста [22]. Уровень соматостатина повышается локально в слизистой оболочке, обеспечивая паракринную регуляцию, но не изменяется в системном кровотоке. Гиперсекреция соматостатина является закономерным регуляторным ответом на гиперрегенерацию слизистой оболочки тонкой кишки и призвана сдерживать ее в определенных пределах. Вместе с тем нельзя исключить, что соматостатин в какой-то мере усугубляет и без того нарушенные процессы всасывания. Помимо воздействия на процессы регенерации и всасывания, одной из точек приложения соматостатина являются другие энтероэндокринные клетки, в т. ч. L-клетки, продуцирующие холецистокинин, и S-клетки, продуцирующие секретин. Нормальные результаты секретинового и холецистокининового тестов говорят о том, что снижение функции поджелудочной железы в активную стадию целиакии связано именно с нарушением паракринной регуляции, но не с непосредственным влиянием соматостатина на ацидные клетки поджелудочной железы [6,12,14,37].
Целиакия характеризуется развитием атрофии слизистой оболочки тонкой кишки, которая является причиной мальабсорбции. Данная атрофия носит гиперрегенераторный характер, что проявляется значительным углублением крипт и повышением митотической активности в них. Вместе с увеличением числа собственно энтероцитов, в криптах увеличивается также число некоторых энтероэндокринных клеток. Характерно повышение числа соматостатин-продуцирующих D-клеток в слизистой оболочке тонкой кишки в активную стадию целиакии и нормализацию их числа в стадию ремиссии [12,31,39,50]. Гиперплазия D-клеток сопровождается стимуляцией их активности и увеличением продукции соматостатина который в свою очередь играет роль в задержке роста [22]. Уровень соматостатина повышается локально в слизистой оболочке, обеспечивая паракринную регуляцию, но не изменяется в системном кровотоке. Гиперсекреция соматостатина является закономерным регуляторным ответом на гиперрегенерацию слизистой оболочки тонкой кишки и призвана сдерживать ее в определенных пределах. Вместе с тем нельзя исключить, что соматостатин в какой-то мере усугубляет и без того нарушенные процессы всасывания. Помимо воздействия на процессы регенерации и всасывания, одной из точек приложения соматостатина являются другие энтероэндокринные клетки, в т. ч. L-клетки, продуцирующие холецистокинин, и S-клетки, продуцирующие секретин. Нормальные результаты секретинового и холецистокининового тестов говорят о том, что снижение функции поджелудочной железы в активную стадию целиакии связано именно с нарушением паракринной регуляции, но не с непосредственным влиянием соматостатина на ацидные клетки поджелудочной железы [6,12,14,37].
Другой механизм повреждения поджелудочной железы связан с нарушением ее трофики. Важными трофическими факторами для ткани поджелудочной железы являются такие регуляторные пептиды желудочно-кишечного тракта, как гастрин и холецистокинин. Уровень гастрина в крови, также под влиянием гиперпродукции соматостатина, снижается в активную стадию целиакии. Количество гастрин-продуцирующих G-клеток при этом не изменяется ни в желудке, ни в двенадцатиперстной кишке. Что указывает на функциональный характер нарушений. Тем не менее, в сочетании со снижением продукции холецистокинина могут развиваться трофические нарушения, способствующие как снижению функции органа, так и создающие условия для развития хронического панкреатита в дальнейшем. Так же недостаточность холецистокинина приводит к снижению сократительной функции желчного пузыря [37,52,53].

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 |



