Сегодня на рынке имеется много заквасок для силосования. Силос, приготовленный на их основе, имеет запах кислой капусты и других овощей.
Помимо таких важных конечных показателей готового силоса как значение рН и питательность, существует еще один важнейший показатель – это аромат. Доказано, что правильно приготовленный и ароматный силос поедается гораздо лучше. Такой силос способствует поддержанию микрофлоры рубца у коров, что обеспечивает увеличение продуктивности и улучшение качественных характеристик молока и повышает суточный удой с 18.5 до 20 л [1].
Для приготовления ароматной закваски для силосования можно использовать такие микроорганизмы, как ароматобразующие молочнокислые стрептококки. К ним относятся Streptococcus diacetilactis, Str. acetoinicus, Str. paracitrovorus (Leuconostoc citrovorum), Str. citrovorus (Leuconostoc citrovorum).
Ароматобразующие бактерии выделяют в молоке и молочных продуктах повышенное количество летучих кислот (уксусная и пропионовая) и ароматических веществ (эфиры, диацетил). Большинство из них содержит фермент цитритазу, поэтому способны сбраживать лимонную кислоту; за эту способность их называют цитроворусами.
Целью данного исследования явился поиск смешанной закваски микроорганизмов для получения силоса с хорошими вкусовыми и органолептическими характеристиками.
В ходе эксперимента был проведен скрининг молочнокислых бактерий из следующих субстратов: рассола помидор, рассола капусты, рассола огурцов, молочнокислых продуктов (творога, сметаны, напитков «Biomax», «Актимель», «Иммуннуле», «Активиа»). Образцы субстратов инкубировали на жидкой пептонной среде в пробирках в течение 5-14 суток при температуре 30оС, затем чистые культуры выделяли на агаризованной среде с 2 % мела на чашках Петри. Выделенные из рассолов микроорганизмы были идентифицированы как Lactobacillus plantarum, а из молочнокислых напитков - Streptococcus diacetilactis.
В ходе эксперимента по модельному силосованию свежей травы были выбраны наиболее активные ароматобразующие бактерии («Иммуннеле» и «Biomax») и наиболее активные лактобактерии. Образцы зеленой травы массой 50 г плотно утрамбовывали в баночках, закупоривали крышками для создания анаэробных условий и инкубировали суспензиями молочнокислых бактерий из расчета 105-106 клеток бактерий на 1 г травы. Силосование длилось 18-20 дней при комнатной температуре. О качестве силосованного корма можно судить по содержанию органических кислот, накопившихся при брожении. В ходе силосования периодически оценивали запах травы, а также измеряли величины рН и кислотности. Результаты экспериментального силосования представлены в таблице 1.
Таблица 1 – Основные показатели качества препаратов силоса
Закваска | L. plantarum | L. plantarum + «Иммуннеле» (1:1)* | L. plantarum + «Biomax» (1:1)* | L. plantarum + «Иммуннеле» (1:10)* |
№ образца | 1 | 2 | 3 | 4 |
Величина рН через 20 суток | 4,2 | 3,7 | 4,02 | 3,87 |
Кислотность, ºТ | 0,7 | 0,7 | 0,7 | 0,7 |
Запах | овощной | овощной | кислых овощей | торфяной, травянистый |
*- в скобках указаны соотношения объемов засеваемых образцов суспензий микроорганизмов
Из таблицы 1 видно, что наиболее качественный образец силоса получили при внесении смешанной закваски бактерий L. plantarum и «Иммуннеле», взятых в соотношении 1:1 (по объему).
Список литературы:
1 Электронный ресурс: Карпов, силосования/ . Режим доступа: http://www. fermer/zhivoth
547.269.352’853.7
, ,
ФУНКЦИОНАЛИЗАЦИЯ СУЛЬФОНИЛИМИНОВ ПОЛИХЛОРАЦЕТАЛЬДЕГИДОВ 2-АМИНОПИРИМИДИНОМ
Федеральное государственное бюджетное учреждение науки
Иркутский институт химии им. СО РАН, г. Иркутск,
E-mail: *****@
Для разработки эффективных подходов к получению функционализированных производных сульфонамидов, содержащих в структуре фармакофорные сульфонамидные и аминопиримидиновые фрагменты, мы изучили взаимодействие арилсульфонилиминов фенилдихлорацетальдегида и хлораля 1, 2 с аминопиримидином. Активированные имины 1, 2 могут быть легко получены реакцией
N, N-дихлораренсульфонамидов с фенилацетиленом или трихлорэтиленом по ранее разработанным методам [1,2].
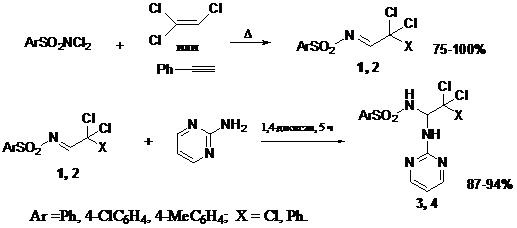
Установлено, что реакция протекает хемоселективно с образованием
N-[1-(пиримидин-2-ил)амино-2-полихлорэтил]аренсульфонамидов 3, 4 – продуктов нуклеофильного присоединения гетероциклического амина к активированным азометиновым группам.
Из-за наличия в структуре сульфонамидной группы, эндоциклических аминогрупп и полихлорметиленового фрагмента соединения 3, 4 представляют интерес в качестве объектов для физико-химических исследований, изучения биологической активности и перспективны для последующей гетероциклизации в имидазопиримидиновые производные.
Работа выполнена при поддержке РФФИ № мол_а.
Список литературы:
1 , , ЖОХ, 2008, 78(7), 1135.
2 Krivdin L. B., Chernyshev K. A., Rosentsveig G. N., Ushakova I. V., Rosentsveig I. B., Levkovskaya G. G. Magnetic Resonance in Chemistry, 2007, 45, 980.
УДК 547.541.1
,
ПОЛУЧЕНИЕ ТЕТРАГИДРОЦИКЛОПЕНТА[b]ИНДОЛОХИНОНОВ
Институт органической химии УНЦ РАН, г. Уфа
E-mail: dos01@ya.ru
Некоторые представители соединений ряда индолохинонов проявляют биологическую активность, благодаря чему привлекают внимание исследователей [1-3]. Структуры подобного типа могут быть получены как непосредственно из хинонов [4], так и последовательными трансформациями производных индола.
С целью выхода к подобным соединениям мы исследовали их синтез исходя из пара-толуидина (I). По методикам [5] были получены индолины (IIa, б), нитрование которых проводили смесью нитрата аммония и (F3CCO)2O в дихлорметане в мягких условиях. Нагреванием соединений (IIIa, б) со свежеприготовленным Fe(OH)2 в аммиачном растворе синтезировали 5-аминопроизводные (IVa, б), окисление которых солью Фреми приводит к образованию индолохинонов (Vа, б). При попытке введения азиридинового фрагмента в положение 6 соединения (Vа) произошло восстановление хиноидной структуры до гидрохиноновой с образованием гетероцикла (VI).
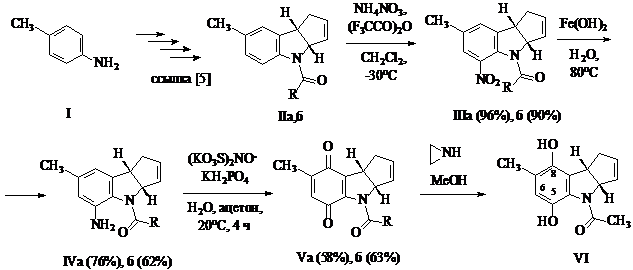
Список литературы:
1 Wang C., Sperry J. J. Org. Chem. 2012, 77, 2584.
2 Xing С., Wu Р., Skibo E. B., Dorr R. T. J. Med. Chem. 2000, 43, 457.
3 Skibo E. B., Xing С., Dorr R. T. J. Med. Chem. 2001, 44, 3545.
4 Luly J. R., Rapoport H. J. Org. Chem. 1984, 49, 1671.
5 , , ЖОрХ. 2012, 48, 962.
УДК 573.6.086.83:550.7
, ,
БИОВЫЩЕЛАЧИВАНИЕ СУЛЬФИДНЫХ МИНЕРАЛОВ КОНСОРЦИУМОМ УМЕРЕННО-ТЕРМОФИЛЬНЫХ ОРГАНИЗМОВ В УСЛОВИЯХ ПОВЫШЕННОЙ КОНЦЕНТРАЦИИ ИОНОВ Fe3+
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Уфимский государственный нефтяной технический университет, г. Уфа
Е-mail:*****@***net
Биовыщелачивание сульфидных минералов заключается в разрушении их кристаллической структуры и высвобождении металлов и серы в виде растворимых форм с участием микроорганизмов. Чаще всего выщелачивание протекает в кислых условиях и достигается за счёт протонных атак на минерал и окисления его компонентов [1]. Микроорганизмы могут принимать участие в биовыщелачивании непосредственно за счёт ферментативного разрушения минерала или опосредованно – за счёт регенерации выщелачивающих агентов, таких как ионы Fe3+ или Н+ [2], а также облегчать химическое выщелачивание минерала ионами Fe3+ благодаря слою внеклеточных полимеров [1]. В настоящее время считается, что основной вклад микроорганизмов в процессы биовыщелачивания заключается в регенерации ионов Fe3+ [1, 3].
Технологии биовыщелачивания являются перспективными поскольку благодаря низким капитальным и эксплуатационным затратам позволяют извлекать металлы из бедных руд, а также отвалов отработанных месторождений, переработка которых традиционными пирометаллургическими методами нерентабельна.
С одного из таких месторождений – отработанного месторождения пирита Куль-Юрт-Тау – нами была выделена накопительная культура микроорганизмов, способная окислять сульфидные минералы. Данная культура продемонстрировала устойчивость к высоким концентрациям железа в среде.
Было обнаружено, что процессы биовыщелачивания пирита и медного концентрата с помощью полученной накопительной культуры интенсифицируются с увеличением концентрации химического окислителя сульфидов (ионов Fe3+) до 40 г/л. Показано, что даже при таких концентрациях происходит не только активное выщелачивание металлов, но и регенерация ионов Fe3+. Обнаружено, что в исследуемых системах не происходит повышения концентрации Fe2+. Полученные данные свидетельствуют о том, что найденный консорциум способен сохранять свою активность даже при концентрациях Fe3+ 75 г/л, что делает его перспективным для применения в процессах биовыщелачивания, поскольку при высоких концентрациях выщелачивающего агента скорость выщелачивания также возрастает.
Список литературы:
1 E. R. Donati, W. Sand Microbial Processing of Metal Sulfides. – Dordrecht, The Netherlands – 2007. – 314 p.
2 Y. Rodríguez, A. Ballester, M. L. Blázquez, F. González, J. A. Muñoz // Hydrometallurgy. – 2003. – Vol. 71. – P.47 – 56
3 D Barrie Johnson, Tadayoshi Kanao, Sabrina Hedrich // Frontiers in microbiology. – 2012. – Vol.3: Art.96.
УДК 547.824:542.91:548.737
,1 ,2 Х. До Тхи Тху,3 1
ОЗОНОЛИЗ ДАММАРАНОВОГО ТРИТЕРПЕНОИДА ДИПТЕРОКАРПОЛА ИЗ DIPTEROCARPUS ALATUS
1Федеральное государственное бюджетное учреждение науки Институт органической химии Уфимского научного центра Российской академии наук,
г. Уфа,
E-mail: *****@***ru
ФГБОУ ВПО Башкирский государственный университет, инженерный факультет, г. Уфа
3Институт химии Вьетнамской академии наук и технологий, г. Ханой, Вьетнам
Тритерпеноиды даммаранового типа, в том числе диптерокарпол, обладают различными видами активности (противораковой, противовирусной, иммуностимулирующей). Учитывая высокие перспективы даммарановых тритерпеноидов как фармакологически ценных агентов (в основном благодаря метаболитам корня женьшеня и листьев березы), а также сырьевую доступность диптерокарпола, нами начаты исследования по его целенаправленной химической модификации.
Одним из путей модификации природных метаболитов является озонолиз. нами осуществлен озонолиз диптерокарпола 1 в среде хлористого метилена, ацетона и спиртах при -40ºС без восстановления перекисных продуктов. В результате взаимодействия диптерокарпола 1 с 1 экв. озона в растворе CH2Cl2 получили триснорлактол 2. Взаимодействие соединения 1 c 2 экв. озона в СН2Сl2 привело к образованию смеси триснорлактола 2 и триснорлактона 3, выделенных колоночной хроматографией с выходами 20 и 68%, соответственно.
Реакция диптерокарпола 1 c 2 экв. озона в ацетоне завершилась образованием триснорлактона 3 с выходом 87%. Взаимодействие индивидуального триснорлактола 2 с 1 экв. озона в растворе CH2Cl2 или ацетона приводило к образованию лактона 3 с количественным выходом.
Озонолиз диптерокарпола 1 в метаноле, этаноле или изопропаноле привел к образованию алкоксилактолов 4, 5 или 6 в виде смеси рацематов по С-24 центру. Структура всех соединений подтверждена спектрами ЯМР 1Н и 13С.
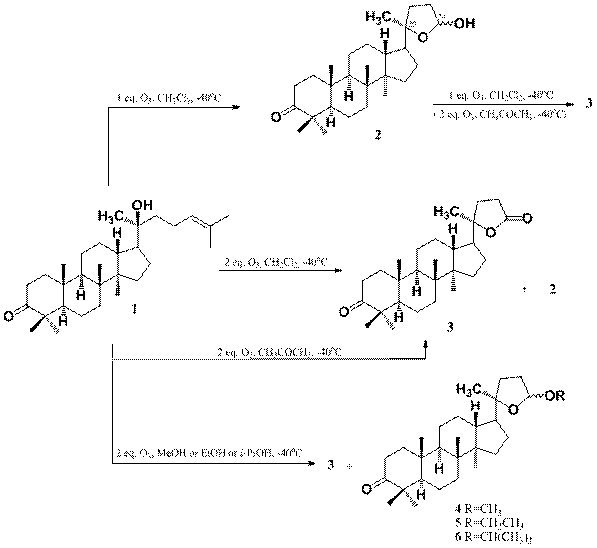
Таким образом, в ходе проведенных реакций наблюдается участие С-20 гидроксигруппы во внутримолекулярной циклизации и взаимодействие с молекулой растворителя по механизму нуклеофильного замещения, что приводит к соединениям с фрагментами лактона, лактола или алкоксилактолов.
Работа выполнена финансовой поддержке гранта РФФИ №.
УДК 378.147:579
, ,
ИССЛЕДОВАНИЕ ВЛИЯНИЯ ПРЕДОБРАБОТКИ ЛИГНОЦЕЛЛЮЛОЗНОГО СЫРЬЯ ГЛИЦЕРИНОМ
НА ЕГО ГИДРОЛИЗ
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Уфимский государственный нефтяной технический университет, г. Уфа
E-mail: *****@***net
Лигноцеллюлозные отходы являются перспективным сырьем для получения практически важных веществ, в том числе биотоплив и биологически активных веществ с помощью микроорганизмов. Вместе с тем гемицеллюлозы и лигнин, содержащиеся в лигноцеллюлозе, являются лимитирующими факторами для ферментативного гидролиза целлюлозы, использующейся микроорганизмами в качестве источника углерода и энергии, поэтому многие исследования направлены на решение вопроса предварительной обработки субстрата для удаления этих нежелательных компонентов без разрушения целлюлозы. Предобработка глицерином, являющимся основным побочным продуктом производства биодизеля, рассматривается как перспективное направление для делигнификации целлюлозного сырья.
В настоящей работе нами исследован гидролиз целлюлозосодержащих субстратов предварительно подвергнутых глицеросольволизу с помощью ферментов и клеток микроорганизмов – продуцентов целлюлаз. Для исследований были использованы коммерческий препарат «Целловиридин Г20Х», используемый в пищевой промышленности и сельском хозяйстве, а также культура Streptomyces sp. К-7 из музея микроорганизмов кафедры БТМП, обладающая высокой КМЦ-целлюлазной активностью. В качестве целлюлозосодержащих субстратов применяли солому и луговые травы.
Было выявлено, что в процессе гидролиза лигноцеллюлозных субстратов с помощью препарата «Целловиридин» при температуре 48°С в течение 5 ч наибольший прирост редуцирующих веществ достигается при гидролизе субстратов, предварительно обработанных глицерином. При использовании соломы, подвергнутой глицеросольволизу выход редуцирующих веществ составил 554 мг/л, тогда как на непредобработанном субстрате - 39 мг/л.
В результате исследования содержания редуцирующих веществ в препаратах 8-ми суточной культуральной жидкости актиномицета Streptomyces sp. К-7 было обнаружено, что в контрольных вариантах (без предобработки субстратов глицерином) их уровень не превышает 54-74 мг/л. В тоже время при использовании в качестве субстрата для культивирования бактерий лигноцеллюлозных отходов, предварительно обработанных водными растворами глицерина, уровень редуцирующих веществ в среде возрастает в 8-11 раз, а КМЦ-целлюлазная активность бактерий увеличивается враза.
УДК 547.36+632.936.2
, ,
СИНТЕЗ ПОЛОВОГО ФЕРОМОНА ФРУКТОВОЙ МОЛИ (ANARSIA LINEATELLA)
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Уфимский государственный нефтяной технический университет, г. Уфа
E-mail: biochem@rusoil.net
(4Е)-Дец-4-ен-1-илацетат (1) идентифицирован как половой феромон фруктовой моли Anarsia lineatella. В литературе описан метод синтеза данного соединения взаимодействием производных эритро-иодгидрина с тетрахлоридом титана в присутствии аллилметилсилана.
Нами изучена возможность получения феромона фруктовой моли Anarsia lineatella на основе промышленно доступного 1,3-дихлорпропена (2) – побочного продукта хлорирования пропилена.
При алкилировании малонового эфира (3) (Е)-1,3-дихлорпропеном (2) с использованием межфазного катализатора и последующим деэтоксикарбоксилированием продукта 4 по методу Крапчо с хорошим выходом образуется этил(4Е)-5-хлоропент-4-еноат (5). Кросс-сочетание эфира 5 с н-пентилмагнийбромидом, катализируемое солями переходных металлов, с высоким выходом приводит к этил(4Е)-дец-4-еноату (6), восстановление которого литийалюминийгидридом и ацетилирование образующегося спирта 7 дает требуемый феромон 1.
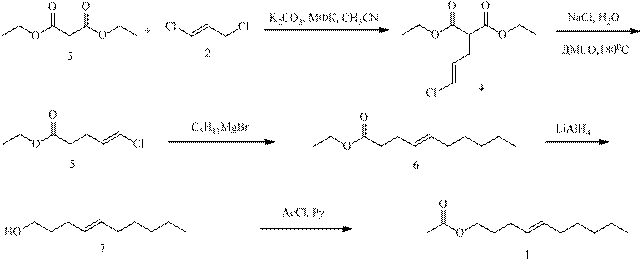
Строение и стереохимическая чистота полученных соединений подтверждена ГЖХ-анализом с использованием капиллярной колонки, данными ЯМР-спектроскопии и масс-спектрометрии.
УДК 542.943;547.532
,
ИК-СПЕКТРОСКОПИЧЕСКОЕ
ИССЛЕДОВАНИЕ ВАНАДИЙСОДЕРЖАЩИХ КАТАЛИЗАТОРОВ
АО «Институт органического катализа и электрохимии им. », г. Алматы
Е-mail: *****@***ru
Методом ИК-спектроскопии аммиака были исследованы кислотные характеристики модифицированных ванадийсодержащих катализаторов. В качестве объектов исследования были выбраны 20%V2О5/TiO2, 20%V2О5-5%МоО3/TiO2 и 20%V2О5-5%МоО3-2%Р2О5/TiO2 катализаторы селективного окисления бензола в малеиновый ангидрид.
Аммиак, благодаря своей сильной основности, может взаимодействовать достаточно быстро даже со слабыми кислыми центрами. Кроме того, он обладает малым размером молекулы, термически устойчив и не склонен к побочным реакциям. Эти свойства отличают его от других адсорбатов [1].
Исследование адсорбции аммиака методом ИК-спектроскопии позволило выявить и идентифицировать кислотные центры ванадийсодержащих катализаторах.
Полученные результаты показали, что аммиак, адсорбированный на ванадийсодержащих катализаторах может существовать в виде двух основных форм: координационно-связанного с льюисовскими кислотными центрами (л. к.ц.) V3+, V4+ или V5+ (п. п. 1250, 1300 и 1620 см-1) и в виде иона NH4+ на бренстендовских кислотных центрах (б. к.ц.) (см-1). Введение модифицирующих добавок (оксиды Мо и P) в состав 20%V2О5/TiO2 катализатора способствует росту интенсивности п. п. в ИК спектрах и по данным термодесорбции [2] приводит к увеличению содержания адсорбированного аммиака. Эти данные могут свидетельствовать об увеличении количества кислотных центров на поверхности катализаторов.
На ванадийсодержащем катализаторе модифицированный фосфором, в отличие от других ванадиевых катализаторов при окислении бензола достигнут наибольший выход (73%) малеинового ангидрида [3]. Это связанно с тем, что фосфор увеличивает содержания как л. к.ц.,так. и б. к.ц. и тем самым повышает селективность и активность катализатора в реакции окисления бензола в малеиновый ангидрид.
Список литературы:
1 Паукштис спектроскопия в гетерогенном кислотно-основном катализе.-Новосибирск :Наука, 1992.-253с.
2 , Асилова -химические методы исследования ванадий-молибденовых катализаторов селективного окисления аренов // 1-я Всероссийская научн. конфер. «Методы исследования состава и структуры функциональных материалов».-Новосибирск, 11-16 октября 2009.-С.233
3 , Ергазиева окисление бензола до малеинового ангидрида на ванадийсодержащих катализаторах //Известия НАН РК, сер. хим.- 2006.
УДК 541.64
ИССЛЕДОВАНИЕ ЗАКОНОМЕРНОСТЕЙ ФЕРМЕНТАТИВНОЙ ДЕСТРУКЦИИ ПЛЕНОК ХИТОЗАНА С ВКЛЮЧЕННЫМИ АНТИБИОТИКАМИ МЕТОДОМ ВИСКОЗИМЕТРИИ
Башкирский государственный университет, г. Уфа
e-mail: tuktarova_irina@rambler.ru
Полимер природного происхождения хитозан (ХТЗ) может быть использован в качестве пленочных покрытий для защиты и лечения хирургических ран и ожогов. Одним из немаловажных преимуществ покрытий на основе ХТЗ является их способность к ферментативной деструкции под действием ферментов, выделяемых раневой поверхностью.
В настоящей работе были изучены пленочные полимерные покрытия на основе ХТЗ и двух антибиотиков – натриевой соли цефазолина (ЦФЗ) - и амикацина сульфата (АМК). Пленки ХТЗ были получены методом полива раствора полимера на поверхность стекла. В ходе эксперимента при получении солевых форм ХТЗ варьировалась природа аниона, что позволяло существенно изменять скорость растворения пленок в воде.
Для моделирования процесса ферментативной деструкции пленочного образца ХТЗ на раневой поверхности, пленку помещали на подложку, смоченную раствором ферментного препарата «Лираза», и выдерживали при температуре 36ºС в течение 1 часа. Степень ферментативной деструкции определяли по данным вискозиметрии в буферном растворе.
В ходе выполняемых исследований были установлено, что введение лекарственного препарата сопровождается существенным уменьшением размеров макромолекулярного клубка ХТЗ. Как следствие этого, собственно хитозановая пленка (без антибиотика) подвергается ферментативной деструкции быстрее, нежели пленки, с включенным внутрь нее антибиотиками. При этом, природа аниона сказывается как на размере макромолекулы ХТЗ, так и на скорости ферментативной деструкции. Установлено, что существует корреляция между скоростью растворения пленок и скоростью ее ферментативной деструкции.
Таким образом, можно утверждать, что введение лекарственных препаратов уменьшает размер клубка и, как следствие, доступность ХТЗ для взаимодействия с ферментным препаратом. В результате этого наблюдается уменьшение скорости ферментативной деструкции ХТЗ в пленке в присутствии лекарственных препаратов-антибиотиков по сравнению со скоростью ферментативной деструкции нативной хитозановой пленки. Следовательно, можно сделать вывод, что на раневой поверхности такие пленки прослужат дольше.
Работа выполнена при финансовой поддержке гранта РФФИ № р_поволжье_а
УДК 622.276
,
ВЛИЯНИЕ ТЕХНОГЕННОГО ЗАГРЯЗНЕНИЯ
НА ФЕРМЕНТАТИВНУЮ АКТИВНОСТЬ ПОЧВ
Башкирский государственный университет, г. Уфа
e-mail: farkhad_m60@mail.ru
Как известно, локальные загрязнения почвы связаны чаще всего с разливами нефти и нефтепродуктов при повреждении трубопроводов и их утечках через неплотности в оборудовании. Загрязнение больших площадей возможно при фонтанировании нефти. Нефть, попадая в почву, опускается вертикально вниз под влиянием гравитационных сил и распространяется вширь под действием поверхностных и капиллярных сил [1, с. 25]. Скорость продвижения нефти зависит от ее свойств, грунта и соотношения нефти, воздуха и воды в многофазной движущейся системе. Первостепенное значение при этом имеют тип нефти, ее количество, характер нефтяного загрязнения. Чем меньше доля нефти в такой системе, тем труднее ее фильтрация (миграция) в грунте. В ходе этих процессов насыщенность грунта нефтью (при отсутствии новых поступлений) непрерывно снижается. При содержании в грунте 10-12 % (уровень остаточного насыщения) нефть становится неподвижной (Ривкин 2007).
Движение прекращается также при достижении нефтью уровня грунтовых вод. Нефть начинает перемещаться в направлении уклона поверхности грунтовых вод. Для предотвращения миграции разлитой нефти бурят серию скважин и извлекают загрязненные грунтовые воды. В некоторых случаях на пути движения грунтовых вод ставится водонепроницаемый барьер (резиновые гидроизолирующие мембраны). Нефть, скопившаяся около барьера, удаляется при помощи специального оборудования. Проявление капиллярных сил хорошо прослеживается при значительной проницаемости и пористости грунта.
Одними из наиболее опасных промышленных отходов являются фенолы, которые попадают в окружающую среду в районах действия нефтехимических предприятий. Фенолы оказывают существенное влияние на почвенные ферменты (Киреева 1997): в одних случаях стимулирующее (полифенолоксидаза, пероксидаза), в других - угнетающее (каталаза, дегидрогеназа, протеаза, уреаза). Чувствительность ферментативных реакций позволяет использовать их в качестве биотеста на загрязнение почв фенольными соединениями [2, с. 179, 182].
Распад нефти и нефтяных углеводородов в почве связан с окислительно-восстановительными процессами, происходящими при участии различных ферментов. Уровень активности окислительно-восстановительных ферментов – один из критериев самоочищающейся способности почвы от углеводородов нефти. При загрязнении почвы нефтью активность этих ферментов резко изменяется [3, с.103].
В загрязненных нефтью почвах ингибируется дегидрогеназная активность. Почвенные дегидрогеназы ингибируются в наибольшей степени не самими углеводородами, а продуктами их деградации, которые могут аккумулироваться в почве и длительное время оказывать токсическое влияние, несмотря на снижение в почве содержания углеводородов. Загрязнение почв нефтью стимулирует активность оксидоредуктаз, участвующих в процессах гумусонакопления в почве. Значительно снижается активность окислительно-восстановительных ферментов азотного обмена (нитрит - и нитратредуктаз) [3, с. 104].
Загрязнение нефтью, обусловливая микробную сукцессию, определенным образом влияет на биохимические процессы почв, меняя ее ферментативную активность. Низкие концентрации нефти могут стимулировать биологическую активность почвы, а повышенные дозы загрязнения приводит к снижению этого показателя. Полученные данные по активности различных ферментов свидетельствует о возможности применения метода ферментативных реакций для биодиагностики и индикации различных типов почв.
Список литературы:
1 Экологические проблемы нефтедобычи»: Тезисы докладов международной молодежной конференции / отв. ред. . – Уфа: РИЦ БашГУ, 2012.
2 «Экотоксикология»: Материалы Всероссийской молодежной конференции. – Уфа: РИЦ БашГУ, 2012.
3 и др. Экологический менеджмент.- Уфа: РИЦ БашГУ, 2008. – 166 с.
УДК 547.954.681.3.06
, ,
КИНЕТИЧЕСКИЕ ЗАКОНОМЕРНОСТИ РЕАКЦИИ ПОЛИФУНКЦИОНАЛЬНЫХ ОРГАНИЧЕСКИХ КИСЛОТ С ОЗОНОМ
ФГБОУ ВПО «Башкирский государственный университет», г. Уфа
E-mail: xajrullina_1990@mail.ru
Очистка воды от органических соединений всегда являлась актуальной темой. Использование озона в качестве окисляющего агента в процессах очистки воды показало его безопасность с экологической точки зрения, способность глубоко окислять органические вещества, снижать цветность воды, дезинфицировать и улучшать ее вкус и запах. В данной работе были исследованы кинетические закономерности и механизм реакции озона с органическими кислотами в водной среде, что представляет собой существенный практический интерес, так как многие важные процессы с участием О3 (атмосферные процессы, очистка сточных вод) протекают либо в водных растворах, либо в присутствии значительных количеств водяных паров.
За кинетикой процесса следили спектрофотометрически по изменению концентрации О3 в реакционной смеси. В качестве объектов исследования были выбраны масляная, молочная, малоновая, янтарная, яблочная, лимонная и галактуроновая кислоты. Опыты проводили при 40-80ºC. Начальные концентрации кислот [S] в реакционной смеси изменяли в диапазоне (0,1¸1,0)×10–3 моль/л, озона – (3,2¸4,9)×10–4 моль/л. При этом в проводимых экспериментах всегда выполнялось условие: [S]0 >> [O3]0.
Исследования показали, что скорость расходования озона в реакции с полифункциональными кислотами подчиняется следующему кинетическому закону:
υ= k·[S]·[O3],
где k – константа скорости реакции озона с изученными кислотами.
Согласно полученным данным, наблюдается следующий порядок реакционной способности органических кислот по отношению к озону (70ºС): янтарная < масляная < лимонная < малоновая < яблочная < молочная < галактуроновая.
Исследуя зависимость между lgA и Е, выявили линейную корреляцию - компенсационный эффект:
lgA = (3.35 ± 1.30) + (0.58 ± 0.11)×Е,
(коэффициент корреляции r = 0.99).
Приведенная корреляционная зависимость кинетических параметров свидетельствует о едином механизме лимитирующей стадии окисления полифункциональных кислот озоном.
УДК 547.94:834.2
2, 1, 1
СИНТЕЗ 3- И 5-N-ЭТИЛОКСИПРОИЗВОДНЫХ НЕКОТОРЫХ ХИНОЛИЗИДИНОВЫХ АЛКАЛОИДОВ
1 ФГБУН Институт органической химии Уфимского научного центра Российской академии наук, г. Уфа
E-mail: tsipisheva@anrb.ru
2 ГОУ ВПО «Башкирский государственный университет», г. Уфа
Известно, что 12-N-этилоксипроизводное хинолизидинового алкалоида
(-)-цитизина обладает высокой антиаритмической активностью [1]. С целью изучения взаимосвязи «структура – антиаритмическая активность» получены производные метилцитизина 2 и термопсина 3 с N-этилоксифрагментом в
2-пиридоновом ядре. Синтез целевых соединений был осуществлен путем сочетания соответствующих галоидпроизводных с моноэтаноламином в присутствии соли одновалентной меди.

Реагенты и условия: а) MeI, K2CO3, ацетон, 56 oC; б) KBr, H2O2, H2SO4, 20 oC; c) моноэтаноламин, CuCl, KOH, 90 oC.
Соответствующие 3-, 5-бром и 3,5-дибромпроизводные общих формул 4 и 5, получены согласно [2] и разделены методом колоночной хроматографии на SiO2. Последующие стадии сочетания с моноэтаноламином в указанных условиях привели к соответствующим N-этилоксипроизводным 6 и 7 с выходами от 43 до 61%.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 |




