Рисунок 3 – Результаты определения всхожести проростков кресс-салата (в мм) при концентрациях нефти 1-10 % масс. в опыте №2
Средняя длина надземной части проростков. Контроль недостоверно отличается от концентрации 1% масс. При 3 % масс. и 5 % масс. резко возрастает изменчивость между отдельными повторностями. При 5 % масс. концентрации достоверны отличия от контроля.
Средняя длина подземной части проростков. При концентрации 1 % масс. нет достоверных различий ни с остальными концентрациями, ни с контролем. При 3 % масс. и 4 % масс. достоверны различия с контролем. При 5 % масс. концентрации достоверны различия с 4 % масс. При 7 % масс. и 10 % масс. всхожесть нулевая, поэтому различия по средней длине определить невозможно.
Результаты измерения среднего сухого веса проростков в опыте №2 представлены на рисунке 4.

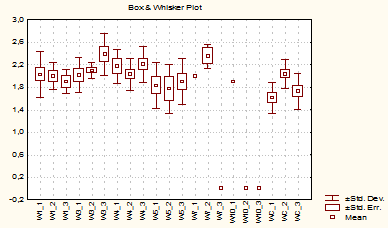
Рисунок 4 –Результаты измерения среднего сухого веса проростков кресс-салата (в мм) при концентрациях нефти 1-10 % масс. в опыте №2
Средний сухой вес проростков при концентрации 1 % масс. достоверно отличается от данного показателя при концентрации нефти 3 % масс. При концентрации 4 % масс. сухой вес достоверно отличается от контроля. При концентрации 5 % масс. достоверные различия с другими анализируемыми параметрами отсутствуют. При 7 % масс. и 10 % масс. концентрации количество анализируемых проростков равно нулю.
У всех анализируемых параметров в опыте №2 выявлена достоверная обратная зависимость с уровнем концентрации нефти в почве (таблица 1).
Таблица 1 – Зависимость анализируемых параметров от содержания нефти в почве
Анализируемый параметр | Величина коэффициента корреляции | |
Опыт №1 | Опыт №2 | |
Всхожесть, % | -0,21 | - 0,76 |
Средняя длина надземной части проростков, мм | 0,006 | - 0,85 |
Средняя длина подземной части проростков, мм | 0,22 | - 0,79 |
Общая средняя длина проростков, мм | 0,33 | - 0,83 |
Средний сухой вес проростков, мг | -0,19 | - 0,62 |
Указанный экспресс-метод позволяет получить достаточно надежные данные о токсичности конкретной пробы.
Список использованной литературы
1 , , и др. Химический состав нефтей Западной Сибири, – Новосибирск: Наука, 19с.
2 , Тагасов и нефтепродукты в окружающей среде, - М.: Изд-во РУДН, 20с.
3 Зейферт кресс-салата как тест-объекта при оценке токсичности природных и сточных вод Стерлитамакского промузла. «Башкирский экологический вестник», 2010, № 2. – С. 39-50.
УДК 6
, , .
ЭФФЕКТИВНОЕ СРЕДСТВО ДЛЯ ПРОТРАВЛИВАНИЯ СЕМЯН
ГБУ РБ «Научно-исследовательский технологический институт гербицидов и регуляторов роста растений АН РБ», г. Уфа
Нами разработана рецептура и технология получения препарата Тебуконазол (ТБК, раксил), 60 г/л, к. с. – протравителя семян с/х культур против комплекса возбудителей болезней, развивающихся на различных видах сельскохозяйственных растений. Препарат стабилен при хранении, легко суспендируется в воде. Рабочий раствор препарата стабилен в течение 3-4 часов.
Таблица – Фунгицидная активность тебуконазола (60 г/л, к. с.) и препарата Дозор (60 г/л, к. с.) на семенах яровой пшеницы.
Препарат | Норма расхода препа- рата по д. в., гр/т. | Удержи- ваемость на семе- нах, % | Лабора- торная всхо- жесть, % | Корневые гнили | Мукор | Вес 100 про- рост- ков, гр. | |
поражен- ность, % | эффек- тивность, % | ||||||
Контроль «Дозор» прототип ТБК, обр.1 ТБК, обр.2 | - 30,0 30,0 30,0 | - 91 96 94 | 77,0 74,0 71,0 74,0 | 40,2 5,4 5,3 1,5 | - 86,6 86,1 96,3 | +++ - + - | 10,1 11,2 10, 7 11,3 |
Представленные в таблице результаты биологических испытаний препарата Раксил (60 г/л, к. с.) не уступают по своим характеристикам известному препарату Дозор (60 г/л, к. с.).
УДК 547.368+547.551+547.8
1, 1, 1,2
КАТАЛИТИЧЕСКОЕ ГИДРОАМИНИРОВАНИЕ ДИВИНИЛ - И ДИАЛЛИЛСУЛЬФИДОВ МОНОЭТАНОЛАМИНОМ
ФГБОУ БашГУ, Инженерный факультет, г. Уфа,
ФГБУН ИНК РАН, г. Уфа
E-mail: vnirara@mail.ru
С целью синтеза сера- азотсодержащих гетероциклов, проявляющих свойства комплексообразователей редкоземельных и благородных металлов и специфических биорегуляторов, нами изучено взаимодействие анилина и моноэтаноламина с дивинил - и диаллилсульфидами в присутствии различных катализаторов.
Исходные реагенты дивинил - (1) и диаллил (2)- сульфиды являются весьма доступными соединениями. Их синтезы базируются на использовании отечественных реагентов, а именно реакциями винил - и аллилгалогенидов с Na2S.
| Следует добавить, что применение в синтезе гетероциклов соединений серы, таких как H2S и Na2S актуально для развития комплексных способов утилизации техногенного H2S, образующегося в огромных масштабах |
при гидроочистке сернистой нефти и газоконденсатов.
Среди изученных нами каталитических систем на основе металлокомплексных катализаторов Ni(acac)2-Et3Al-Ph3P; Ni(acac)2-Et3Al; PdCl2-BuONa; PdCl2-Et3Al-Ph3P, PdCl2-CF3COOH-Ph3P, а также H2SO4 и I2, эффективными оказались Ni(acac)2-Et3Al и PdCl2-BuONa и PdCl2-CF3COOH-Ph3P ([М]).
Установили, что каталитическое гидроаминирование диалкенов 1 и 2 осуществляется по двум направлениям: происходит образование анти - Марковниковских продуктов гидроаминирования 3,5 и окислительного гидроаминирования с образованием сера - и азотсодержащих гетероциклов 4,6.
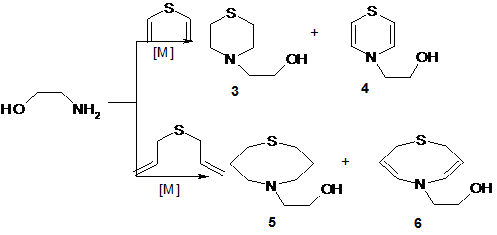
Отметим, что преимущественной стадией является анти- Маркониковское присоединение с образованием тиоморфолина 3 и 1-тио-5-азацината 5. Строение гетероциклов 3-6 установлены методами ИК-, ЯМР-спектроскопией и масс-спектрометрией.
Список литературы:
1 , Благородные, редкоземельные и цветные металлы в железо-марганцевых корках Японского моря // Дан. 2008. т. 422. № 4. с. 522-527.
2 , , и др. // Координационная химия. 2001. Т.27. С.12.
УДК 620.92
, ,
ПОЛУЧЕНИЕ БИОЭТАНОЛА ИЗ СУЛЬФИТНЫХ ЩЕЛОКОВ
Казанский национальный исследовательский технологический университет
E-mail: *****@***ru
Для производства биоэтанола предназначенного для добавления в бензин или потребления в чистом виде, традиционно применяют следующие виды сырья: Бразилия – сахарный тростник, США – кукуруза, Европа – злаковые. В России сырьём могут стать древесные отходы и отходы целлюлозно-бумажной промышленности [1].
При варке на каждую тонну полученной целлюлозы приходится 6,5-8 м3 сульфитного щелока. Щелок, отделяемый после варки, содержит 90-100 кг/м3 органических веществ. Из них около половины составляют лигносульфоновые кислоты, 25-35% редуцирующие вещества, т. е. сумма сахаров и других веществ, имеющих карбонильную группу. В составе редуцирующих веществ примерно 80-85 % различных сахаров, образовавшихся при варке вследствие гидролиза гемицеллюлоз и части целлюлозы. Активная кислотность щелока составляет (pH) 1-1,5. В щелоке еще содержится растворенный сернистый ангидрид, а так же соли сернистой кислоты (моносульфит и бисульфит), небольшое количество уксусной кислоты, фурфурола и других соединений. Поэтому сначала щелок подготавливают к биохимической переработке (удаляют SO2, фурфурол и другие летучие соединения), продувая его острым паром и затем охлаждают до 350С. В подготовленный щелок вводят спиртообразующие дрожжи, которые с помощью выделяемого ими фермента зимазы расщепляют гексозные сахара до этилового спирта и двуокиси углерода. Спиртовое брожение осуществляют в бродильном аппарате при 32-350С. Затем на сепараторе от сброженной жидкости действием центробежных сил отделяют дрожжевую суспензию, которую возвращают в головной аппарат. Оставшуюся жидкость, содержащую 1-1,3 % этилового спирта и в качестве примеси небольшое количество метилового спирта, альдегидов, эфиров направляют в бражную колонну, где из нее отгоняют острым паром спиртовую фракцию. Конденсат, выводимый из конденсатора бражной колонны и содержащий около 20 % этилового спирта, ректифицируют в колонне для отделения некоторого количества примесей. Полученный продукт повторно ректифицируют в спиртовой колонне для доведения массовой доли этилового спирта до 95-96%. Двуокись углерода выделяется и отводится в газгольдеры. После её очищают и применяют для газирования напитков, зарядки огнетушителей, как сухой лед и т. д. Выход товарного этилового спирта составляет около 90 л на 1 т выработанной целлюлозы нормального выхода [2,3].
Список литературы:
1 Инновационное развитие альтернативной энергетики: науч. изд. – Ч.1. – М.:ФГНУ «Росинформагротех», 2010. – 348 с.
2 Авербух, А. Я., «Что делает химия из древесины». /, . – М: Лесная промышленность, 1970. –167 с.
3 Ковернинский, И. Н. «Основы технологии химической переработки древесины». /. – М: Лесная промышленность, 1984.-184 с.
УДК 632.93:631.53.01
ВЛИЯНИЕ БИОУДОБРЕНИЯ «АЗОЛЕН» НА ПОВЫШЕНИЕ УСТОЙЧИВОСТИ РАСТЕНИЙ К АБИОТИЧЕСКИМ СТРЕССАМ
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования Уфимский государственный нефтяной технический университет, г. Уфа
E-mail: nastenka140890@mail.ru
Для защиты растений от болезней наряду с химическими фунгицидами широко используются биопрепараты на основе живых культур микроорганизмов [1]. Эти препараты часто называют биофунгицидами благодаря способности используемых в качестве их основы микроорганизмов непосредственно подавлять развитие фитопатогенных грибов, проявляя антагонизм [1-3]. В основе биоудобрения «Азолен» культуральная жидкость штамма Azotobacter vinelandii ИБ 4 (титр 4-8 · 109 КОЕ/мл). Готовый препарат представляет собой водную суспензию жизнеспособных клеток штамма и компонентов питательной среды от бесцветной до цвета слоновой кости со слабым специфическим запахом, свойственным микробным препаратам. Биоудобрение «Азолен» повышает всхожесть семян, снижает развитие болезней сельхозкультур, улучшает показатели фитосанитарного состояния посевов, способствуя развитию и повышению урожайности выращиваемых культур [4].
Не исключено, что биоудобрение «Азолен» может повышать устойчивость растений и к абиотическим стрессовым факторам. Поэтому целью работы было выявление способности биоудобрения «Азолен» повышать устойчивость растений к действию абиотических стресс-факторов.
В данной работе объектом исследований служили трехсуточные проростки озимой пшеницы Безенчукская 380 . Семена перед посевом стерилизовали 96%-ным этанолом в течение трех минут, тщательно промывали дистиллированной водой и обрабатывали культуральной жидкостью клеток. Зерновки проращивали в чашках Петри. В экспериментах измеряли длину колеоптиля и главного корня.
В экспериментах с засолением среды в контроле неинокулированные и обработанные бактерией проростки пересаживали в чашки Петри на раствор 1%-ной сахарозы, в опыте - на ту же среду, дополнительно содержащую 1% NaCl. В опыте с действием дефицита влаги проростки высаживали на 10%-ный раствор поли этиленгликоля (ПЭГ, молекулярная масса 6000) в 0,5%-ном растворе сахарозы, контрольные проростки находились на растворе сахарозы.
При засолении среды торможение роста корня у неинокулированных растений было примерно в 2,5 раза сильнее, чем у инокулированных. Инокулированные «Азоленом» проростки быстрее преодолевали кратковременное воздействие водного дефицита; корни неинокулированных проростков не росли даже через 48 часов опыта, тогда как обработанные проростки проявили способность к росту через 20 часов после стресса. Темпы роста корня и колеоптиля обработанных «Азоленом» растений оставались более высокими, в сравнении с необработанными (7,7% и 13,8%, 2,8% и 11% соответственно).
Так как при действии различных стресс - факторов растения могут включать одни и те же сигнальные пути и активировать одинаковые классы защитных белков, неудивительно, что инокуляция растений бактерией Azotobacter vinelandii ИБ 4 повышает также их устойчивость к хлоридному засолению среды, а также к дефициту влаги, имитированному ПЭГ.
Список литературы:
1. , , и др. Роль бактерий-антагонистов фитопатогенов в защите сельскохозяйственных растений от болезней.- Уфа: Гилем, 2001.- 66с.
2. в., , Томилова в защите растений: Учебное пособие.- Новосибирск: Новосиб. гос. аграр. Ун-т, 200с.
3. стратегические задачи исследований по обеспечению фитосанитарного оздоровления агроэкосистем в условиях адаптивно-ландшафтного земледелия// Фитосанитарное оздоровление экосистем (материалы II Всероссийского съезда по защите растений).- С.-Пб.- Пушкин,2005.-Том 2.-594с.
4., , и др. Микробиологические препараты Елена, Азолен, Ленойл для сельского хозяйства и экологии: Монография.- Уфа, 20с.
УДК 615.36:547.
1, 1,2, 2
ИЗУЧЕНИЕ КОМПЛЕКСООБРАЗОВАНИЯ АРАБИНОГАЛАКТАНА ЛИСТВЕННИЦЫ СИБИРСКОЙ И ЕГО ОКИСЛЕННЫХ ФРАКЦИЙ С ИОДОМ
1Федеральное государственное бюджетное учреждение науки Институт органической химии Уфимского научного центра Российской академии наук, г. Уфа
2Федеральное государственное бюджетное образовательное учреждение Высшего профессионального образования «Башкирский государственный аграрный университет», г. Уфа
E-mail: *****@***ru
В работах [1,2] показано, что лекарственные вещества в сочетании с биогенными полимерами в большинстве случаев более эффективны, чем индивидуальные фармаконы. Использование полимерной матрицы (полисахариды) позволяет увеличить продолжительность действия лекарственного препарата и существенно снизить его токсичность за счет сокращения дозы на курс лечения. Одним из перспективных носителей лекарственных соединений является арабиногалактан лиственницы сибирской (АГ), обладающий высокой водорастворимостью, иммуномодулирующей, противоопухолевой и антиоксидантной активностью [1,2]. В связи с этим актуальным является исследование взаимодействия АГ и его окисленных форм с иодом и получение на их основе новых физиологически активных соединений.
Спектрофотометрическими методами исследована термодинамика комплексообразования систем иод-арабиногалактан, иод-полимерная форма окисленного арабиногалактана и иод-олигомерная форма окисленного арабиногалактана в водных и водно-спиртовых растворах при различных температурах. Синтез комплексов АГ и его окисленных фракций с иодом проводили при комнатной температуре в течение двух часов. Содержание иода в продуктах реакции составило 43-59 %. Выделенные соединения были проанализированы спектрофотометрическими методами.
В электронном спектре изученных комплексов АГ с иодом наблюдаются полосы поглощения при 285 нм и 344 нм, соответствующие колебаниям трииодидных ионов. Согласно данным ИК - спектроскопии в иодсодержащих комплексах происходит увеличение интенсивности, а также смещение полос поглощения валентных колебаний гидроксильных групп на 20 – 30 см-1 (3см-1) и полос поглощения в области 1см-1, соответствующих валентным колебаниям эфирной С-О связи пиранозного и фуранозного циклов, на 10 – 15 см-1 в низкочастотную область.
Установлено, что понижение температуры реакции и повышение полярности растворителя увеличивают устойчивость продуктов реакции. Термодинамические характеристики процесса комплексообразования биополимер – иод указывают, на то, что при взаимодействии компонентов системы не происходит существенных структурных перестроек поли - и олигосахаридов. Показано, что главными активными центрами в АГ и его окисленных формах, участвующими во взаимодействии с иодом, могут быть как гидроксильные группы, так и эфирная связь пиранозного и фуранозного циклов.
Работа выполнена при финансовой поддержке Федеральной целевой программы «Научные и научно-педагогические кадры инновационной России» на г. г. (Заявка 2012-1.2.06-004. Соглашение 8458).
Список литературы:
1 Yamada H., Kiyhara H., Cyong J. C., Otsuka Y. // Carbohydrate. Res. 1987. V.159. N 3. P.275-291.
2 , , // Химия растительного сырья. 2003. № 1. С. 27-44.
УДК 547.394
, ,
СТЕРЕОСЕЛЕКТИВНЫЙ СИНТЕЗ
4-[(2E,4E)-УНдека-2,4-диеноил]морфолина
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования Уфимский государственный нефтяной технический университет, г. Уфа
E-mail: *****@***net
(2E,4E)-Диенамиды обладают фармакологическим, пестицидным, фунгицидным действием, а также используются при создании лекарственных средств и препаратов сельскохозяйственного назначения. Часто в их структуру входят пиперидиновые и пирролидиновые фрагменты.
Нами исследована возможность стереонаправленного синтеза синтетического аналога природных (2Е,4Е)-диенамидов – 4-[(2E,4E)-ундека-2,4-диеноил]морфолина (1) на основе реакции сочетания метилакрилата с (1E)-1-иодокт-1-еном (2).
Установлено, что сочетание винилиодида (2), полученного гидроалюминированием-иодированием 1-октина (3), с метилакрилатом (4) в присутствии Pd(OAc)2, K2CO3 и тетрабутиламмонийхлорида с высоким выходом приводит к метиловому эфиру (2Е,4Е)-ундека-2,4-диеновой кислоты (5). Стереохимическая чистота сложного эфира (5) подтверждена ГЖХ анализом, а также данными спектров ЯМР 1H и 13С. КССВ винильного атома водорода при атоме С2 составляет 15.2 Гц, что свидетельствует о трансоидной конфигурации двойной связи.
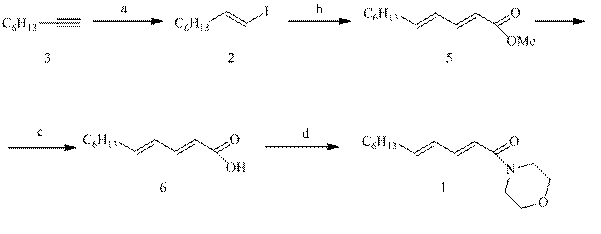
а. ДИБАГ, I2; b. метилакрилат (4), Pd(OAc)2, Bu4NCl, K2CO3; c. KOH, EtOH; d. SOCl2, морфолин
Завершающие стадии – гидролиз сложного эфира (5) с образованием (2Е,4Е)-ундека-2,4-диеновой кислоты (6), трансформация ее в хлорангидрид и амидирование последнего морфолином приводят к требуемому соединению (1) с общим выходом 47% на исходный винилиодид (2).
УДК 579.61+547.394
, ,
ОПРЕДЕЛЕНИЕ АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТИ САРМЕНТИНА И ПЕЛЛИТОРИНА
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования Уфимский государственный нефтяной технический университет, г. Уфа
E-mail: *****@***net
Пеллиторин – (2E,4E)-N-изобутилдека-2,4-диенамид, выделенный из различных видов Piperaceae [1], является хорошо известным природным инсектицидом [1,2] и обладает противораковой [3], противотуберкулезной, анальгетической, антибактериальной и противогрибковой активностью [1, 4-6].
Сарментин – 1-[(2E,4E)-дека-2,4-диеноил]пирролидин, впервые выделенный из плодов Piper sarmentosum [7], проявляет седативное, анальгетическое и антибактериальное действие [1]. Относительно недавно было обнаружено, что сарментин обладает противотуберкулезной и антиплазмодиальной активностью [6].
Определение антибактериальной активности сводилось к выявлению роста исследуемых микробных культур на чашках Петри с питательной средой, на поверхность которой помещены бумажные диски, обработанные разными концентрациями тестируемых соединений (согласно оптимизированной методике [8]).
Готовую агаризованную питательную среду (40 г) суспендировали в дистиллированной воде (1 л) и перемешивали до полного растворения. Среду и чашки Петри автоклавировали при давлении 1,12 кгс/cм2 в течение 45 мин. После застывания среды в чашках Петри, инокулировали 0,05 мл 24 часовой культуры тестируемых организмов. В каждую чашку помещали бумажные диски (диаметр 10 мм), пропитанные исследуемым раствором с различными концентрациями. Обработанные чашки инкубировали при 32оС в течении 48 ч и затем определяли зону подавления. Проводили три повторных опыта для каждой концентрации исследуемого соединения. Результаты испытаний представлены в таблицах 1,2.
Таблица 1 – Оценка антибактериальной активности 1-[(2E,4E)-дека-2,4-диеноил]пирролидина (сарментина)
Микроорганизм | Концентрация испытуемого образца | |||
100 мкг/мл | 50 мкг/мл | 25 мкг/мл | 12.5 мкг/мл | |
Диаметр зон подавления роста образцами, мм | ||||
Bacillus subtilis | 24 | 20 | 17 | 10 |
Micrococcus luteus | 16 | 13 | 12 | 0 |
Pseudomonas putida | 12 | 10 | 10 | 0 |
Таблица 2 – Оценка антибактериальной активности (2E,4E)-N-изобутилдека-2,4-диенамида (пеллиторина)
Микроорганизм | Концентрация испытуемого образца | |||
100 мкг/мл | 50 мкг/мл | 25 мкг/мл | 12.5 мкг/мл | |
Диаметр зон подавления роста образцами, мм | ||||
Bacillus subtilis | 21 | 17 | 15 | 10 |
Micrococcus luteus | 17 | 14 | 10 | 0 |
Pseudomonas putida | 11 | 10 | 0 | 0 |
Высокую ингибирующую активность в отношении грамвариабельных бактерий (Bacillus subtilis) показал как сарментин, так и пеллиторин (диаметр зон подавления роста 15-17 мм при концентрации образцов 25 мкг/мл). Оба испытуемых соединения проявили среднюю способность к ингибированию роста грамположительных бактерий (Micrococcus luteus), в то время как в отношении грамотрицательных Pseudomonas putida наблюдается лишь умеренное подавление роста и только при высоких концентрациях тестируемых соединений.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 |