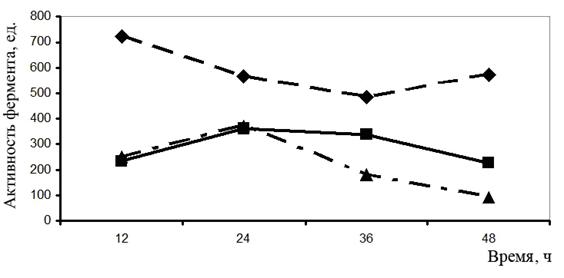
Рисунок 1 - Активность протеаз штаммов: ![]() - B. subtilis 49РН,
- B. subtilis 49РН,  - B. subtilis 26Д,
- B. subtilis 26Д, ![]() - B. subtilis 11В
- B. subtilis 11В
Список литературы:
1 Тарасюк и перспективы применения биополимеров в пищевой промышленности // Консервная промышленность сегодня: технологии, маркетинг и финансы. – 2011. – № 3. – С. 55-62.
2 Хазиев почвенной энзимологии // М.: Наука, 2005. – 252 с.
3 Extracellular proteases produced by the Quorn myco-protein fungus Fusarium graminearum in batch and chemostat culture / A. M. Griffen [et al.] // Microbiology. – 1997. – Vol. 143. – P. 3007–3013.
Работа выполнена при финансовой поддержке Федеральной целевой программы «Научные и научно-педагогические кадры инновационной России» на г. г. (Заявка 2012-1.2.06-004, Соглашение 8458).
УДК 547.541.1
,
ПОЛУЧЕНИЕ ПРОИЗВОДНОГО 2-(1-ГИДРОКСИЭТИЛ)ИНДОЛИНА
Институт органической химии УНЦ РАН, г. Уфа
E-mail:gataullin@anrb.ru
Известно, что некоторые 2-(1-гидроксиалки)индолы являются мощными агонистами SARM, модуляторами андрогенных рецепторов. В исследованиях эти соединения предотвращали рост опухоли простаты, разрушение кости и потерю массы тела после операций. Поэтому привлекают внимание исследователей.
С целью получения производного 2-(1-гидроксиэтил)индолина через реакцию непосредственного нуклеофильного замещения иода индолин 1 нагревали с KOH в ДМФА. Основным продуктом реакции оказалось этилиденовое производное 2, соотношение которого с винильным изомером 3 составляет ≈ 100:35. Доля 2-(1-гидроксиэтил)-замещенного индолина 4 не превышает 10%.
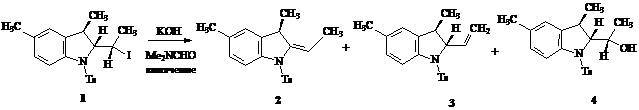
Кипячение йодэтилиндолинов 1а, б в ДМФА в течение 5 ч дает эфир муравьиной кислоты 5а, б.
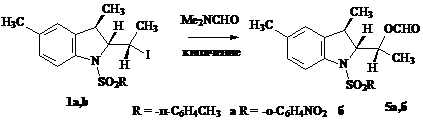
Формиатную группу удаляли выдерживанием эфира 5а в этанольном растворе щелочи.
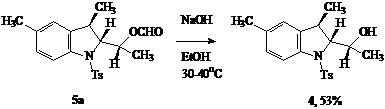
УДК 547.57
, ,
СИНТЕЗ 2-МЕТИЛ-2-(4’-МЕТИЛСУЛЬФАМИДОФЕНИЛ)-
1,3-ДИОКСОЛАНА
Уфимский государственный нефтяной технический университет, г. Уфа
E-mail: bio2@rusoil.net
2-Метил-2-(4’-метилсульфамидофенил)-1,3-диоксолан является промежуточным соединением в синтезе соталола – безопасного и эффективного антиаритмического лекарственного препарата III класса с регулируемой блокадой β-адренергических рецепторов.
Нами оптимизирован метод синтеза 2-метил-2-(4’-метилсульфамидофенил)-1,3-диоксолана путем интенсификации отдельных стадий синтеза микроволновым излучением.
На первой стадии осуществляли ацетализацию 4-нитроацетофенона (1) этиленгликолем в присутствии кислотного катализатора и толуола в качестве водовыносителя при температуре кипения реакционной смеси и соотношении реагентов, равном 1 : 2.

1 2
Установлено, что по сравнению с конвекционным нагревом, микроволновое излучение мощностью 200 Вт увеличивает выход 2-метил-2-(4’-нитрофенил)-1,3-диоксолана (2) и сокращает время синтеза в 2 раза.
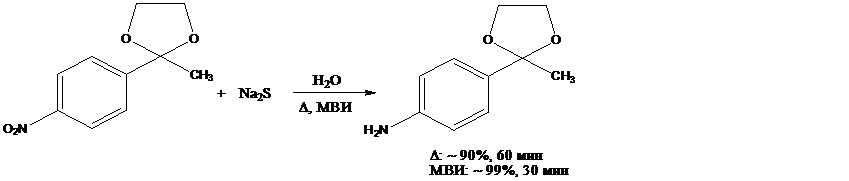
2 3
Восстановление нитродиоксолана (2) до аминодиоксолана (3) в условиях микроволнового нагрева протекает с количественным выходом и в 2 раза быстрее, чем при конвекционном нагреве.
Взаимодействие аминодиоксолана (3) с метилсульфохлоридом при пониженной температуре в пиридине приводит к 2-метил-2-(4’-метилсульфамидофенил)-1,3-диоксолану (4) с выходом 70%.
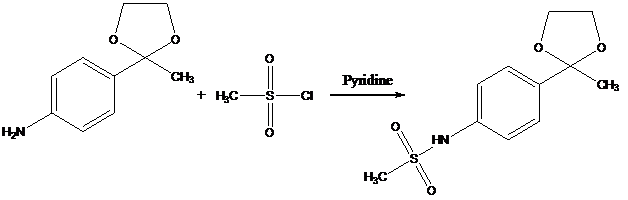
3 4
Строение полученных соединений доказано методами спектроскопии ЯМР 1H и 13C.
УДК 547.458.88
1, 1, 2, 1
ПОЛУЧЕНИЕ БАКТЕРИЦИДНЫХ ПЛЕНОК И ПОРОШКОВ НА ОСНОВЕ КОМПЛЕКСОВ ЯБЛОЧНОГО ПЕКТИНА И ЙОДА
1 ФГБОУ ВПО Башкирский государственный университет, Инженерный факультет, г. Уфа
2Институт органической химии УНЦ РАН, г. Уфа
E-mail: Levkoteya@yandex.ru
Особенности химической и пространственной структуры пектина определяют его способность к формированию специфических комплексов с различными молекулами. Комплексование биополимеров с йодом, обладающим уникальным спектром бактерицидной активности, позволяет уменьшить токсичность йода, сохраняя при этом его антимикробное действие, а введение лекарственного вещества усиливает фармакологические свойства. Поэтому особую актуальность имеет разработка биологически активных субстанций, способных усиливать терапевтический эффект лекарственных средств и пролонгировать их действие.
Нами получены различные формы тройных комплексов – допированные тонкие пленки и тонкодисперсные порошки. Использовано два подхода к их получению. Первый – это насыщение пленок и порошков парами йода при комнатной температуре, при этом происходит постепенное увеличение массы образцов. Насыщение порошка пектина йодом происходит в течение 5 суток, тогда как для пленки достаточно 4 суток. Быстрее всего насыщение йодом наблюдается для порошков пектинов в виде комплексов с органическими молекулами. Дольше всего процесс протекает при использовании пленочного образца исходного пектина. Такое поведение исследуемых полимерных соединений при допировании, скорее всего, связано с различной надмолекулярной организацией и плотностью упаковки полисахарида. Диффузия молекул йода может протекать значительно легче при допировании комплекса, чем исходного полимера. Согласно данным ИК-спектроскопии, в спектрах комплексов пектин – йод, полученных жидкофазным способом, наблюдается исчезновение плеча и уширение полосы поглощения валентных колебаний гидроксильных групп в области см-1. Кроме того, происходит резкое увеличение интенсивности колебания полосы поглощения в области 1734 см-1 , соответствующей валентным колебаниям карбонильных групп и ее низкочастотный сдвиг на 16 см-1 . Это может являться прямым следствием понижения силовых констант этой связи, которое обусловлено переходом электрона от донора к акцептору. Полосы 773, 840 и 916 см-1 могут быть отнесены к внешним деформационным колебаниям СН2- и СН- групп и пульсационным колебаниям пиронозных колец. Из ИК - спектров комплексов можно сделать вывод, что главными активными центрами в пектине, участвующими во взаимодействии с йодом могут быть как гидроксильные группы так и С=О связь карбонильных групп. Для комплекса пектина с йодом, полученного твердофазным способом, в области 3200 – 3400 см-1 наблюдается смещение в длинноволновую область валентных колебаний гидроксильных групп на 4 см-1, происходит низкочастотный сдвиг полосы при 1743 см-1 на 11 см-1. Кроме того, наиболее сильно изменяется характер колебаний полос в области 720 – 920 см-1. В этой области наблюдается исчезновение сигнала при 773 см-1, что может говорить об изменении конформации макромолекулы при взаимодействии с йодом. Таким образом, на основании ИК-спектров можно предположить, что при жидкофазном способе синтеза образуются «внешние» комплексы, тогда как при твердофазном, скорее всего, происходит образование «внутренних» комплексов. Более жесткие условия, используемые при твердофазном способе синтеза, способствуют образованию полииодидных цепей, вокруг которых происходит определенная ориентация полисахаридных молекул. При твердофазном синтезе порошкообразных йодсодержащих комплексов при высокой температуре были получены очень устойчивые йодсодержащие порошки. Содержание йода в них контролировалось методом титрования и остается постоянным в течение нескольких месяцев. Очевидно, во взаимодействии с йодом в этом случае принимают участие не только карбонильные и гидроксильные группы полимеров, но и непосредственно гликозидные связи, что следует из данных ИК-спектроскопии.
При создании лекарственных полимерных пленок, важную роль имеет высвобождение фармакофоров из полимерной матрицы. Изучены свойства пленок комплексов, в том числе, кинетические закономерности выхода йода из образца. Полное высвобождение йода из пектиновой пленки наблюдается уже через 25-30 минут, тогда как из пленки комплекса пектина с никотиновой кислотой за 90-100 минут, а из пленки комплекса пектина с 5-аминосалициловой кислотой за 180 минут. То есть, полимерная матрица на основе комплекса пектина с никотиновой и 5-аминосалициловой кислотами более прочно удерживает йод, что коррелирует с константами устойчивости данных соединений.
При изучении электропроводящих свойств пленок полимерных комплексов установлено, что допированные йодом полимерные образцы обладают большей электропроводностью по сравнению с исходными соединениями.
Таким образом, введением йода в комплекс возможно получение бактерицидных полимерных комплексов с пролонгированным действием, причем молекулы йода не способны диффундировать во всю толщину образцов при мягких условиях, а более жесткие условия реакции способствуют образованию устойчивых полииодидов, но приводят к деструкции пленочных образцов.
УДК 675.043.42
ВЯЗКОУПРУГИЕ СВОЙСТВА РАСТВОРОВ ЦИЛИНДРИЧЕСКИХ МИЦЕЛЛ ПОВЕРХНОСТНО-АКТИВНОГО ВЕЩЕСТВА
Московский государственный университет имени , г. Москва
E-mail: *****@***phys. *****
В данной работе исследованы реологические свойства солевых растворов анионного поверхностно активного вещества (ПАВ) – олеата калия. При высокой концентрации низкомолекулярной соли KCl в водной среде амфифильные молекулы олеата калия образуют цилиндрические мицеллы. Они могут переплетаться между собой подобно полимерным цепям, что придает растворам ПАВ вязкоупругие свойства. Были исследованы концентрационные зависимости реологических характеристик растворов ПАВ. На концентрационной зависимости вязкости растворов ПАВ в двойных логарифмических координатах обнаружено 3 линейные области, характеризующиеся различными наклонами.
В первой области вязкость растворов порядка вязкости воды. В этих условиях растворы содержат короткие цилиндрические непереплетающиеся мицеллы. Граница между первой и второй областью соответствует переходу от разбавленных к полуразбавленным растворам ПАВ, где мицеллы начинают пересекаться. Наклон концентрационной зависимости во второй области характерен для систем, содержащих короткие перепретающиеся мицеллы.
При дальнейшем возрастании концентрации ПАВ в растворе происходит переход в третью область. Наклон концентрационной зависимости падает и становится характерен для систем, содержащих длинные переплетающиеся мицеллы. В этой области так же получены частотные зависимости упругой и вязкой составляющей комплексного модуля упругости. Они хорошо описываются моделью Максвелла вязкоупругой жидкости с одним временем релаксации. В третьей области вязкость растворов ПАВ достигает 103 Па*с, а модуль упругости 40 Па. При этом G’>G” в широкой области частот, что указывает на гелеобразное состояние системы при данных временах воздействия.
Такие вязкоупругие растворы олеата калия перспективны для применения в нефтедобыче в качестве загустителей жидкостей для гидроразрыва пласта.
Работа выполнена при финансовой поддержке гранта РФФИ № .
УДК 661.725.031.74
,
НЕКОТОРЫЕ ФАКТОРЫ, ВЛИЯЮЩИЕ НА ФЕРМЕНТАТИВНЫЙ ГИДРОЛИЗ ЛИГНОЦЕЛЛЮЛОЗНОГО НЕДРЕВЕСНОГО СЫРЬЯ
Бийский технологический институт (филиал) ФГБОУ ВПО
«Алтайский государственный технический университет
им. », г. Бийск
Федеральное государственное бюджетное учреждение науки
Институт проблем химико-энергетических технологий
Сибирского отделения Российской академии наук, г. Бийск
E-mail: moma.08@mail.ru
Необходимость исследования механизма ферментативной биоконверсии растительного сырья обусловлена прогрессирующим дефицитом невозобновляемых источников энергии и материалов [1]. Некоторыми факторами, влияющими на гидролиз целлюлозосодержащих материалов, являются вид используемого сырья, способ его предобработки, выбор реакционной среды, концентрация субстрата, частота перемешивания и другие. Многие из этих факторов взаимозависимы, и это делает весь процесс довольно сложным. В оптимальном случае реакция должна быть быстрой и полной, с образованием больших концентраций глюкозы без существенной потери активности фермента [2].
Одними из нетрадиционных источников целлюлозы, используемых в ИПХЭТ СО РАН, являются мискантус и плодовые оболочки овса (ПОО). Их объединяет следующее: недревесное происхождение, общедоступность, легкая возобновляемость. Исследовался ферментативный гидролиз (ФГ) лигоцеллюлозных материалов (ЛЦМ) обоих видов сырья, полученных методом азотнокислой варки. Данный метод выбран в силу доступности реагентов и возможности использования стандартного емкостного оборудования для варки.
При равных условиях ЛЦМ ПОО гидролизуется полнее, чем ЛЦМ мискантуса (выход составил 75,4 % и 34,2 % соответственно), что объясняется природой и морфологическими особенностями разных видов сырья [3-5].
Ферментативный гидролиз целлюлозосодержащего сырья (ЦСС) обычно проводят в ацетатном буфере. Однако уксусная кислота является ингибитором спиртового брожения, поэтому для получения доброкачественных гидролизатов и в последующем биоэтанола ферментативный гидролиз следует проводить в водной среде. Гидролиз быстрее проходил в ацетатном буфере, а концентрация редуцирующих веществ (РВ) через сутки гидролиза была примерно в два раза выше, чем в водной среде. При ФГ ЛЦМ ПОО после вторичного добавления ферментных препаратов в водной среде получен выход РВ, аналогичный выходу в ацетатном буфере – 75,4 % и 76,3 % соответственно [3]. Возможно, в процессе гидролиза происходит необратимая адсорбция ферментных препаратов на субстрате и тем самым вывод их из системы [6]. Эта версия подтверждается увеличением скорости гидролиза после вторичного внесения ферментных препаратов.
Зависимость выхода РВ от концентрации субстрата для ЛЦМ мискантуса и ПОО аналогична описанным в литературе: при повышении концентрации субстрата выход РВ снижается [4].
Также на ферментативный гидролиз ЛЦМ влияет частота перемешивания. Ферментация в статических условиях в первые 8 часов обеспечивает более быстрое накопление РВ. Однако в дальнейшем гидролиз в статических условиях идёт очень медленно, а при перемешивании с частотой 150 мин-1 проходит быстрее и глубже. Возможно, это объясняется тем, что лимитирующей стадией ферментативного гидролиза целлюлозы является присоединение фермента к субстрату [1, 5].
Проблема ферментативного гидролиза является нерешённой, и влияние многих факторов остаётся неоднозначным [6]. Интенсификация ферментативного гидролиза позволит эффективно использовать колоссальные резервы растений и древесины, образующихся в процессе фотосинтеза [1].
Список литературы:
1 , , Черноглазов лигноцеллюлозных материалов: учеб. пособие. – М.: Изд-во МГУ, 1995. – 224 с.
2 , , Богдановская синтез на основе целлюлозы: Белок и другие ценные продукты.— Минск: Наука и техника, 1988.—261 с.
3 , Скиба гидролиз лигноцеллюлозного материала в ацетатном буфере и водной среде/ Всероссийская школа-конференция «Химия биологически активных веществ» молодых учёных, аспирантов и студентов с международным участием «ХимБиоАктив-2012» 24-28 сентября 2012. – В печати.
4 Момот ферментативного гидролиза лигноцеллюлозных материалов в водной среде от концентрации субстрата: материалы Международной молодежной конференции «Биокаталитические технологии и технологии возобновляемых ресурсов в интересах рационального природопользования», 10 – 12 сентября 2012 г. / Под общ. ред. ; ФГБОУ ВПО «Кемеровский технологический институт пищевой промышленности». – Кемерово, 2012. – С. 142-146.
5 , , Скиба гидролиз лигноцеллюлозных материалов в зависимости от частоты перемешивания: материалы Международной молодежной конференции «Биокаталитические технологии и технологии возобновляемых ресурсов в интересах рационального природопользования», 10 – 12 сентября 2012 г. / Под общ. ред. ; ФГБОУ ВПО «Кемеровский технологический институт пищевой промышленности». – Кемерово, 2012. – С. 147-150.
6 Evaluation of the Factors Affecting Avicel Reactivity Using Multi-Stage Enzymatic Hydrolysis // Biotechnology and Bioengineering. 2012. – Vol. 109, № 5, May, 2012. – Р. 5-15.
УДК 661.725.031.74 : 612.015.161
,
ПОЛУЧЕНИЕ БИОЭТАНОЛА ИЗ ТЕХНИЧЕСКОЙ ЦЕЛЛЮЛОЗЫ ПЛОДОВЫХ ОБОЛОЧЕК ОВСА МЕТОДОМ ОДНОВРЕМЕННОГО ОСАХАРИВАНИЯ – СПИРТОВОГО БРОЖЕНИЯ
Бийский технологический институт (филиал) ФГБОУ ВПО
«Алтайский государственный технический университет
им. », г. Бийск
Федеральное государственное бюджетное учреждение науки
Институт проблем химико-энергетических технологий
Сибирского отделения Российской академии наук, г. Бийск
E-mail: moma.08@mail.ru
Биоконверсия возобновляемого растительного сырья в топливо рассматривается в настоящее время как одна из ключевых отраслей биотехнологии [1].
Целью данной работы являлось исследование одновременного процесса осахаривания – спиртового брожения при получении биоэтанола. В качестве сырья был выбран возобновляемый источник: отходы переработки злаковых культур на примере плодовых оболочек овса (ПОО). Субстрат для гидролиза (техническая целлюлоза ПОО, № 000-12) получен азотнокислым способом на опытном производстве в ИПХЭТ СО РАН. Характеристика субстрата представлена в таблице 1.
Таблица 1 – Характеристика технической целлюлозы ПОО
Характеристики, м. д., % *на а. с.с. | ТЦ ПОО |
Пентозаны* | 3,03 |
Зола* | 5,68 |
Кислотонерастворимый лигнин* | 0,84 |
α-целлюлоза* | 94,62 |
Влага | 75,7 |
Осахаривание целлюлозы ПОО проводили в водной среде, активная кислотность на уровне 5,10-5,30 в процессе гидролиза регулировалась с помощью ортофосфорной кислоты. Концентрация субстрата составила 56 г/л. В качестве катализаторов использовали композицию ферментных препаратов: «Целлолюкс - А» (0,04 г/г субстрата) и «Брюзайм BGX» (0,2 г/г субстрата).
В течение первых суток проводилось только осахаривание субстрата при температурах 50, 40 и 30 ºС (варианты А, Б и В соответственно).
Затем в гидролизат внесены засевные дрожжи, находящиеся в экспоненциальной фазе развития, в количестве 10 % и в течение трёх последующих суток проводилось спиртовое брожение, совмещенное с осахариванием. В качестве продуцента биоэтанола использовались дрожжи Saccharomyces сerevisiae, штамм ВКПМ Y-1693. Брожение проводилось при 30 ºС в анаэробных условиях.
Концентрацию редуцирующих веществ (РВ) определяли спектрофотометрическим способом в пересчете на глюкозу. Объёмную долю спирта в бражках определяли ареометром в дистилляте, полученном после предварительной перегонки спирта из бражки согласно ГОСТ Р .
Таблица 2 – Зависимость концентрации редуцирующих веществ от продолжительности одновременного процесса осахаривания-спиртового брожения
Продолжительность процесса осахаривания-спиртового брожения, ч | Концентрация РВ, г/л | ||
А | Б | В | |
6 | 22,8 | 10,0 | 3,5 |
24 | 44,0 | 30,5 | 24,8 |
48 | 37,8 | 48,9 | 49,2 |
72 | 21,5 | 33,2 | 38,2 |
96 | 14,2 | 15,9 | 18,8 |
С повышением температуры осахаривания эффективность процесса повышается, что наблюдается и через 6 и через 24 часа. Это закономерно и соответствует паспортным характеристикам ферментных препаратов.
После внесения дрожжей концентрация РВ в гидролизате во всех случаях убывает медленно, что можно объяснить адсорбцией дрожжевых клеток на субстрате.
Суммарный выход этанола из технической целлюлозы для процессов осахаривания-спиртового брожения для вариантов А и Б составил 58,3 %, а для варианта В – 61,1 %.
Исследована конверсия технической целлюлозы плодовых оболочек овса в этанол путем одновременного осахаривания – спиртового брожения. Показано, что несмотря на увеличение эффективности осахаривания при повышении температуры, процесс одновременного осахаривания – спиртового брожения можно проводить при температуре 30 ºС. Это приводит к экономии энергоресурсов и обеспечивает тождественный выход этанола. Оптимизация стадии брожения позволит повысить выход этанола.
Список литературы:
1 , , Черноглазов лигноцеллюлозных материалов: учеб. пособие. – М.: Изд-во МГУ, 1995. – 224 с.
УДК 579.66
, ,
БАКТЕРИЯ ОСHROBACTRUM SP. ИБ ДТ-5.3/2, РАЗЛАГАЮЩАЯ НЕФТЯНЫЕ УГЛЕВОДОРОДЫ
Федеральное государственное бюджетное учреждение науки
Институт биологии Уфимского научного центра РАН, г. Уфа
E-mail: *****@***ru
Загрязнение окружающей среды нефтью и ее производными до сих пор остается одной из самых актуальных мировых экологических проблем. По степени вредного воздействия на экосистемы нефть, нефтепродукты и нефтесодержащие промышленные отходы занимают второе место после радиоактивных поллютантов [1]. Физические, термические и химические методы разрушения нефтяных соединений, несмотря на то, что способствуют интенсификации их разложения, не обеспечивают полное удаление из почвенного слоя и могут являться дополнительным источником поступления загрязняющих веществ в окружающую среду [2, 3]. Использование биологических средств для ликвидации нефтяных загрязнений почвы часто является единственно возможным способом восстановления экологически чистой обстановки в природных условиях без нарушения естественного биоценоза. Внесение дополнительных количеств эффективных микроорганизмов-деструкторов, способных разлагать большой круг органических экотоксикантов, позволяет ускорить разрушение нефти [4]. Поэтому поиск и идентификация микроорганизмов, обладающих такими свойствами, является актуальным.
Штамм Ochrobactrum sp. ИБ ДТ-5.3/2 был выделен из серой лесной почвы, искусственно загрязненной дизельным топливом, и проявлял окислительную активность по отношению к нефтяным углеводородам.
Целью данной работы являлось описание обнаруженного штамма по биохимическим и культурально-морфологическим признакам.
Клетки штамма Ochrobactrum sp. ИБ ДТ-5.3/2 грамположительные, аэробные, эндоспор не образуют. Бактерии представляют собой короткие палочки, по мере роста и старения культуры, распадающиеся на кокковидные клетки. На плотных питательных средах колонии круглые, матового цвета, плоские, по краям менее плотные, чем в центре.
Оптимальная температура роста и развития +300С. Не растут на среде с 6,5% NaCl. Реакция Фогес-Проскауера отрицательная. Каталазоположительны, не гидролизуют желатину, крахмал, казеин, разлагают мочевину, не обладают липазной и лецитиназной активностью. Не образуют индола, сероводорода. Потребляют малонат, цитрат. Используют в качестве источника углерода углеводы (глюкоза, L-арабиноза, сахарозу, лактоза, мальтоза, L-рамноза, ксилоза и др.), некоторые спирты (маннит, сорбит). При этом образует газ. Фиксируют атмосферный азот. Усваивают аланин, серин, метионин. Способны окислять углеводороды нефти парафинового ряда (гептан, декан, ундекан, додекан), нафтеновые углеводороды (циклогексан), ароматические углеводороды (бензол, толуол).
Список литературы:
1 , , Чушкина различных технологий при ликвидации последствий аварийных разливов нефти и нефтепродуктов и переработки нефтесодержащих отходов // Проблемы безопасности и чрезвычаных ситуаций. 2004. № 6. С. 34-40.
2 Абросимов переработки углеводородных систем. М.: Химия, 20с.
3 Роев очистка // Охрана от коррозии и защита окружающей среды. 1998. № 1. С. 12-21.
4 Eriksson M., Dalhammar G., Borg-Karlson A. K. Biological degradation of selected hydrocarbons in an old РАН/creosote contaminated soil from a gas work site // Appl. Microbiol. Biotechnol. 2000. V. 53. P. 619-626.
УДК 541.64:542.952
1, 1,2, 3
ПОЛУЧЕНИЕ ПОРФИРИНСОДЕРЖАЩИХ ПОЛИМЕРОВ МЕТОДОМ РАДИКАЛЬНОЙ СОПОЛИМЕРИЗАЦИИ
1 Федеральное государственное бюджетное учреждение науки
Институт органической химии Уфимского научного центра Российской академии наук, г. Уфа
E-mail: *****@***ru
2 Федеральное государственное бюджетное образовательное учреждение высшего профессионального образовании
«Башкирский государственный аграрный университет», г. Уфа
3 Институт макрогетероциклических соединений Ивановского государственного химико-технологического университета, г. Иваново
Исследована радикальная сополимеризация винилпорфирина метилфеофорбида “А” (МФФ) и стирола или метилметакрилата (ММА), инициированная азодиизобутиронитрилом (АИБН) при 60-90°С.
Обнаружено, что общая скорость процесса сополимеризации винилпорфирина и стирола (ММА) в массе при 60-90°С меньше по сравнению с гомополимеризацией стирола или ММА. При этом сополимеризация ММА и МФФ протекает до глубоких степеней превращения с гель-эффектом, в то время как в случае стирола наблюдается значительное замедление процесса и вырождение автоускорения. Повышение температуры синтеза приводит к увеличению общей скорости сополимеризации и уменьшению времени достижения максимальных конверсий. Изучение растворной сополимеризации МФФ и стирола (ММА) показало, что введение сомономера МФФ приводит к снижению скорости сополимеризации по сравнению с гомополимеризацией стирола (ММА) при всех исследованных концентрациях МФФ: при содержании МФФ 0.1 мол. % наблюдается незначительное замедление процесса, тогда как повышение концентрации винилпорфирина до 0.5 мол. % сопровождается снижением общей скорости в 2-5 раз в зависимости от условий процесса. Последующее увеличение содержания МФФ в исходной реакционной смеси (до 1.0 мол. %) способствует дальнейшему замедлению сополимеризации. При увеличении температуры синтеза наблюдается закономерное ускорение процесса, а при снижении содержания инициатора с 10.0 до 1.0 ммоль/л – снижение общей скорости сополимеризации при всех исследованных соотношениях сомономеров.
Константы сополимеризации для стирола при 90°С и ММА при 60 и 80°С, определенные по уравнению Майо-Льюиса (для МФФ принято r2 → 0), составили соответственно: r1 = 1.71 ± 0.06, r1 = 0.36 ± 0.03 и r1 = 0.62 ± 0.03.
Работа выполнена при финансовой поддержке Федеральной целевой программы «Научные и научно-педагогические кадры инновационной России» на г. г. (Заявка 2012-1.2.06-004, Соглашение 8458).
УДК 579.66:547.94
, ,
Исследование Влияния условий предобработки
на БИОКОНВЕРСИЮ растительного сырья
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Уфимский государственный нефтяной технический университет, г. Уфа
Е-mail: *****@***net
Древесная целлюлоза является сырьём, трудно конвертируемым в растворимые сахара, поскольку ее высокоупорядоченная структура пронизана лигнином – инкрустирующим групповым полимером, состоящим из фенил-пропановых структурных звеньев. Для более полной конверсии целлюлозы необходимо увеличение её поверхности и разрушение ее микрофибриллярной структуры, поэтому различные методы предобработки играют важную роль в биодоступности целлюлозосодержащего сырья.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 |




