Проблема увеличения степени конверсии целлюлозы в растворимые сахара остается актуальной, так как многие способы предобработки невозможно применить в промышленных масштабах вследствие их высокой стоимости, токсичности реагентов или образования побочных продуктов.
Органосольвентная варка древесины является перспективным процессом делигнификации лигноцеллюлозы. В то же время несомненный интерес представляет использование в качестве реагента для делигнификации глицерина, который в настоящее время, являясь отходом производства биодизеля, становится более доступным и дешевым продуктом.
Целью данной работы являлось исследование влияния органосольвентной варки древесных опилок в водных растворах глицерина на степень их гидролиза в присутствии ферментного препарата «Целлолюкс F».
Показано, что при глицеросольволизе древесных опилок происходит их делигнификация. В области концентраций глицерина 5-30% содержание лигнина в опилках уменьшается на 24-34%.
Установлено, что последующий ферментолиз опилок, предобработанных 6%-ным раствором глицерина, с помощью ферментного препарата «Целлолюкс F» при температуре 450С в 0,1 М ацетатном буфере (рН 4,8) увеличивает выход редуцирующих веществ на 10,3%, что в 3 раза превышает этот показатель в контрольном варианте.
Показано, что глицеросольволиз опилок 6%-ным раствором глицерина в присутствии щелочных катализаторов (1%-ные растворы NaHCO3, NaOH) позволяет дополнительно увеличить выход редуцирующих веществ на стадии ферментолиза до 16-26%.
УДК 547.822.362
Синтез насыщенного аналога 1-(2-этоксиэтил)-4-метокси-4-{3-[N-метил-N-(2-гидроксиэтил)амино]-1-пропин-1-ил}пиперидина и его дифенилметилового эфира
Каспийский государственный университет технологий и инжиниринга
им. Ш Есенова, Республика Казахстан
Институт нефти и газа
На биологические свойства соединений большое влияние оказывает присутствие в их структуре насыщенной или ненасыщенной группировки. Продукт исчерпывающего гидрирования аналога соединения (2) (рис.1) с этоксигруппой в положении 4 проявил высокую антибактериальную и противоаллергическую активность [1] и рекомендуется для лечения колибактериоза животных. Кроме того, этот препарат обладает мембраностабилизирующей и спазмолитической активностью [2]. Чтобы проверить, как отразится на биологических свойствах препаратов замена этоксигруппы в положении 4 на метоксильную, 1-(2-этоксиэтил)-4-метокси-4-{3-[N-гидроксиэтил)амино]-1-пропин-1-ил}-4-метоксипиперидин (1) (рис.1) был исчерпывающе прогидрирован на катализаторе никеля Ренея в спиртовой среде при атмосферном давлении.
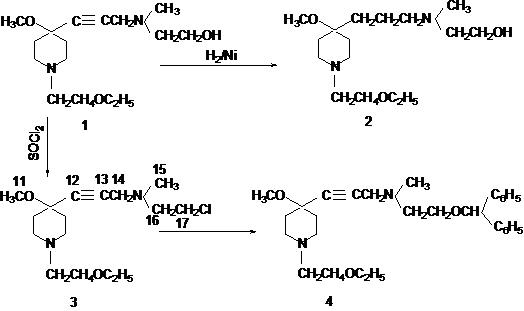
Рисунок 1.
Соединение (2) выделялось в виде маслообразного основания, которое затем превращалось в кристаллическую соль – диоксалат 1-(2-этоксиэтил)-4-метокси-4-{3-[N-метил-N-(2-гидроксиэтил)амино]-1-пропин-1-ил}пиперидина (2, ДОК). Выходы, физико-химические данные и результаты элементного анализа основания (2) и его диоксалата (2, ДОК) приведены в таблице 1.
В спектре ПМР соединения (2), записанном DMCO-D6 имеются два триплетных сигнала группы СН2О в области 3,42 м. д. и 3,43 м. д. Это, по-видимому, связано с образованием внутримолекулярной водородной связи:
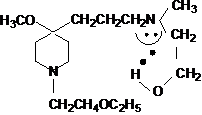
Протон группы ОН дает широкий сигнал с центром 3,33 м. д. В спектре диоксалата (2, ДОК) уширенный синглетный сигнал при d 6,23 м. д. дают протоны щавелевой кислоты.
Введение в структуру эфира дифенилметильного остатка, входящего в молекулу димедрола [3] и некоторых других антигистаминных препаратов [4, 5], может увеличить его антигистаминную активность.
Для синтеза такого «аналога» димедрола соединение (1) (рис.1) обработкой свежеперегнанным хлористым тионилом в абсолютном хлороформе превращалось в хлорэтиламинопроизводное (3) (рис.1), которое выделялось и характеризовалось в виде дигидрохлорида (3, ДГХ).
В спектре ЯМР 13С, записанном в СН3ОН, для соединения (3, ДГХ) сделаны следующие отнесения (d м. д.): 14,3(С10); 32,4 и 33,8 (С3,5); 37,4(С15); 40,0(С17); 45,8(С14); 47,2(С16); 50,8(С2,6); 51,1(С7); 56,6(С11); 64,2(С9); 66,8(С8); 67,6(С4); 74,2(С13); 76,9(С12).
Реакцией хлориэтиламинопроизводного (3, ДГХ) с бензгидролом в присутствии избытка NaOH получен дифенилметиловый эфир 1-(2-этоксиэтил)-4-метокси-4-{3-[N-метил - N-(2-гидроксиэил)амино]-1-пропин-1-ил}пиперидина (4) (рис.1).
В спектре ЯМР 13С диоксалата этого соединения (4, ДОК) сделаны следующие отнесения сигналов (d м. д.): 14,3(С10); 32,6 (С3,5); 40,5(С15); 45,6(С14); 49,3 (С2,6); 51,2 (С16); 54,8 (С7); 55,6(С11); 58,1 (С17); 64,3(С9); 66,4(С8); 68,8 (С18); 76,4 (С4); 83,6 (С13); 87,8 (С12); 126,8(4Соар); 127,5 (2Спар); 128,3 Смар); 141,5 (С1ар); 164,9 (4С щавелевой кислоты).
Контроль за ходом реакций и индивидуальность синтезированных соединений осуществлялся с помощью тонкослойной хроматографии на пластинках “Silufol UV-250” (элюент: изопропанол – 20% раствор аммиака 9,3:0,7) и “Alufol” (изопропанол – бензол 1:10) с проявлением пятен парами йода. Все температурные данные приведены в 0С.
ИК-спектры соединений записаны на приборе “Specord M-80” в таблетках KBr для кристаллических образцов и в тонком слое для жидких. Спектры ПМР сняты на приборе “Mercury - 300” (300 МГц). Спектры ЯМР 13С получены на приборе “Bruker WP-80” (20,155 МГц) и “Mercury - 300” (75 МГц). Внутренний или внешний стандарт – ГМДС.
Список литературы:
1 Предпатент РК. № 000. Дималеат 1-(2-этоксиэтил)-4-{3-[4-N-метил - N-(2-гидроксиэил)амино]пропил}-4-этоксипиперидина, обладающий противоаллергической и антибактериальной активностью // , , К, , Шин . Б. И. -2002. -№3.
2 Предпатент РК. № 000. Дималеат 1-(2-этоксиэтил)-4-{3-[N-метил-(2-гидроксиэил)амино]пропил}-4-этоксипиперидина, обладающий мембраностабилизирующей и спазмолитической активностью // , , К, , Тен ВБ. Опубл. Б. И. -2000. -№6.
3 Машковский средства. –М. Медицина, 1994. –чс.
4 Заявка Франции. № 000. Procede d’hydrogenaton selective des composes insatures // Didillon Blaise, Le Peltier Fabienne. –РЖХим. -20Н18П.
5 Науырызова , структура и свойства продуктов трансформации 1-(2-этоксиэтил)-4-этинил-4-гидроксипи-перидина. Дисс…канд. хим. наук. – Алматы, 2003. – 132с.
УДК 543.422.25
1, 2, 2,
2, 2
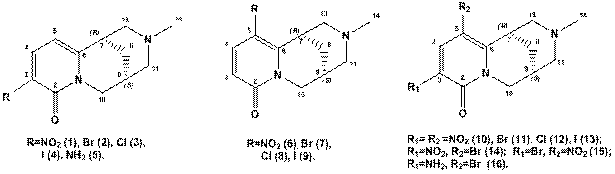
СТРУКТУРА 3-, 5- ЗАМЕЩЕННЫХ ПРОИЗВОДНЫХ N-Me-(-)-ЦИТИЗИНА ПО ДАННЫМ СПЕКТРОСКОПИИ ЯМР 1H и 13C.
1 Башкирский Государственный университет, г. Уфа
2 Институт органической химии УНЦ РАН, г. Уфа
e-mail: lobovan@anrb.ru
Как известно, функционализация пиридонового ядра (-)-цитизина до сих пор представляет собой острую проблему. В данной работе мы представляем спектральные характеристики и установленные структуры производных хинолизидинового алкалоида N-Me-(-)-цитизина.
Введение нитрогруппы в пиридоновое кольцо молекулы N-Me-(-)-цитизина в значительной степени расширяет его синтетический потенциал – становятся возможными реакции, характерные для 1,3-динитроароматических соединений, а восстановление нитрогруппы до амина позволяет проводить реакции наращивания цепи с помощью реакций, характерных для аминогруппы. Кросс-сочетание галоидпроизводных N-Me-(-)-цитизина с ненасыщенными соединениями представляет собой перспективный подход к синтезу разнообразных 3-алкенилзамещенных производных и, далее, к построению новой циклической системы путем вовлечения полученного диена в реакцию Дильса-Альдера с подходящими диенофилами.
|
Структуры 3-, 5- замещенных N-Me-(-)-цитизина. |
Структуры новых соединений 1-16 изучены с помощью метода ЯМР спектроскопии. Полное отнесение сигналов в спектре ЯМР 13С и 1H проведено с помощью корреляционной спектроскопии ЯМР 1Н-1Н COSY, 1H-13С HSQC, 1H-13С HMBC, 1Н-1Н NOESY. На основании анализа хим. сдвигов 1H и 13С предложены критерии установления региоизомерии положения заместителя и природы заместителя в пиридоновом кольце.
УДК 6
,
ЭКСТРАКЦИЯ ВОДОРАСТВОРИМЫХ ПОЛИСАХАРИДОВ, ФЛАВОНОИДОВ И КАРОТИНОИДОВ ИЗ ЛЕКАРСТВЕННОГО РАСТИТЕЛЬНОГО СЫРЬЯ
Башкирский государственный университет, г. Уфа
e-mail:nikvalent@mail.ru
В связи с высокой физиологической активностью растительных полисахаридов, флавоноидов и каротиноидов изучение рациональных способов совместного их выделения из лекарственного растительного сырья имеет актуальное значение для создания высокоэффективных терапевтических средств.
Целью данной работы являлось сравнительное изучение совместного извлечения разными экстрагентами водорастворимых полисахаридов, флавоноидов и каротиноидов из некоторых лекарственных растений - девясила высокого Inula helenium , одуванчика лекарственного Taraxacum officiale Wigg. , эхинацеи Echinacea и стевии медовой Stevia rebaudiana.
Анализ содержания полифруктанов осуществляли по известной из литературы методике на основе проведения колориметрической реакции полифруктанов с резорцином в присутствии тиомочевины в пересчете на фруктозу. Содержание растворимых полифенольных соединений и флавоноидов определяли по реакции комплексообразования флавоноидов с хлоридом алюминия в пересчете на рутин. В таблице приведены значения содержания полифруктанов, флавоноидов и каротиноидов в исходном растительном сырье.
Растительное сырье | Содержание | ||
полифруктанов, % масс. | флавоноидов (по рутину) мг/г | каротиноидов, мг/г | |
листья стевии | 9,4 | 2,98 | 5,56 |
листья эхинации | 4,4 | 4,42 | 5,85 |
корни девясила | 17, 0 | 1,58 | 4,00 |
корни одуванчика | 2,7 | 2,30 | 4,50 |
Изменчивость выхода экстрактивных веществ в зависимости от качества растительного сырья и состава экстрагента представлена на рисунке. Как видно, при использовании 0,5%-ного раствора HCl (pH=1,15) выход экстрактивных веществ был на 3-5% ниже, чем при экстракции другим экстрагентом – эквимолярной смесью оксалата аммония и щавелевой кислоты (pH= 2,57).
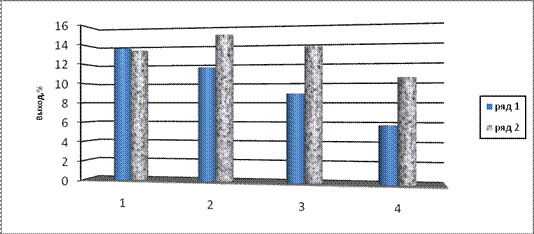
Рисунок 1 - Изменчивость выхода экстрактивных веществ в зависимости от качества растительного сырья и состава экстрагента (ряд 1 - соляная кислота 0,5% раствор, ряд 2 – эквимолярная смесь 0,5%-ных растворов оксалата аммония и щавелевой кислоты). 1 – корни девясила, 2 – корни одуванчика, 3 – листья стевии, 4 – листья эхинацеи.
Выделенные экстракты полностью растворялись в воде при комнатной температуре, состояли из полисахаридов %), флавоноидов (1,5-2%) и каротиноидов (около 1%). Разносторонняя фармакологическая активность растительных полисахаридов, флавоноидов и каротиноидов позволяет рассматривать экстрактивные смеси этих биологически активных соединений, полученные из соответствующего растительного сырья, как перспективные источники новых терапевтических средств.
УДК 504
, ,
БИОЛОГИЧЕСКАЯ ОЧИСТКА ВОДОЕМОВ И ПОЧВЫ
Башкирский государственный университет, г. Уфа
E-mail *****@***ru
В настоящее время в мире существует большая проблема очистки почвы и подземных вод от нефтепродуктовых загрязнений. Для решения этой проблемы используются много методов, однако самой рациональной в настоящее время является биологическая очистка. Ее преимуществом является относительная простота технологической реализации установки и эксплуатации, а также относительно невысокие финансовые затраты. Она широко используется во многих странах уже в течение 29 лет, успешно применяется при очистке почв и водных ресурсов от бензина, дизельного топлива и других нефтепродуктов.
Биологическая очистка представляет собой внесение бактерий, микроорганизмов способных разлагать нефтепродукты и вырабатывающих вещества, способствующих его быстрому разложению, также для удаления органических загрязнителей, азотных и фосфорных соединений.
Биологические методы очистки можно подразделить на два типа:
- методы микробиодеградации загрязнителей;
- методы биопоглощения и перераспределения загрязнителей.
Методы микробиодеградации основаны на деструкции загрязнителей различными видами микроорганизмов. Эффект достигается за счет активизации аборигенной микрофлоры или внесения в грунт определенных культур микроорганизмов, а также всевозможных комплексных препаратов. В результате этого микроорганизмы начинают активно поглощать загрязнитель и вызывать его деструкцию. Ускоряют биодеградацию нефти целлюлозосодержащие отходы — солома, опилки. Эффективно внесение опилок со стимуляторами разложения нефти.
Технология микробиологического обезвреживания органических экотоксикантов основаны на активации аборигенной микрофлоры или внесении в грунт культур определенных микроорганизмов и создании оптимальной среды для их развития.
Идеальной для биоразложения является нейтральная среда. Для нейтрализации щелочных грунтов вносят гипс, для нейтрализации кислых грунтов — известь.
Одним из методов, обеспечивающих диспергирование нефтяных загрязнений и улучшающих контакт с микроорганизмами, является внесение поверхностно-активных веществ (ПАВ). Сочетание применения ПАВ с внесением минеральных удобрений ускоряет биодеструкцию.
Внесение культур микроорганизмов используется только при аварийных загрязнениях или при отсутствии развитого естественного биоценоза. Однако иногда происходит вырождение микроорганизмов до достижения требуемого уровня очистки. Их применение также может нарушать естественные биоценозы.
Обычно для очистки используют сообщества бактерий Bacterium, Actinomyces, Artrobactes, Thiobacterium, desullfotomasilium Pseudomons, Hydiomonas, Bacillus и другие, а также низшие формы грибов.
В России для очистки от нефтепродуктов используют бактериальные препараты «Деворойл», «Олеоворин», «Путидойл», «Сойлекс», «Фаерзайн» и др.
Биопрепараты содержат в своем составе удобрения и микроорганизмы, выделенные из природных биоценозов, обладающие повышенной окислительной способностью по отношению к нефти, прошедшие адаптацию в естественных условиях.
Используют либо один штамм, либо смесь штаммов углеводородоокисляющих бактерий, в основном аэробов.
Препараты эффективно окисляют нефтепродукты, ароматические углеводороды в температурном диапазоне от –5 до +45 °C при значительных начальных концентрациях загрязнений в грунтах.
Биологическая очистка находит широкое применение во всем мире и продолжает усовершенствоваться и развиваться.
Список литературы:
1 , Башин допустимое содержание нефтепродуктов в почвенных экосистемах Пермской области// Известия вузов. Нефть и газ. 2004. №2. С.91-96.
2 , "Химия воды и микробиология" М: Стройиздат, 1983
3 Протасов , здоровье и природопользование в России /, - М.: Изд-во Финансы и статистика, 1995. –
528 с.
УДК 622.276.64
О ПРИМЕНЕНИИ БИОПАВ ПРИ РАЗРАБОТКЕ НЕФТЯНЫХ МЕСТРОЖДЕНИЙ
ФГБОУ ВПО «Башкирский государственный университет», г. Уфа
E-mail:dodger86@ya.ru
Большинство крупных месторождений в России находятся на поздней стадии разработки, как следствие наблюдается ухудшение качества остаточных запасов нефти с переходом их в разряд трудноизвлекаемых. Повышению коэффициента извлечения нефти способствует применение методов увеличения нефтеотдачи. Одним из таких методов являются химические методы, основанные на повышении коэффициента вытеснения нефти водными растворами поверхностно-активных веществ (ПАВ).
При выборе ПАВ, используемого при заводнении, внимание уделяют их физико-химическим свойствам, стоимости ПАВ, наличию источников сырья и экологической безопасности. Проблема синтеза хорошо биоразлагаемых ПАВ приобрела в настоящее время особенную актуальность [1].
Перспективным направлением при заводнении пластов является применение ПАВ биологического происхождения (биоПАВ). Их преимущество перед синтетическими – биодеградабельность при высоких температурах, рН, концентрации солей в пластовой воде. Данные ПАВ могут быть разделены на две основные группы:
1) низкомолекулярные соединения, называемые собственно биоПАВ, представленны гликолипидами (глюколипиды, рамнолипиды, трегалозолипиды, софоролипиды) и липопептидами (сурфактин, стрептофактин, полимиксин, грамицидин). Они эффективно снижают поверхностное и межфазное натяжение на границе «вода-нефть»;
2) высокомолекулярные соединения, называемые биоэмульгаторами, представленны полисахаридами, липополисахаридами, липопротеинами, протеинами, и их комплексами [2]. Данная группа объединяет полимеры, которые эффективны для стабилизации эмульсий типа «масло в воде».
Масштабное внедрение технологий повышения нефтеотдачи с применением биоПАВ было осуществлено в . Использовался биоПАВ КШАС-М, который представляет собой природную композицию гликолипидной природы, продуцируемую культурой микроорганизмов Pseudomonas aeruginosa S-7. Растворы биоПАВ КШАС-М могут снижать поверхностное натяжение воды до 30 мН/м, обладают высокой эмульгирующей Е24 до 60-80%, где E24 - устойчивость эмульсии в течение 24 часов.
В 1995 г. проведены опытно-промысловые работы по применению биоПАВ на Северо-Сергеевской площади Сергеевского месторождения республики Башкортостан. Была осуществлена обработка нагнетательных скважин с БКНС № 3. После закачки биоПАВ среагировали 29 добывающих скважин. Дополнительная добыча нефти по этим скважинам составила за шесть месяцев около 2,5 тыс. т. Удельный технологический эффект составил 54 т дополнительной нефти на 1 т биореагента [3].
Список литературы:
1 Петров анионных и катионных ПАВ для применения в нефтяной промышленности / Н. А Петров, , : Учеб. пособие/ УГНТУ.– Уфа, 2008. – 54с.
2 и др. Образование нефтевытесняющих соединений микроорганизмами из нефтяного месторождения Дацин (КНР) / , , -Ф., , // Микробиология, 2003, №2. – C.206-211.
3 Сафонов извлечения остаточной нефти на месторождениях Башкортостана. – Уфа: РИЦ АНК "Башнефть", 1997. – 247 с.
УДК 547.94:834.2
2, 1, 1
Восстановительное алкилирование
3-аминометилцитизина
1 ФГБУН Институт органической химии Уфимского научного центра Российской академии наук, г. Уфа
E-mail: tsipisheva@anrb.ru
2 ГОУ ВПО «Башкирский государственный университет»,г. Уфа
Ранее нами показано, что производные хинолизидинового алкалоида
(-)-цитизина, несущие в 2-пиридоновом ядре карбоксамидные группы проявляют высокую ноотропную активность [1]. С целью расширения круга тестируемых соединений получен новый скаффолд производных 2-14 путем восстановительного алкилирования 3-аминометилцитизина 1.
В реакцию вовлечены метокси-, гидрокси - замещенные бензальдегиды, пиридин-3-бензальдегид, терефталевый и коричный альдегиды, а также фурфурол, тиофен-, имидазол - и тиазолкарбальдегид.

Структура вторичных аминов 2-13 установлена на основании данных спектроскопии ЯМР 1Н и 13С.
Работа выполнена при поддержке гранта РФФИ № -а.
Список литературы:
1 , , Химия природных соединений, 4,
2 Sh. B. Rakhimov, V. I. Vinogradova, Yu. R. Mirzaev, N. L. Vypova, D. S. Kazantseva, Chemistry of Natural Compounds, 42,
УДК 547.94:834.2
2, 1, 1
Формилирование N-метилцитизина
1 ФГБУН Институт органической химии Уфимского научного центра Российской академии наук, г. Уфа
E-mail: tsipisheva@anrb.ru
2 ГОУ ВПО «Башкирский государственный университет», г. Уфа
Известно, что продукты функционализации 2-пиридонового ядра хинолизидинового алкалоида (-)-цитизина проявляют высокую нейрофизиологическую активность [1]. Стратегия синтеза этих соединений практически во всех случаях базируется на синтетической последовательности «электрофильное галогенирование – кросс-сочетание», что позволяет ввести в 2-пиридоновое ядро арильные, алкильные, алкенильные и алкинильные фрагменты [2].
Описан способ синтеза 3-формильного производного 3 путем карбонилирования магнийорганического соединения полученного из соответствующего галогенида 2 [2a].
Нами реализовано прямое формилирование N-метилцитизина по методу Даффа с выходом 82%.
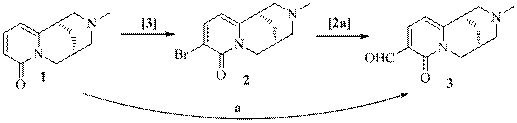
Реагенты и условия: а) уротропин, CF3COOH, 70 оС.
Структура альдегида 3 установлена на основании данных спектроскопии ЯМР 1Н и 13С. Физико-химические константы 3 соответствуют литературным данным [2a].
Работа выполнена при поддержке гранта РФФИ № -а.
Список литературы:
1 E. G. Pérez, C. Méndez-Gálvez, B. K. Cassels, Nat Prod Rep, 29,
2 a) WO 1998/018798; b) WO 2007/100430 A2; c) WO 2007/115092 A2.
3 A. V. Kovalskaya, A. N. Lobov, I. P. Tsypysheva, V. I. Vinogradova, J. V. Vakhitova, M. S. Yunusov, Organic Chemistry:an Indian Journal, 8, 3,
УДК 543.422.25
1, 2, 2,
2, 1, 2
СТРУКТУРА ПРОДУКТОВ ОКИСЛЕНИЯ 2,3-ИНДОЛО-28-ОКСОАЛЛОБЕТУЛИНА ПО ДАННЫМ ЯМР СПЕКТРОСКОПИИ.
1 Башкирский государственный университет, г. Уфа
2 Институт органической химии Уфимского научного центра РАН, г. Уфа, e-mail:lobovan@anrb.ru
Сложность строения полифункциональных замещенных тритерпеноидов требует комплексного подхода к установлению структуры биологически важных соединений данного класса, с комбинацией квантово-химических расчетов (PBE/3z) и ЯМР-спектроскопии.
В результате окисления 2,3-индоло-28-оксоаллобетулина (1) диметилдиоксираном были выделены основные продукты реакции 2 и 3.
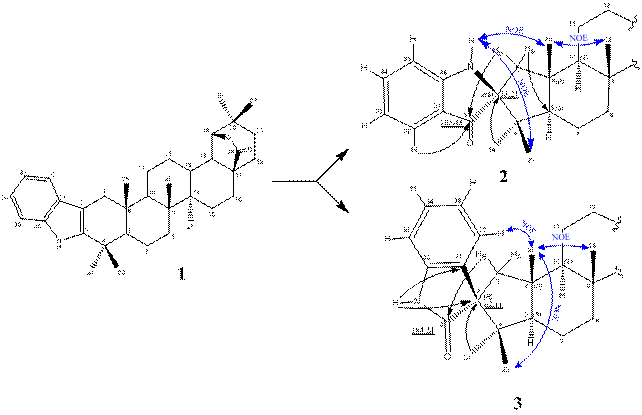
Регио - и стереоизомерия спиросочленения продуктов озонолиза была установлена на основании спектров ЯМР 1H и 13C с использованием двумерных корреляционных методик HSQC, HMBC, COSY и NOESY.
В качестве критерия на основании которого установлено положение C═O группы для структур 2 и 3 выступают значения хим. сдвигов δС 205.48 м. д. (2) и 184.24 м. д. (3). Наличие в спектрах HMBC кросс-пиков данных сигналов с ароматическими протонами H-32 и протонами при С1 доказывает, что они принадлежат углеродным атомам C3. Образовавшиеся центры спиросочленения также имеют характерные для предложенных структур значения хим. сдвигов δС 78.24 м. д. (2) и 62.11 м. д. (3).
Стереохимическое строение образовавшихся продуктов подтверждено с помощью двумерных корреляционных спектров NOESY. Так для структуры 2 найдены NOE-взаимодействия NH протона δH 4.99 м. д. с протонами метильных групп С23 (δH 0.96 м. д.) и С25 (δH 1.04 м. д.). Положение индольного остатка для соединения 3 относительно каркаса молекулы установлено на основании NOE кросс-пиков протона H-32 c протонами метильных групп С23 (δH 0.88 м. д.) и С25 (δH 1.22 м. д.).
Таким образом, установлены структуры продуктов окисления 2,3-индоло-28-оксоаллобетулина с использованием спектроскопии ЯМР.
УДК 541.64
,
ЦИРКОНОЦЕНДИХЛОРИД В СОСТАВЕ ИНИЦИИРУЮЩИХ СИСТЕМ ДЛЯ КОМПЛЕКСНО-РАДИКАЛЬНОЙ ПОЛИМЕРИЗАЦИИ
Уфимский государственный нефтяной технический университет, г. Уфа
E-mail: *****@***ru
Башкирский государственный аграрный университет, г. Уфа
Металлоцены являются объектами повышенного интереса в органической и полимерной химии. Детально изучаются металлоценсодержащие мономеры, (со)полимеры на их основе с целью придания полимерам определенных свойств. Большое число работ посвящено исследованию каталитических систем полимеризации, включающих металлоцены. На основе ценовых соединений циркония получены эффективные системы ионно-координационной полимеризации виниловых мономеров [1].
Имеется ряд публикаций, касающихся инициирования радикальной полимеризации виниловых мономеров в присутствии металлоценов. Описана полимеризация ММА и стирола в присутствии системы ферроцен – CCl4 [2]. Показано [3], что системы металлоцен – пероксид являются весьма эффективными инициаторами радикальной полимеризации метилметакрилата и стирола. В то же время кинетические закономерности процессов изучены явно недостаточно для обоснованных суждений о влиянии металлоценов на механизм радикальной полимеризации виниловых мономеров.
Мы провели цикл работ по исследованию кинетических закономерностей полимеризации метилметакрилата и стирола в присутствии цирконоцендихлорида и некоторых свойств полученных полимеров.

Цирконоцендихлорид (ЦРЦ)
При полимеризации ММА, инициированной пероксидом бензоила, в присутствии цирконоцендихлорида (ЦРЦ) наблюдается увеличение начальной скорости полимеризации W0 в интервале температур 30-60°С, сопровождающееся значительным уменьшением средней степени полимеризации Pη полимеров по сравнению с образцами, полученными в отсутствие добавки (табл. 1).
Таблица 1 - Параметры полимеризации ММА в присутствии ЦРЦ
Т, °С | [Cp2ZrCl2]´103, моль/л | [ПБ]´103, моль/л | W0´103, моль/(л´мин) | Pη ´ 10-3 | Полидисперс-ность MW/MN |
60 | 0 | 1,0 | 3,9 | 15,7 | 2,3 |
0,25 0,5 1,0 | 1,0 | 4,4 3,9 3,8 | 11,4 10,0 7,9 | 2,6 3,1 2,7 | |
1,0 | 0,5 1,0 1,5 | 2,8 3,8 4,3 | 10,0 7,9 8,2 | 2,5 2,7 2,4 | |
45 | 0 | 1,0 | 1,1 | 22,8 | 1,9 |
0,25 0,5 1,0 | 1,0 | 1,2 0,9 1,0 | 13,1 6,8 3,2 | 4,1 3,3 2,4 | |
1,0 | 0,5 1,0 1,5 | 0,7 1,0 1,1 | 3,2 3,2 2,0 | 2,2 2,4 3,1 | |
30 | 0 | 1,0 | 0,3 | 25,4 | 1,9 |
0,25 0,5 1,0 | 1,0 | 0,14 0,16 0,18 | 6,8 6,5 3,7 | 2,7 2,6 2,5 | |
1,0 | 0,5 1,0 1,5 | 0,12 0,18 0,22 | 9,6 3,7 7,5 | 3,0 2,5 2,1 |
При этом значения порядка полимеризации по ЦРЦ составляют 0,2 во всём изученном интервале температур; по пероксиду бензоила порядок составляет 0,4. Можно заключить, что процесс полимеризации в присутствии ЦРЦ протекает по радикальному механизму с квадратичным обрывом цепей. По температурным зависимостям скорости полимеризации была рассчитана эффективная энергия активации полимеризации в присутствии ЦРЦ. Она оказалась равной 32,7±0,4 кДж/моль, что заметно ниже, чем в случае инициирования только пероксидом бензоила (80 кДж/моль) [4], а также в случае инициирующих систем пероксид бензоила – ферроцен (48,3 кДж/моль [4]). Это означает, что снижается, в первую очередь, энергия активации инициирования полимеризации, так как энергии активации роста и обрыва цепей незначительны, и что происходит формирование инициирующей системы пероксид бензоила – ЦРЦ, ускоряющей полимеризацию и переводящей её в режим комплексно-радикального процесса.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 |