Работа выполнена при поддержке гранта РФФИ № -р_поволжье_а.
Список литературы:
1 D. V. Shishkin, A. R. Shaimuratova, A. N. Lobov, N. Z. Baibulatova, L. V. Spirikhin, M. S. Yunusov, N. S. Makara, N. Zh. Baschenko, V. A. Dokichev, Chemistry of Natural Compounds, 43, 190, (2007).
2 A. V. Kovalskaya, A. N. Lobov, I. P. Tsypysheva, V. I. Vinogradova, J. V. Vakhitova, M. S. Yunusov, Organic Chemistry:an Indian Journal, 8, 3,
УДК 547.917
, ,
ЛЕВОГЛЮКОЗЕНОН В СИНТЕЗЕ ПРОИЗВОДНОГО ДЕКАНОЛИДА И ЕГО ПРЕВРАЩЕНИЕ В ЭФИР N-МЕТИЛУРОКАНОВОЙ КИСЛОТЫ
Федеральное государственное учреждение науки
Институт органической химии Уфимского научного центра РАН; г. Уфа
E-mail: *****@***ru
С целью изучения возможностей синтеза оптически активных лактонов среднего размера цикла мы использовали в качестве хирального источника левоглюкозенон.
Так, взаимодействием левоглюкозенона с морфолинцигексеном в EtOH получили аддукт Михаэля 2a,b. Обработка диастереомерных пар 2a,b HCl-MeOH сопровождается их превращением в три - 3а и тетраметилкетали 3b.
Расщепление пиридинийхлорхроматом (РСС) мостиков с кетальной функцией в голове моста соединений 3a,b привело к образованию среднециклического лактона 4.
Для синтеза потенциального цитотоксического N-метилуроканата действием NaBH4 восстановили деканолид 4 в спирт. Реакция сопровождается раскрытием лактонного кольца и этерификацией карбоксильной группы в этиловый эфир. Полученный дигидроксиэфир 5 ввели в реакцию этерификации с N-метилурокановой кислотой в описанных выше условиях. При этом произошла этерификация более активной первичной ОН-группы с образованием N-метилуроканата 7, представляющего собой ациклическую форму N-метилуроканата деканолида 4.
Схема 1
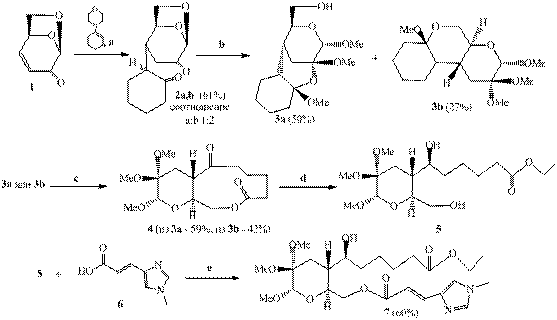
Реагенты и условия: a) 1. EtOH, 2. 3%-ный HCl в H2O; b) HCl-MeOH; с) PCC, CH2Cl2; d) NaBH4, EtOH; е) DCC, DMAP, CHCl3, кипячение.
Работа выполнена при финансовой поддержке гранта РФФИ-Поволжье “-р_поволжье_а”
УДК 573.6.086:582.28
, ,
ИССЛЕДОВАНИЕ ВЛИЯНИЯ ЛИГНОЦЕЛЛЮЛОЗНОГО СЫРЬЯ
НА ЛАККАЗНУЮ АКТИВНОСТЬ ГРИБОВ
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Уфимский государственный нефтяной технический университет, г. Уфа
E-mail: bio@rusoil.net
Лакказа (КФ 1.10.32, дифенол:кислород-оксидоредуктаза), катализирующая окисление различных органических соединений с одновременным восстановлением кислорода воздуха до воды без образования пероксида водорода, часто обнаруживается у грибных микроорганизмов.
Лакказа грибов играет важную роль в разложении растительных лигнинсодержащих материалов, гумификации органических остатков, а также выполняет функции образования плодовых тел, образования пигментов, детоксификации ксенобиотиков. Большинство грибов продуцирует несколько изоформ и изоферментов лакказ.
В качестве эффективных индукторов синтеза лакказы могут выступать их естественные субстраты, например, лигноцеллюлоза.
Целью работы являлось исследование влияния лигноцеллюлозного сырья (древесных опилок, травяной соломы, пшеничных отрубей) на лакказную активность грибов.
В работе исследованы условия культивирования базидиомицетов Russula vesca (сыроежка), Pleиrotus ostreatus (вешенка устричная), Agaricus arvensis (шампиньон) на жидких питательных средах в присутствии 2 % масс. опилок, соломы, отрубей в течение 20 сут.
Обнаружено, что исследуемые грибы проявляют максимум лакказной активности (42-37 ед/мл для Pleиrotus ostreatus и 16-22 ед/мл для Russula vesca) при росте на отрубях на 14-18 сутки.
При культивировании грибов и на средах с опилками максимальная лакказная активность наблюдается на 11-14 сутки роста и составляет 21-27 ед/мл для Pleиrotus ostreatus и 17-18 ед/мл для Russula vesca.
Внесение пирокатехина в концентрации 10-20 мкМ в качестве эффективного индуктора в среды с опилками и отрубями увеличивает активность лакказ Pleиrotus ostreatus и Russula vesca в 1,5-1,7 и 2,0-2,3 раза соответственно.
Синтез лакказы грибом Agaricus arvensis наблюдается на 5-е и 12-е сутки роста на среде с соломой и отрубями, однако при внесении пирокатехина лакказная активность проявляется на 3-4 сутки и возрастает в 8-11 раз по сравнению с контролем.
УДК
, ,
,
МИКРОВОЛОКНА СИНДИОТАКТИЧЕСКОГО 1,2-ПОЛИБУТАДИЕНА
Башкирский государственный университет, Инженерный факультет, г. Уфа.
Электроспиннинг является одним из наиболее перспективных методов получения полимерных нановолокон неограниченной длины путем растяжения струи полимерного раствора в электрическом поле. К достоинствам метода относятся его относительная технологическая простота и низкая стоимость, а также возможность создания волокон практически из любых растворимых полимеров.
Полимерные микро - и нановолокнистые нетканые материалы полученные методом электроспининга широко используются для очистки и фильтрации различных сред от примесей аэрозольных частиц, дисперсий, эмульсий и т. д., создания эффективных носителей каталитических систем при тонком химическом синтезе, в электронных устройствах в качестве сенсоров, в медицине для очистки и разделения крови.
Перспективным полимером для получения указанных материалов представляется синдиотактический 1,2-ПБ. Благодаря комплексу ценных свойств синдиотактический 1,2-ПБ находит широкое применение в резинотехнической, шинной, электротехнической, строительной, обувной отраслях промышленности, в производстве пластмасс и адгезивов. Полимер является физиологически безвредным, что определяет возможность его использования в медицине и фармацевтике.
На основе синдиотактического 1,2-ПБ методом электроспининга получены микроволокнистые нетканые материалы. Определены основные параметры получения нетканых материалов. Изучено влияние природы растворителя на тип и толщину получаемых волокон. Установлено, что наиболее подходящим растворителем для получения волокнистых материалов является хлористый метилен. Экспериментальные данные свидетельствуют о том, что наиболее тонкие волокна синдиотактического 1,2-ПБ (диаметр < 1 мк) с анизотропией по всей длине формируются при следующих условиях: концентрация полимера 3-4%, напряжение между флиерой и коллектором
13-15 кВ, расстоянии между флиерой и коллектором 19-22 см.
Предложены способы получения нетканых материалов на основе синдиотактического 1,2-ПБ. Показана возможность поверхностной модификации микроволокон синдиотактического 1,2-ПБ эпоксидными группами. Определены физико-механические свойства полученных образцов.
УДК 661.163
1, 1, 2
ФУНГИЦИДНАЯ АКТИВНОСТЬ СОЛЕЙ МЕТИЛОВОГО ЭФИРА
2-БЕНЗИМИДАЗОЛИЛКАРБАМИНОВОЙ КИСЛОТЫ С ЗАМЕЩЕННЫМИ БЕНЗОЙНЫМИ КИСЛОТАМИ.
1ГБУ РБ «Научно-исследовательский технологический институт гербицидов и регуляторов роста растений АН РБ», г. Уфа
E-mail: g. *****@***ru
2Уфимский государственный нефтяной технический университет, г. Уфа
Метиловый эфир 2-бензимидазолилкарбаминовой кислоты (БМК, карбендазим) используется в сельском хозяйстве в качестве фунгицидного препарата. Нами получены соли БМК с салициловой, бензойной, 3,6-дихлор-2-метоксибензойной кислотой (дикамба), 5-хлор-салициловой, 2-йодбензойной, 2-хлор-4-нитробензойной, п-хлорбензойной, о-хлорбензойной, сульфасалициловой и 2-аминобензойной кислотами. На их основе были приготовлены 30%-ные препаративные формы в виде пленкообразующих текучих паст, которыми обработаны зерна пшеницы. Сравнение эффективности полученных протравителей против комплекса семенной было осуществлено в лабораторных условиях. Результаты испытаний приведены в таблице.
Таблица - Фунгицидная активность солей БМК с бензойными кислотами на проростках пшеницы
Препарат | Норма расхода кг/т по преп. | Содер жание БМК, % масс. | Всхо-жесть семян, % | Пораженность корневыми гнилями, % | Эффектив- ность, % | Вес 100 пророст-ков, гр. |
Контроль | - | - | 88 | 23 | - | 12,0 |
БМК – эталон (очищ.) 30% т. п. | 1.7 | - | 91 | 2 | 91,3 | 12,5 |
БМК· салициловая кислота** 20% т. п. БМК· бензойная кислота, 30% т. п. БМК· дикамба***, 30 % т. п. БМК· 5Cl-салицило-вая к-та**, 30 %т. п. БМК·2-I-бензойная к-та, 30 % т. п. БМК·2-Сl-4-NO2-бензойная к-та БМК·п-Cl-бензой-ная к-та, 30 % т. п. БМК·сульфосалици-ловая к-та, 30 % т. п. БМК·о-бромбензой-ная к-та, 30 % т. п. БМК·2-аминобен-зойная к-та ,30 % т. п. | 0,8 0,5* 1,0 0,6 1,7 1,1 0,8 1,0 1,7 0,8 1,0 1,7 0,8 1,0 1,7 0,8 1,0 1,7 0,8 1,0 1,7 0,8 1,0 1,7 0,8 1,0 1,7 0,8 1,0 1,7 0,8 1,0 1,7 | 58,03 61,01 46,36 52,52 43,51 48,65 54,95 42,90 46,53 58,20 | 92 93 90 90 94 91 91 90 92 94 93 91 93 90 94 90 89 91 94 93 93 93 90 88 94 92 92 91 92 90 | 14 8 10 10 10 5 22 12 10 9 12 6 10 9 8 13 12 10 16 12 10 14 12 11 10 7 5 19 17 16 | 39,1 65,2 56,5 56,5 56,5 78,3 4,3 47,8 56,5 60.9 47.8 73,9 56,5 60,9 65,2 43,5 47,8 56,5 30,4 47,8 56,5 39,1 47,8 52,2 52,2 69,6 78,3 17,4 26,1 30,4 | 12,4 12,6 12,5 12,7 13,0 12,6 12,7 13,1 13,2 12,8 12,9 13,0 12,9 12,7 12,8 12,7 11,9 13,0 12,6 12,0 12,2 12,9 12,4 12,3 12,3 12,0 12,0 12,1 12,4 12.2 |
*- норма расхода семян в пересчете на 30% форму
**- густая паста
***- паста не растворяется при обработке семян
Наилучшие результаты в испытаниях показали соли БМК с
5-хлорсалициловой и о-бромбензойными кислотами. Использование солей при приготовлении препаративных форм позволяет существенно снизить в них дозу карбендазима.
УДК
, ,
Ферментативный гидролиз карбамида в составе композиции ПАВ для снижения вязкости нефти
Федеральное государственное бюджетное учреждение науки
Институт химии нефти СО РАН, Томск
e-mail:shagabieva1412@mail.ru,
В настоящее время существует целый спектр технологий добычи вязких нефтей для залежей с высокой температурой, но для низкотемпературных месторождений вязкой нефти эффективными являются энергоемкие и экономически затратные термические методы.
Для повышения вытеснения нефти из пласта разработаны и применяются десятки композиций с высокими моющими свойствами. Одним из компонентов композиций является карбамид, который в пластовых условиях, при температуре свыше 80 °С гидролизуется с образованием углекислого газа и аммиака [1,2]. Аммиак образует щелочную буферную систему с рН=9.0, что повышает моющие свойства композиции, стимулирует десорбцию нефти с пористой породы пласта и увеличивает нефтеотдачу. Углекислый газ растворяется в нефти, тем самым снижает ее вязкость, что увеличивает ее вытеснение из пласта.
В условиях низких температур (20‑40 °С) гидролиз карбамида с выделением СО2 и аммиака катализирует фермент уреаза, что позволяет использовать ее при создании биотехнологии увеличения нефтеотдачи низкотемпературных залежей [3]. Источниками уреазы служат бобовые культуры (соя), свекла и кизяки животных.
Нами разработаны основы комплексного физико-химического и микробиологического метода увеличения нефтеотдачи с применением раствора композиции ПАВ, содержащей карбамид и природные источники уреазы микробиального или растительного происхождения.
Активность гидролиза карбамида оценивали по изменению pH, концентрации карбамида, накоплению CO2 и аммиака в растворе композиции с добавлением природных источников уреазы и уробактерий. Для сравнения гидролиз карбамида проводили при добавлении кристаллической уреазы. При гидролизе карбамида максимальное значение pH 9.3 ед. получено при оптимальном соотношении фермент - субстрат 0.1:32 в течение 2 часов.
Из растительных объектов высокую уреазную активность проявляет кожура свеклы, содержащая уреазу и группу уробактерий, численность который достигает 3.2 ·109 клет/г. Максимальное значение pH 9.4.
Таким образом, уреаза природных источников растительного и бактериального происхождения (соевая мука, свекла, кизяки домашних животных) проявляет высокую активность в процессах гидролиза карбамида с выделением СО2, снижающего вязкость нефти, и NН3, повышающего рН и моющие свойства композиции, что способствует вытеснению вязкой нефти из пласта.
Полученные данные служат научной основой для разработки комплексного физико-химического и микробиологического метода увеличения нефтеотдачи вязкой нефти низкотемпературных залежей.
Работа выполнена при финансовой поддержке Государственного контракта № П514 Федеральной целевой программы «Научные и научно - педагогические кадры инновационной России» на годы и гранта РФФИ № Монг_а.
Список литературы:
1 Сваровская комплексного микробиологического и физико-химического метода увеличения нефтеотдачи / , , // Интервал. – 2001. – № 9. – С. 52-53.
2 Абрамзон -активные вещества. Ленинград: изд-во Химия, 1981. – 303 с.
3 X. Ферментативная активность. Ф. X. Хазиев. – М.: Знание, 1976. – 322 с.
4 Svarovskaya L. bined physico-chemical and microbiological EOR method / L. I. Svarovskaya, L. K.Altunina, Z. A. Rozhenkova // Proceedings of the 10th European Symposium "Improved Oil Recovery". – Brighton, Unaited Kingdom, August 18-– Report N 038.6 pages.
5 Горелова метод определения карбамида в водных, спиртоводных и углеводородных растворах / , , // Заводская лаборатория. – 1992. – № 11. – С. 14-16.
6 Большой практикум по микробиологии под ред. . – М.: Высшая школа, 1962. – 491с.
7 Нефтяная микробиология: пер. с англ. Э. Бирштехер. – СПб.: Гостоптехиздат, 1957. – 314 с.
УДК 544.473:577.15
, ,
ПОИСК БИОКАТАЛИЗАТОРОВ ДЛЯ ВОССТАНОВЛЕНИЯ
п-МЕТОКСИАЦЕТОФЕНОНА
Уфимский государственный нефтяной технический университет, г Уфа
E-mail: *****@***net
Оптически активный (S)-1-(4-метоксифенил)этанол является ключевым синтоном в синтезе циклоалкил[b]индолов, которые могут быть использованы при лечении аллергических реакций [1, 2]. Перспективным подходом к получению этого энантиомера является биовосстановление его прохирального предшественника (п-метоксиацетофенона) с помощью микроорганизмов.
С целью создания эффективного метода получения
(S)-1-(4-метоксифенил)этанола на первом этапе исследований осуществлен поиск продуцентов оксидоредуктаз, способных восстанавливать п-метоксиацетофенон в высокой концентрации (5 г/л).
Трансформацию п-метоксиацетофенона проводили при при 35°С в 0.1 М фосфатном буфере (рН 7), содержащем 10% изопропанола, 5 г/л субстрата и 0.3 г/л биомассы микроорганизмов, при перемешивании в течение 36-72 ч. В результате тестирования 15 дрожжевых культур из коллекции кафедры биохимии и технологии микробиологических производств Уфимского государственного нефтяного технического университета были выявлены 3 культуры базидиомицетных дрожжей (Р-3,
ГБ-3, ГБ-4), трансформирующих п-метоксиацетофенон в
1-(4-метоксифенил)этанол с выходом продукта 51-85%.

Таким образом, найдены перспективные микроорганизмы, способные осуществлять восстановление п-метоксиацетофенона при его концентрации в растворе 5 г/л. Показано, что для получения энзиматически активной биомассы найденных перспективных микроорганизмов в качестве доступного сырья может быть использован глицерин – отход производства биодизеля.
Список использованной литературы
1. Hillier C., Marcoux J. F., Zhao D. L., Grabowski E. J.J., Mckeown A. E., Tillyer R. D. // J. Org. Chem.- 2005.- V. 70.- P. 8385
2. Hillier C., Desrosiers J. N., Marcoux J. F., Grabowski E. J.J. // Org. Lett.- 2004.- V. 6.- P. 573
УДК 544.473:577.15
, ,
РАЗРАБОТКА МЕТОДА ПОЛУЧЕНИЯ ОПТИЧЕСКИ ЧИСТОГО
(S)-2-БРОМ-1-(4-НИТРОФЕНИЛ)ЭТАНОЛА
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Уфимский государственный нефтяной технический университет, г. Уфа
E-mail: *****@***net
(S)-2-бром-1-(4-нитрофенил)этанол является предшественником в синтезе (S)-соталола – соединения, обладающего способностью блокировать
β-адренергические рецепторы и используемого для лечения сердечно-сосудистых заболеваний [1]. (S)-Соталол также применяется для лечения астмы и бронхита [2]. Терапевтическими свойствами обладает только (S)-энантиомер соталола. В связи с этим создание стереонаправленного метода синтеза оптически чистого (S)-2-бром-1-(4-нитрофенил)этанола является актуальной задачей.

В результате скрининга микроорганизмов, способных катализировать энантиоселективное ацетилирование 2-бром-1-(4-нитрофенил)этанола винилацетатом, найдены культуры микроорганизмов Rhodococcus sp. 77-32s, Rhodococcus sp. 78-5 и Bacillus sp. 77-34, в присутствии которых преимущественно ацетилируется (R)-2-бром-1-(4-нитрофенил)этанол.
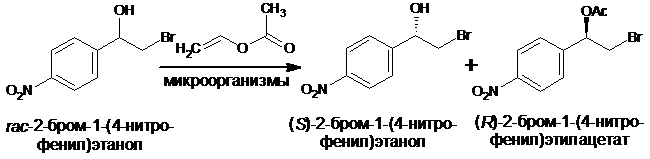
Установлено влияние состава среды культивирования микроорганизмов на активность и энантиоселективность клеточных катализаторов. На основе обезвоженной ацетоном биомассы Rhodococcus sp. 77-32s, выращенной на среде с содержанием 3оБ сусла, создан биокатализатор, способный трансформировать ~50% рацемического спирта с преимущественным образованием (R)-2-бром-1-(4-нитрофенил)этилацетата с оптической чистотой 60,3 % ее. Оптическая чистота остаточного спирта, в котором преобладает (S)-энантиомер, составляет 62,7 % ее.
Список литературы:
1 Agustian J., Kamaruddin A. H., Bhatia S. // Process Biochemistry.- 2010.- V. 45.- P. 1587
2 Kapoor M., Anand N., Ahmad K., Koul S., Chimni S. S., Taneja S. C., Qazi G. N. // Tetrahedron: Asymmetry.- 2005.- V. 1
УДК 577.3.001.57
,
ИССЛЕДОВАНИЕ ПРОЦЕССА БИОДЕГРАДАЦИИ ХЛОРФЕНО-ЛОВ
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Уфимский государственный нефтяной технический университет, г. Уфа
E-mail: *****@***ru
С целью эффективной биодеградации хлорпроизводных фенолов была выделена культура микроорганизмов-деструкторов, способных потреблять хлорфенолы максимальной начальной концентрации 250 мг/л.
Через 7 дней после начала культивирования микроорганизмов в качалочных колбах наблюдается окрашивание раствора в малиновый цвет. Причем, окрашивание наблюдалось в колбах с начальными концентрациями хлорфенолов от 100 до 250 мг/л с увеличением интенсивности окрашивания пропорционально концентрации. Пигменты у многих микроорганизмов представляют собой вторичные метаболиты; это означает, что они не принадлежат к тем соединениям, которые имеются у всех этих организмов [1]. Мы предположили, что пигментация может быть связана с образованием фенолами, находящимися в среде в большой концентрации, соединений с компонентами клеток микроорганизмов.
Подобные явления были замечены и в других исследованиях. Так в опытах по утилизации высоких концентраций нетепродуктов культурой микроорганизмов рода Pseudomonas fluorescens отмечалось выделение насыщенного желто-зеленого пигмента в питательную среду через 12 часов после начала культивирования [2]. Как и в нашем случае, возможно, это связано с активизацией окисляющих путей метаболизма и адаптативной способностью штамма к повышенной концентрации субстрата.
Такие основные признаки, как: Грам(-), форма клеток, цвет колонии, аэробное окисление углеводов, гидролиз крахмала, разжижение желатины, рост на синтетической среде, каталазная активность согласно определителю Берги, позволяют предположить, что культура относится к роду Pseudomonas [1]. Выделение в среду нефлуоресцирующего пигмента и сравнение физиолого-биохимических признаков позволяет с большой долей вероятности считать выделенный штамм относящимся к виду Pseudomonas сepacia.
Список литературы:
1 Хоулт Дж. Определитель бактерий /Дж. Берджи Хоулт, Н., Снит. — М., 1997.
2 Станкевич, углеводородокисляющих бактерий рода Pseudomonas для биоремедиации нефтезагрязненных почв: дис. канд. биол. наук: защищена 03.05.2002; утв. 05.07.2002; . – Москва, 2002 – 132с.
УДК 579.66
, ,
ПОИСК ДРОЖЖЕЙ - ПРОДУЦЕНТОВ КАРБОКСИЭСТЕРАЗ И ЭКЗОПОЛИМЕРОВ НА ГЛИЦЕРИНЕ
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Уфимский государственный нефтяной технический университет, г. Уфа
E-mail: *****@***ru
Перспективными направлениями в переработке глицерина – отхода производства биодизеля является микробиологический синтез ферментов и полимеров с помощью микроорганизмов.
К практически важным ферментам относятся карбоксиэстеразы, которые катализируют реакции расщепления эфирной связи в сложных эфирах, проявляя широкую субстратную специфичность, высокую регио - и энантиоселективность, что позволяет их использовать в качестве эффективных биокатализаторов для получения оптически активных соединений методами биотрансформации. Ферменты стабильны и проявляют высокую активность в органических растворителях, используемых для трансформации гидрофобных соединений.
Особый интерес представляют продуценты внутриклеточных карбоксиэстераз, на основе которых могут быть созданы экономичные биокатализаторы, представляющие собой целые или пермеабилизованные клетки микроорганизмов. Рациональная переработка остатка культуральной жидкости после удаления из нее энзиматически активной биомассы, позволит получать дополнительные практически важные продукты и снизить затраты на приготовление биокатализатора.
Известно, что микроорганизмы способны продуцировать экологически безопасные внеклеточные полимеры, которые могут заменить токсичные синтетические флокулянты, эмульгаторы, ПАВы, загустители, широко используемые в различных отраслях промышленности. Получение внеклеточных полимеров и клеточных катализаторов в одном биотехнологическом процессе может быть экономически целесообразным.
С целью разработки такого процесса в настоящей работе осуществлен поиск культур дрожжей из коллекции микроорганизмов УГНТУ, способных при росте на глицерине одновременно продуцировать экзополимеры и внутриклеточные карбоксиэстеразы.
В результате исследования гидролиза этилацетоацетата микроорганизмами выявлены 13 культур, проявляющих карбоксиэстеразную активность. Обнаружено, что 5 культур накапливают в среде внеклеточные полимеры, осаждаемые органическими растворителями (этанолом, ацетоном).
Таким образом, были найдены перспективные штаммы, обладающие эстеразной активностью, и способные синтезировать экзополимеры в процессе роста на глицеринсодержащих средах.
УДК 547.917
, ,
СИНТЕЗ 2-((1R,5R,6S)-6-(1,3-ДИТИАН-2-ИЛ)-5-МЕТИЛЦИКЛОГЕКС-3-ЕНИЛ)ЭТАНОЛА – ПЕРСПЕКТИВНОГО ХИРАЛЬНОГО СИНТЕТИЧЕСКОГО БЛОКА ДЛЯ АНАЛОГОВ ЭЛЕУТЕЗИДОВ
Федеральное государственное учреждение науки
Институт органической химии Уфимского научного центра РАН, г. Уфа
e-mail: *****@***ru
С целью выхода к базовым соединениям для получения аналогов элеутезидов [1] на основе аддуктов Дильса - Альдера в качестве модельного соединения выбран аддукт левоглюкозенона и пиперилена 1. Так, углеводную часть в аддукте левоглюкозенона с пипериленом 1 в 10 стадий трансформировали с общим выходом 22% в 2-((1R,5R,6S)-6-(1,3-дитиан-2-ил)-5-метилциклогекс-3-енил)этанол 10 – ключевой синтон в синтезе аналогов элеутезидов, модифицированных по циклу А [1, 2].
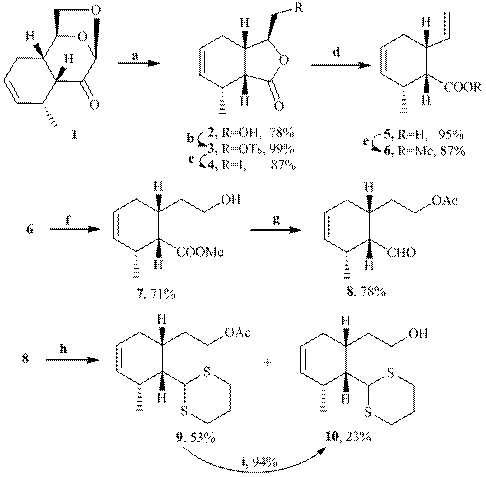
Реагенты и условия: a) H2O2, EtOH, H2SO4, 70oC; b) p-TsCl, Py; c) NaI, MeCN; d) Zn, AcOH, MeOH; e) MeI, K2CO3, Me2CO; f) 1) 9-BBN, THF; 2) 30%-H2O2, NaOAc; g) 1) p-TsOH, CH2Cl2; 2) ДИБАГ, CH2Cl2, -78oC; 3) Ac2O, Py; h) CH2(CH2SH)2, BF3·Et2O, -78oC; i) KOH, EtOH, H2O.
Работа выполнена при финансовой поддержке гранта РФФИ-Поволжье “-р_поволжье_а”
Список литературы:
1 Nicolaou K. C., Winssinger N., Vourlomis D., Ohshima T., Kim S., Pfefferkorn J. JACS. 1998. V.120. P.10814
2 Chen X-T., Gutteridge C. E., Bhattacharya S. K., Zhou B., Pettus Thomas R. R., Hascall T., Danishefsky S. J. A. Angew. Chem. Int. Ed. 1998. V.37. P. 185.
УДК 547.917
, ,
РЕАКЦИЯ ДИЛЬСА-АЛЬДЕРА ЛЕВОГЛЮКОЗЕНОНА С ЦИКЛОПЕНТАДИЕНОМ В ВОДНЫХ УСЛОВИЯХ
Федеральное государственное учреждение науки
Институт органической химии Уфимского научного центра РАН, г. Уфа
e-mail: *****@***ru
Известно, что реакция Дильса-Алдера левоглюкозенона 1 с циклопентадиеном в кипящем хлорбензоле приводит к смеси аддуктов 2 и 3 с выходами 65% и 16.5% соответственно [1]. В препаративном отношении более предпочительна катализируемая ZnCl2 реакция Дильса-Альдера позволяющая получить с выходом 75% эндо-изомер 2 без примеси второго [2].
Исследования показали, что при проведении реакции Дильса-Альдера в водных условиях скорость может увеличиваться до 1000 раз, а также возрастать региоселективность процесса [3].
В данной работе нами изучена реакция циклоприсоединения левоглюкозенона 1 с циклопентадиеном. Так реакция в воде в присутствии LiCl, проходила за 4 часа, но выход составил 53%. Использование смеси вода-изопропанол (1:1) позволило увеличить выходы аддуктов 2, 3 до 70%, реакция проходила за 6 часов, содержание второго экзо-изомера не более 10%.
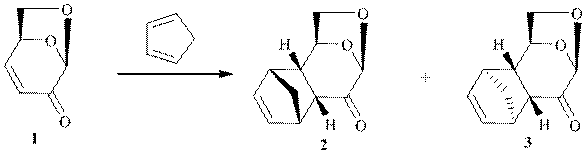
Работа выполнена при финансовой поддержке гранта РФФИ-Поволжье “-р_поволжье_а”
Список литературы:
1 Bhate P., Horton D. Car. Res. 1983. V.122. P.189-199
2 , , Мифтахов . орг. хим. 1992. т.28. с.2072.
3 Fringuelli F., Taticchi A. The Diels-Alder Reaction: Selected Practical Methods. John Wiley & Sons 20р.
УДК 541.64
ИЗУЧЕНИЕ ДИФФУЗИИ ЛЕКАРСТВЕННОГО ВЕЩЕСТВА ИЗ ХИТОЗАНОВЫХ ПЛЕНОК
Башкирский государственный университет, г. Уфа
e-mail: anzhela_murzagil@mail.ru
В последние десятилетия проводятся интенсивные исследования полимерных систем для контролируемого высвобождения биологически активных веществ. Применение полимерных систем для контролируемого высвобождения в качестве пленок позволяет дозировано и целенаправленно вводить в организм препарат. Используя форму лекарственного препарата, можно варьировать время контролируемого высвобождения, что повышает эффективность биологически активного вещества. Уникальные свойства аминополисахарида хитозана (ХТЗ) – биосовместимость с тканями организма, бактериостатичность, способность усиливать регенеративные процессы при заживлении ран, биодеградируемость, а также способность к пленкообразованию, предопределяют возможность использования ХТЗ в качестве пленочных покрытий пролонгированного действия.
При создании таких систем важно уметь управлять транспортными свойствами полимерной матрицы. Подходы, позволяющие регулировать скорость перехода лекарственного вещества из пленочного покрытия, были установлены ранее. Это, в первую очередь, термическое модифицирование пленок и во-вторых, обработка пленки мицеллярным раствором ПАВ, например, додецилсульфатом натрия (ДСН). И термическое модифицирование, и обработка раствором ПАВ, сказываются как на диффузии биологически активного вещества из матрицы, так и на сорбции полимерной матрицей паров воды. Была изучена система хитозан – лекарственное вещество, подвергнутая обработке мицеллярным раствором ДСН. В качестве лекарственного вещества были использованы антибиотики – цефазолина натриевая соль (ЦФЗ) и хлорид амикацина (АМХ). Хитозановые пленки были сформированы из раствора 1% уксусной кислоты. Концентрация полимера в исходном растворе составляла 1,0 г/дл. Толщина пленок во всех экспериментах поддерживалась постоянной и равной 0,1 мм. Антибиотик в виде водного раствора вносился в раствор ХТЗ непосредственно перед формированием пленки. Концентрация лекарственного соединения в пленке - 0,1 моль на моль ХТЗ. Пленки хитозана подвергались изотермическому отжигу при 1200С в течении 15, 30, 60 и 120 минут. Кинетику высвобождения лекарственного вещества измеряли с помощью спектрофотометра «Specord-М 80».

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 |




