Объем потребления флокулянтов с каждым годом растет. Поэтому встает вопрос об их удешевлении либо повышении их эффективности.
Достаточно дешевым флокулянтом на сегодняшний день является полиэлектролит ВПК-402. Основным недостатком на сегодня является содержание в нем соли – хлорида натрия, негативно влияющего на процесс флокуляции. По этой причине важным является решение данной проблемы.
Образование соли происходит при взаимодействии диметиламина и аллилхлорида в присутствии щелочи с получением мономера для синтеза полиэлектролита – диаллилдиметиламмонийхлорида (ДАДМАХ) – согласно уравнению:
2 С3Н5С1 + (СН3)2NH + NaOH → [(СН3)2N(C3H5)2]+C1- + NaC1 + H2О
Одним из простых методов снижения содержания соли является его выкристаллизовывание путем концентрации раствора мономера с последующим фильтрованием. Однако данный способ является малоэффективным, так как излишнее концентрирование приводи к выпадению в осадок вместе с хлоридом натрия и мономера. Предложенный вариант позволяет снизить содержание соли лишь на 2-3%.
Существует вариант обессоливания путем разделения синтеза мономера диаллилдиметиламмонийхлорида на 3 стадии:
1. Синтез аллилдиметиламина взаимодействием диметиламина и аллилхлорида при мольном соотношении 1 : 1,05;
2. Ректификационное выделение аллилдиметиламина;
3. Синтез диаллилдиметиламмонийхлорида взаимодействием аллилдиметиламина и аллилхлорида при мольном соотношении 1 : 1,05.
Однако данный метод является энергоемким и является актуальным подбор метода, позволяющего проводить очистку от соли при низких температурах.
В качестве такого предлагается метод экстрактивного выделения мономера из получаемой в ходе синтеза реакционной массы.
В качестве экстрагентов были испытаны различные органические соединения. Результаты экспериментов свидетельствуют о весьма плохом растворении мономера в неполярных растворителях. Хлорорганические растворители также не дали удовлетворительных результатов по извлечению ДАДМАХ из водного раствора. Подобрано несколько экстрагентов, позволяющих извлечь заметные количества мономера из раствора. Однако попытки полимеризовать ДАДМАХ в среде экстрагента не увенчались успехом. Поэтому была предложена обратная экстракция мономера обессоленной водой. В результате полимеризации мономера в водном растворе получен продукт с содержанием соли, в пересчете на сухоевещество, около 1 % против исходных 24 %-ного. При этом в этот 1% вносится также и вклад продуктов разложения инициатора – персульфата калия. Поэтому возможно снижение содержания соли в товарном продукте за счет его замены на другие инициаторы, например, пероксид водорода, дающий при разложении воду.
Список литературы:
1 Воюцкий коллоидной химии. Л.: Химия – 1975, 513 с.
УДК + 543 42
, ,
ИЗУЧЕНИЕ МОЛЕКУЛЫ (Е)-6-АЦЕТИЛ-3-(2-ГИДРОКСИ-5-МЕТИЛФЕНИЛ)-5-СТИРИЛ ЦИКЛОГЕКСЕН-1-ОНА МЕТОДОМ ЯМР
Бакинский государственный университет, Азербайджан, г. Баку
E-mail:bsu.nmrlab@mail.ru
Изучение с помощью спектроскопии ядерного магнитного резонанса (ЯМР) динамики молекул в растворе дает ценную информацию о реориентации молекул, быстром внутримолекулярном вращении, пространственных и других взаимодействиях, образованиях молекулярных ассоциатов за счет водородной связи и т. д.
Как известно, халконы и их производные обладают некоторыми медико-биологическими свойствами. Вследствие этого, на основе них получают лекарственные средства для лечения сердечных заболеваний, нервно-сосудистых проблем, язвы желудка, свертывания крови, спазма, диабета, рака.
Учитывая вышеуказанные, на основе халкона (2Е, 4 Е )-1-(2-гидрокси-5-метилфенил)-5-фенил-2,4-пентадиен-1-она (I) был синтезирован (Е)-6-ацетил-3-(2-гидрокси-5-метилфенил)-5-стирил циклогексен-1-он (II) и были изучены его различные растворы методом ЯМР.

Исследования, проводимые в ацетоне-d6, ДМСО-d6, метаноле-d4, выявили наличие таутомерных переходов в растворах. На основе исследований с помощью ЯМР, в зависимости от температуры и времени, для (Е)-6-ацетил-3-(2-гидрокси-5-метилфенил)-5-стирил циклогексен-1-она (II) было доказано существование нижеуказанного таутомерного перехода от вероятных трех форм.
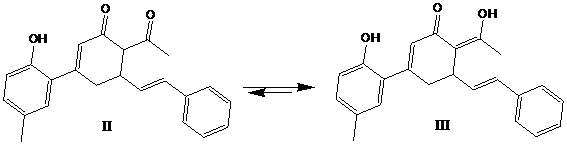
В отличие от вышеуказанных, в растворе хлороформа-d1 таутомерные переходы происходят частично, а в растворе четыреххлористого углерода практически не происходят.
Существование вышеуказанных таутомерных форм в растворе также было доказано химическим путем. Учитывая данные, полученные с помощью ЯМР, можно получить различные соединения в указанных растворителях. На основе соединения (III) нами были получены ряд гетероциклических соединений.
УДК + 543 42
, ,
ИЗУЧЕНИЕ МОЛЕКУЛ 6-МЕТИЛ-2-ФЕНИЛ-2,3-ДИГИДРО-4Н-ХРОМЕН-4-ОНА И 6-МЕТИЛ-2-(4-НИТРОФЕНИЛ)-2,3-ДИГИДРО-4Н-ХРОМЕН-4-ОНА (ФЛАВАНОНЫ) МЕТОДОМ ЯМР
Бакинский государственный университет, Азербайджан, г. Баку
E-mail: bsu. *****@***ru
Изучение различных процессов (обратимые реакции, обменные процессы, образование водородных связей, пространственные и другие взаимодействия, протекающие в растворе) методом ЯМР имеет теоретическое и практическое значение. Химики и биохимики широко используют современные возможности ЯМР для изучения молекулярных систем в растворах. Мы применили этот метод для изучения молекул 6-метил-2-фенил-2,3-дигидро-4Н-хромен-4-она (I) и 6-метил-2-(4-нитрофенил)-2,3-дигидро-4Н-хромен-4-она (II), полученных на основе 2-гидрокси-5-метилацетофенона.
Как известно, флаваноны являются гетероциклическими соединениями природного происхождения и обладают биологической и фармакологической активностью.
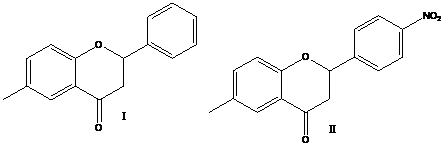
Для соединения 6-метил-2-фенил-2,3-дигидро-4Н-хромен-4-она (I), проводимые исследования методом ЯМР в растворах ацетона-d6 и ДМСО-d6 в зависимости от температуры (20- 90°C) и времени (10 дней), не выявили протекaние каких-либо динамических процессов.
А исследования молекулы 6-метил-2-(4-нитрофенил)-2,3-дигидро-4Н-хромен-4-она (II) в вышеуказанных растворителях при определенных условиях привели к интересным результатам. Так, исследования в растворах сухого ацетона-d6 (8-10 дней) и ДМСО-d6 (4-5 дней), содержащего 0,3% остаточной воды, показали самопроизвольное раскрытие пиронового кольца при 22°C и образование нового соединения (III), содержащего две внутримолекулярные водородные связи.

Самопроизвольное раскрытие пиронового кольца при 22°C можно объяснить наличием нитрогрупп, поляризующих молекулу флавонона, и воздействием кристаллической воды на соединение. По сравнению с ацетоном-d6 , относительно быстрое самопроизвольное раскрытие пиронового кольца в ДМСО-d6 объясняется тем, что молекула растворителя более полярна и содержит 0,3% остаточной воды. Методом ЯМР была вычислена энергия внутримолекулярной водородной связи (7.81 ккал/моль или 32.72 кДж/моль), образованная между фенольным гидроксидом и кислородом карбонильной группы.
УДК 620.193.4:665.73
,
ИССЛЕДОВАНИЕ ВЛИЯНИЯ НА КОРРОЗИОННУЮ АКТИВНОСТЬ ТОПЛИВ И МЕТОДЫ ЕЕ ОЦЕНКИ
ФГБОУ ВПО Уфимский государственный нефтяной технический университет, *****@***ru
Перспективными компонентами топлив для двигателей внутреннего сгорания (ДВС) являются оксигенаты - кислородсодержащие соединения (эфиры, спирты и их смеси), которые вовлекают в автомобильные бензины в качестве антидетонационных добавок. Однако применение кислородсодержащих соединений требует решения ряда проблем, связанных прежде всего с их коррозионной активностью по отношению к металлам. Поэтому проблема коррозионной активности таких топлив приобрела особую актуальность.
Для оценки защитных свойств бензинов в настоящее время используют два показателя: коррозионную активность в условиях конденсации воды, коррозионную активность в присутствии электролита.
Коррозионная активность топлив в условиях конденсации воды определяется по методу, предложенному (ГОСТ ). Особенность этого метода - приближение условий испытания к реальному проявлению защитных свойств топлива при конденсации растворенной воды за счет перепада температуры.
Коррозионная активность в присутствии электролита позволяет более дифференцированно оценить защитные свойства бензинов, обладающих малой коррозионной активностью в условиях конденсации воды, что очень важно при подборе и исследовании эффективности ингибиторов коррозии. Метод оценки разработан и К А. Демвденко.
Недостаток этих методов заключается в использовании металлической пластинки с малой площадью удельной поверхности (~0,0000042 м2), в то время, когда нами была разработана методика определения коррозионной активности с площадью рабочей поверхности пластинок (~0,0002 м2). Это позволило увеличить точность получаемых данных. К тому же конструкция аппарата дает возможность оценивать влияние различных параметров проведения анализа, как в отдельности, так и в совокупности друг с другом, на получаемые результаты.
Дальнейшее направление исследования будет направлено на определение влияния добавок оксигенатов и гидрогенезатов на коррозионную активность товарных бензинов.
Список литературы:
1 ГОСТ . Коррозионная активность топлив в условиях конденсации воды.
УДК 547.665
, ,
ПОИСК НОВЫХ СЫРЬЕВЫХ ИСТОЧНИКОВ ДЛЯ ПОЛУЧЕНИЯ ПИРЕТРОИДНЫХ ИНСЕКТИЦИДОВ
Уфимский государственный нефтяной технический университет
E-mail: *****@***ru
В результате многолетних исследований природных инсектицидов пиретринов химикам удалось получить фотостабильные синтетические аналоги - пиретроиды, пригодные для использования в сельском хозяйстве [1].
Ассортимент пиретроидов ежегодно расширяется, и в настоящее время они преобладают в мировом масштабе среди средств защиты растений от вредителей. Одним из перспективных в плане внедрения является инденсодержащий инсектицид – ципотрин [2].
Ранее был проведен синтез ципотрина на основе индена по следующей схеме [3].
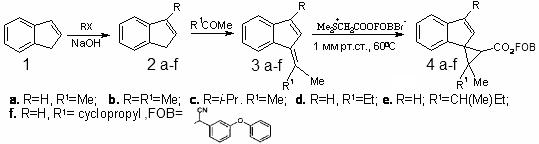
Нами было определено, что недорогим и достаточно распространенным источником индена является инден-кумароновая фракция, получаемая на коксохимических производствах. Эта фракция входит в состав тяжелого бензола, выкипающая при температуре 160–190°С.
Однако вследствие того, что весной этого года КХП Нижнетагильского МК было закрыто, сбыт данного продукта прекратился. Поэтому следующим этапом поиска сырьевого источника мы предполагаем идентификацию индена и определение его содержания во фракции 170-190°С смолы пиролиза и фракции пиролиза С-9 .
Список литературы:
1 Патент США № 000
2 Eliott M., Janes N. F. // Chem. Soc. Rev., 473-
3 , , . // Ж. Орг. химии, 25, 1202-1
УДК 665.63.048.390
, ,
ИССЛЕДОВАНИЕ ПРОЦЕССА ТЕПЛОПЕРЕДАЧИ В ТЕПЛООБМЕННИКЕ ТИПА «ТРУБА В ТРУБЕ»
Уфимский государственный нефтяной технический университет, г. Уфа
E-mail:donzraikiri@mail.ru
Теплообменные аппараты типа «труба в трубе» универсальны по сфере применения и предназначены для теплообмена между технологическими средами с температурой от минус 30°С до плюс 400°С в химической, нефтехимической, нефтеперерабатывающей, газовой, металлургической и других отраслях промышленности. Ввиду их широкого использования, было проведено исследование процесса теплопередачи в данной конструкции теплообменников.
Теплообменники данного типа эффективно работают при небольших расходах теплоносителей и при высоких давлениях. Достаточно высокие скорости жидкости в аппаратах данного типа достигаются, благодаря небольшим поперечным сечениям трубного и межтрубного пространства даже при небольших расходах. Исследуемые аппараты используются главным образом для охлаждения или нагревания в системе жидкость-жидкость, когда расходы теплоносителей невелики и последние не меняют своего агрегатного состояния.
Благодаря небольшому поперечному сечению трубного и межтрубного пространства в теплообменниках данной конструкции достигаются довольно высокие скорости движения жидкостей, значения которых на прямую влияют на интенсивность теплообмена. Таким образом, увеличение скорости движения теплоносителей позволяет получать и высокие коэффициенты теплопередачи и значения теплонапряженности поверхности нагрева. В таких аппаратах легче обеспечить противоток между тепло-обменивающимися средами.
Целью работы являлось изучение основных закономерностей процесса теплопередачи в поверхностном теплообменном аппарате с использованием уравнения теплового баланса, учитывающего теплообмен свободной конвекцией между окружающей средой и наружной поверхностью теплообменника.
В данной работе был рассмотрен случай процесса теплопередачи без изменения агрегатного состояния при вынужденном движении теплоносителей внутри труб и в кольцевом канале.
Для чистоты протекания эксперимента опыты необходимо проводить при установившемся режиме течения теплоносителей и постоянной температуре теплоносителей на входе в теплообменный аппарат.
Уравнение теплового баланса с учетом подвода тепла от окружающей среды выражают равенством:
![]() , (1)
, (1)
где Q – тепловая нагрузка теплообменного аппарата, Вт; Q1 и Q2 – тепловая нагрузка горячего и холодного теплоносителей, Вт; Q3 – подвод тепла от окружающей среды за счет свободной конвекции, Вт,
![]() (2)
(2)
![]() (3)
(3)
где V1, V2 – объемные расходы теплоносителей, м3/с; ρ1, ρ2 – плотности теплоносителей, кг/м3; с1, с2 – удельные теплоемкости теплоносителей; t1н, t1к, t2н, t2к – температуры теплоносителей, ºС,
![]() (4)
(4)
где α3 – коэффициент теплообмена свободной конвекцией, Вт/(м2·град);
F – наружная поверхность теплообменника, м2; Δt – разность температур стенки и упругой жидкости, ºС.
Эксперимент проводили для 16 точек различных схем движения теплоносителей (прямоток и противоток) при различных расходах теплоносителей с регистрацией начальной и конечной температур потоков и учетом изменения температуры окружающей среды. В качестве теплоносителей использовались горячая и холодная вода.
В результате проведенных экспериментов, выполнения расчетов и построения графических зависимостей было доказано, что холодный теплоноситель принимает тепло от воздуха, подводимого к наружной поверхности теплообменника за счет свободной конвекции. При этом установлено и доказано, что загрязнение труб оказывает существенное влияние на данный процесс и на величину коэффициента теплопередачи. Это объясняется низким значением тепловой проводимости загрязнений стенок труб и их высоким термическим сопротивлением.
Список литературы:
1 , , Молоканов и аппараты нефтеперерабатывающей и нефтехимической промышленности. – М.: Химия, 1982.-584 с.
2 Зиганшин процессы. Лабораторный практикум по курсу «Процессы и аппараты химической технологии».– Уфа: УГНТУ. 199с.
УДК 547.525.5
,
РАСЧЕТ ЭНЕРГИИ ДЕЛОКАЛИЗАЦИИ БЕНЗОЛА
Уфимский государственный нефтяной технический университет, г. Уфа
Ароматичность ― проявление электронной делокализации в циклических молекулах, что приводит к снижению энергии молекулы и ряду необычных химических и физических свойств. Возможность существования ароматических систем обусловлена тем, что циклическая делокализация π-электронов повышает термодинамическую стабильность молекулы, снижая величину ее внутренней энергии. Мерой энергетической оценки ароматичности служит энергия резонанса Ерез – разница между энергиями ароматической молекулы и молекулы с локализованными связями. В тоже время, ароматическая молекула и молекула с делокализованными связями не являются тождественными понятиями [1, 2] Энергия делокализации не соответствует эмпирической энергии резонанса, так как она основывается на гипотетической модели локализации с геометрией, идентичной геометрии делокализованной системы. Для того чтобы установить соотношение между ними, необходимо от эмпирической энергии резонанса отнять энергию, необходимую для сжатия структуры с чередующимися простыми и кратными связями до структуры с не чередующимися связями:
Ерез = Есж + Едел
где Есж – энергия сжатия структуры;
Едел – энергия делокализация связей.
Эта энергия деформации, рассчитанная для бензола, равна
Есж = –27 ккал/моль (–113 кДж/моль), т. е. весьма существенную величину по сравнению с эмпирической энергией резонанса Ерез = –36÷–38 ккал/моль
(–150,7÷–159,0 кДж/моль) [3], т. е. Едел = –9÷–11 ккал/моль (–37,7÷–46,0 кДж/моль):
Нами проанализировано влияние пиррольных колец сконденсированных с центральным бензольным ядром на ароматичность молекулярной системы. Выявлены структуры, позволяющие оценить разность между энергией резонанса и энергией делокализации. При последовательном увеличении числа пиррольных колец, сконденсированных с молекулой бензола по положению 3, 4 в пирроле, от изоиндола 1 к дипирроло[3,4-e]изоиндолу 2 и
трис(3,4-пирролдиил)у 3, наблюдается выравнивание длин связей в бензольном кольце (рисунок 1) при уменьшении ароматичности бензольного остова (таблица 1) вплоть до ее потери для структуры 3.
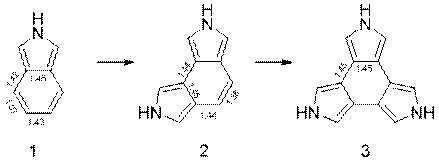
Рисунок 1 – Значения длин связей в молекулах 1, 2, 3
Однако, если рассматривать увеличение числа пиррольных колец, сконденсированных с молекулой бензола по положению 2, 3 в пирроле, ситуация меняется – ароматичность не теряется, а остается практически прежней. В ряду от индола 4 к дипирроло[2,3-e]индолу 5 и трис(2,3-пирролдиил)у 6, как и в первом случае, наблюдается выравнивание длин связей в бензольном кольце (рисунок 2), но с сохранением ароматичности центрального фрагмента на прежнем уровне (таблица 1).
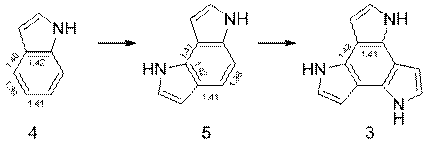
Рисунок 2 –Значения длин связей в молекулах 4, 5, 6
Таблица 1 – Рассчитанные значения критерия NICS (1) для центрального бензольного фрагмента молекул 1 – 6 (B3LYP/6-31G(d, p))
Молекулы | Величина NICS (1) | Молекулы | Величина NICS (1) |
1 | -9,54 | 4 | -11,90 |
2 | -5,69 | 5 | -11,50 |
3 | -2,5 | 6 | -10,40 |
Для бензола NICS (1) = –11,3. Таким образом, ароматичность шестичленного цикла 6 соответствует бензолу, а молекулы 3 – неароматическому шестичленному кольцу с выровненными связями.
Можно предположить, что разности полных энергий изомеров 6 и 3 соответствует энергия делокализации (разница между энергиями резонанса и сжатия связей): Eдел = ΔЕ = Еполн (6) – Еполн (3) = –8 – (–4) = –12,4 ккал/моль (–51,9 кДж/моль). Поскольку, встречающаяся в литературе,
Едел = –9÷–11 ккал/моль (–37,7÷–46,0 кДж/моль), то можно говорить о соответствии полученного нами результата и известного из литературных источников.
Таким образом, нами предложен новый подход к оценке величины энергии делокализации бензола по разностям полных энергий изомеров соединений бензола, сконденсированного с пиррольными кольцами.
Список литературы:
1 Zhongfang Chen, Nucleus-Independent Chemical Shifts (NICS) as an Aromaticity Criterion Chem. Rev. 2005, 105,
2 Кузнецов концепции ароматичности: полиэдрические структуры. Институт общей и неорганической химии им. . Наука 2009.
3 Химия гетероциклических соединений: Пер. с англ. – М.: Мир, 1996 г.
УДК 66
,
НОВЫЕ ХИММОТОЛОГИЧЕСКИЕ ПОКАЗАТЕЛИ АЛЬТЕРНАТИВНЫХ МОТОРНЫХ ТОПЛИВ
Уфимский государственный нефтяной технический университет, г. Уфа
E-mail: *****@***ru
Для более полной оценки эксплуатационных качеств моторных топлив нами предлагается принципиально новые химмотологические показатели - топливная энергоемкость (Эт, МДж/кгвоз.) и относительный расход топлива (Gотн.). Эт - отношение низшей теплоты сгорания топлива (Qн, МДж/кг) к стехиометрическому (α=1) расходу воздуха (lвоз, кгвоз/кг топл.). Значения Qн и lвоз рассчитываются по данным элементного состава топлива. Поскольку мощности поршневых ДВС принято оценивать по суммарному литражу цилиндров, т. е. по объему расходуемого воздуха, то показатель Эт косвенно характеризует мощностную возможность моторного топлива применительно к двигателям с одинаковыми степенями сжатия [1].
Относительный расход топлива удобнее определить как отношение низшей теплоты сгорания и условного топлива (эквивалента) н.-гептана с Qн=45 МДж/кг i-го топлива. У прямогонных бензинов в зависимости от их фракционного состава Qн составляет около 45 МДж/кг.
Ниже приведена таблица с результатами расчетов Эт и Gотн. некоторых индивидуальных углеводородов и оксигенатов.
Результаты расчета показывают, что у алканов, цикланов и аренов по мере увеличения молярной массы энергоемкость практически остается одинаковой, а относительный расход топлива увеличивается. Низшая теплота сгорания увеличивается по мере снижения мольной доли водорода, но по мере уменьшения мольной доли кислорода у оксигенатов низшая теплота сгорания растет. У оксигенатов по мере увеличения молярной массы энергоемкость остается также одинаковой, а относительный расход топлива уменьшается. Отсюда следует, что применяя биоспирты и биоэфира в качестве топлива или добавки к ним, значительно уменьшается расход топлива.
Таблица - Результаты расчетов химмотологических показателей углеводородов и оксигенатов
Углеводород, оксигенат | М | mc | mН | mo | Qн, МДж /кг | lвоз., кгвоз/кг топл | Эт, МДж/кгвоз. | Gотн. |
Гептан, С7Н16 | 100,2 | 0,8391 | 0,1610 | - | 45,02 | 3,53 | 12,772 | 0,990 |
Октан, С8Н18 | 114,22 | 0,8413 | 0,1589 | - | 44,88 | 3,51 | 12,771 | 1,003 |
Нонан, С9Н20 | 128,26 | 0,8428 | 0,1572 | - | 44,76 | 3,50 | 12,771 | 1,003 |
Декан, С10Н22 | 142,29 | 0,8441 | 0,1559 | - | 44,67 | 3,50 | 12,770 | 1,007 |
Циклогексан, С6Н12 | 84,16 | 0,8563 | 0,1437 | - | 43,83 | 3,43 | 12,767 | 1,027 |
Циклогептан, С7Н14 | 98,19 | 0,8363 | 0,1437 | - | 43,83 | 3,43 | 12,767 | 1,027 |
Бензол, С6Н6 | 78,12 | 0,9225 | 0,0774 | - | 39,25 | 3,08 | 12,745 | 1,126 |
Этилбензол, С8Н10 | 106,17 | 0,9050 | 0,0949 | - | 39,95 | 3,17 | 12,749 | 1,112 |
Пропилбензол, С9Н12 | 120,19 | 0,8994 | 0,1006 | - | 40,46 | 3,20 | 12,773 | 1,101 |
Метанол СН3ОН | 32,04 | 0,9749 | 0,1258 | 0,4994 | 20,22 | 1,50 | 13,421 | 2,224 |
Этанол С2Н5ОН | 46,07 | 0,5214 | 0,1313 | 0,3473 | 27,41 | 2,09 | 13,094 | 1,641 |
Бутанол С4Н9ОН | 74,12 | 0,6482 | 0,1342 | 0,2159 | 33,62 | 2,60 | 12,903 | 1,338 |
Диметиловый эфир | 46,07 | 0,5214 | 0,1360 | 0,3473 | 27,41 | 2,09 | 13,094 | 1,641 |
Диэтиловый эфир | 74,12 | 0,6482 | 0,1360 | 0,2159 | 33,62 | 2,60 | 12,930 | 1,338 |
Дибутиловый эфир | 130,23 | 0,7378 | 0,1393 | 0,1229 | 38,02 | 2,95 | 12,849 | 1,183 |
МТБЭ | 88,15 | 0,6813 | 0,1372 | 0,1815 | 35,25 | 2,73 | 12,898 | 1,276 |
ЭТБЭ | 102 | 0,7065 | 0,1384 | 0,1569 | 36,49 | 2,83 | 12,876 | 1,233 |
Список литературы:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 |




