Взаимодействие окисленного АБИНОГАЛАКТАНА С ПРОИЗВОДНЫМИ УРАЦИЛа В ВОДНОЙ СРЕДЕ
ФГБОУ ВПО «Башкирский государственный университет», г. Уфа
E-mail: *****@***ru
В последнее время большое внимание уделяется созданию лекарственных препаратов пролонгированного действия для лечения и профилактики различных заболеваний. Подобные препараты позволят увеличить время действия лекарства в организме человека и одновременно снизить его суточную дозу. Одним из способов достижения такого результата является иммобилизация лекарственного вещества на полимерной матрице. В качестве такой матрицы было предложено использовать модифицированный природный полимер арабиногалактан Сибирской лиственницы, полученный озонированным окислением в водной среде. Окисленный полисахарид обладает меньшей молекулярной массой и большей комплексообразующей способностью по сравнению с исходным полимером, что позволяет использовать его в качестве носителя биологически активных веществ, например, производных урацила.
Комплексообразование окисленного арабиногалактана с урацилами изучали в водной среде, как при комнатной температуре, так и при нагревании. Показано, что в условиях эксперимента урацил и его производные (5-фторурацил, 6-метилурацил, 5-амино-6-метилурацил, 5-бром-6-метилурацил, 5-гидрокси-6-метилурацил, 5-нитро-6-метилурацил) находятся в дикето-форме.
Согласно литературным данным в УФ-спектре урацилов имеются две полосы поглощения в областях 200-220 и 255-275 нм. Методом ультрафиолетовой спектроскопии было установлено, что добавление окисленного арабиногалактана к водным растворам урацилов приводит к гипсохромным сдвигам максимумов поглощения и увеличению интенсивностей пиков полос поглощения, которые свидетельствую об образовании комплексов.
Состав полученных комплексных соединений определяли методами изомолярных серий и молярных отношений. Во всех случаях их состав оказывался равным 1:1, т. е. на одну карбоксильную группу арабиногалактана приходится одна молекула урацила или его производного. Константы устойчивости комплексов, образованных урацилами и арабиногалактаном, меняются в пределах (1÷5)·104 л/моль. Установлено, что электронодонорные заместители в пятом положении молекулы 6-метилурацила способствуют увеличению устойчивости образующихся комплексных соединений.
Работа выполнена при поддержке проекта № 3.1151.2011, исполняемого в рамках государственного задания Министерства образования и науки РФ, и ГНТП РБ «Химические технологии и новые материалы для инновационного развития экономики Республики Башкортостан».
УДК 504.5
, ,
БИОСОРБЕНТ ДЛЯ ОЧИСТКИ НЕФТЕЗАГРЯЗНЕННЫХ СРЕД
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Уфимский государственный нефтяной технический университет, г. Уфа
В настоящее время с развитием нефтяной промышленности, в частности добычи, транспортировки и переработки нефти и нефтепродуктов, проблема загрязнения окружающей среды нефтяными углеводородами остается актуальной. Особенно остро данная проблема стоит в вопросах аварийного загрязнения водных объектов, в частности прибрежных зон морских акваторий, территорий рек и озер. Нефть и нефтепродукты, попадая на водную поверхность, быстро распространяются на значительные территории, образуя тончайшую пленку. Образующаяся нефтяная пленка препятствует естественному газообмену, оказывая негативное воздействие на местные биоценозы, приводя к необратимым изменениям в водной среде [1]. Мировой опыт решения данной проблемы показывает, что наиболее эффективным является применение сорбционных технологий, позволяющих быстро локализовать нефтяное загрязнение [2]. При выборе сорбента большое внимание уделяется его сорбционным характеристикам, а также стоимости его изготовления и доступности сырьевой базы. В связи с этим достаточно перспективным, является изучение возможности получения сорбционных материалов на основе отходов производства.
Целью работы являлось исследование нового сорбента на основе гидрофобизированных отходов деревообрабатывающего производства с иммобилизованной на его поверхности культурой нефтеокисляющих микроорганизмов.
В качестве древесных отходов использовали опилки лиственных пород деревьев с крупностью фракций 2-7 мм. Гидрофобизацию опилок осуществляли жидкими парафинами, путем их распыления на поверхности сорбента.
Предварительно перед гидрофобизацией, с целью создания запаса биогенных питательных веществ, опилки насыщали биостимулятором.
Иммобилизацию микроорганизмов осуществляли путем смешивания концентрированной биомассы микроорганизмов с носителем в соотношении 1:1. В качестве микроорганизмов - деструкторов нефти и нефтепродуктов исследовали ассоциацию аборигенных нефтеокисляющих микроорганизмов (АОМ). Биоактивированный сорбент высушивали в потоке воздуха, при температуре не более 35 °С.
Суспензию аборигенных нефтеокисляющих микроорганизмов получали путем отбора проб нефтезагрязненных сред, с последующей активацией присутствующих в них микроорганизмов в полной минеральной среде. В качестве единственного источника углерода и энергии использовали нефть, из расчета 1 % масс.[3] Наработку биомассы осуществляли в ферментере при температуре 30 °С до титра клеток 109 кл/мл.
Сорбционные характеристики получаемых сорбентов определяли в соответствии с ТУ 8-03-95. Численность гетеротрофных нефтеокисляющих микроорганизмов определяли путем высева на плотные среды по методу Коха [4].
Для оценки эффективности очистки нефтезагрязненных сред иммобилизованной нефтеокисляющей микрофлорой готовили емкости с водой с различной толщиной нефтяной пленки. Обработку нефтезагрязненной поверхности производили исследуемым биосорбентом до полного впитывания нефтепродуктов. Биодеструкцию отработанного сорбента после извлечения из воды осуществляли в лабораторных условиях при комнатной температуре. Убыль нефтепродуктов определяли по остаточному содержанию нефти и нефтепродуктов в пробах методом ИК - спектрометрии по известной методике [5]. Определение концентрации нефти и нефтепродуктов в пробах производили через 90 дней. Культивирование проводили при комнатной температуре.
Таким образом, иммобилизация нефтеокисляющей микрофлоры на поверхности сорбента позволяет значительно ускорить процесс биодеградации нефтяных углеводородов. Предлагаемый биосорбент при относительно невысокой себестоимости изготовления обеспечивает высокоэффективную очистку водных поверхностей от нефтяных загрязнений и может быть рекомендован к широкому внедрению.
Список литературы:
1 Ягафарова Л. А., , Барахнина экология в нефтегазовом комплексе. Учебное пособие, Уфа: Изд-во УГНТУ, 20с.
2 , , Ягафаров методы переработки нефтешламов. – М.: Химия, 2010. – 190 с.
3 Патент РФ № 000. Способ выделения и активации консорциума аборигенных микроорганизмов-деструкторов нефти и нефтепродуктов. , , и др. Опуб. 20.04.2009 Бюл. № 11
4 Егоров к практическим занятиям по микробиологии. - М.: МГУ, 1995. – 224 с.
5 ПНДФ 14.1:2.5-95 «Методика выполнения измерений массовой концентрации нефтепродуктов в природных и сточных водах методом ИК-спетрометрии».
УДК 612.015.161
,
НЕКОТОРЫЕ ФАКТОРЫ, ВЛИЯЮЩИЕ НА ПРОЦЕСС СПИРТОВОГО БРОЖЕНИЯ ПРИ ПОЛУЧЕНИИ БИОЭТАНОЛА ИЗ ГИДРОЛИЗАТОВ ЦЕЛЛЮЛОЗОСОДЕРЖАЩЕГО СЫРЬЯ
Бийский технологический институт (филиал) ФГБОУ ВПО
«Алтайский государственный технический университет
им. », г. Бийск
Федеральное государственное бюджетное учреждение науки
Институт проблем химико-энергетических технологий
Сибирского отделения Российской академии наук, г. Бийск
E-mail: *****@***ru
Спиртовое брожение – сложный биохимический процесс, который происходит при каталитическом действии ферментов дрожжевых клеток на глюкозу, фруктозу и другие шестиуглеродистые сахара [1]. На выход и качество этилового спирта влияет много факторов: интенсивность аэрирования сбраживаемого гидролизата, концентрация в нем сахара, активная кислотность, температура брожения, раса применяемых дрожжей и др. [3].
В данной работе для сбраживания гидролизатов использовался штамм Saccharomyces сerevisiae Y-1693 коллекции ВКПМ. Штамм был выделен из ферментера Котласского целлюлозно-бумажного комбината и использовался для производства этанола на гидролизатах древесины. Сахаромицеты являются устойчивыми к вредным примесям гидролизатов и обладают высокой бродильной активностью.
С повышением интенсивности аэрирования содержание спирта в гидролизатах снижается, что связано с увеличением расхода сахара на синтез биомассы дрожжей и образование других продуктов брожения, поэтому получение маточных дрожжей в лабораторных условиях мы проводим при небольшой аэрации, а процесс спиртового брожения – в анаэробных условиях.
Активная кислотность среды является одним из основных факторов, влияющих на жизнедеятельность дрожжей в спиртовом производстве. Для создания благоприятных условий жизнедеятельности микроорганизмов необходимо поддерживать значение рН питательной среды на оптимальном уровне, так как активная кислотность в значительной степени влияет на деятельность ферментов дрожжей и на состояние их клеток. При сбраживании гидролизатов активная кислотность поддерживалась в пределах 4,5-5,0 активных единиц рН. Снижение активной кислотности ведёт к замедлению процесса брожения, а повышение – к контаминации среды посторонней микрофлорой.
Метаболическая активность и репродуктивная способность микроорганизмов находятся в функциональной зависимости от температуры, причем при брожении выделяется тепло, вызывающее повышение температуры бродящего сусла. С повышением температуры брожения увеличивается скорость этерификации и быстрее идет синтез биомассы и дрожжевых клеток за счет органических кислот, содержание которых уменьшается [3]. В нашем случае брожение проводилось в анаэробных условиях и температуре 28 ºС.
Известно, что гидролизные среды не являются полноценными для спиртового брожения в силу наличия вредных примесей и недостаточного содержания питательных веществ и витаминов. В качестве биологически активной добавки к среде в работах использован дрожжевой экстракт. Установлено, что в целях экономии дрожжевого экстракта нецелесообразно вносить его в количестве более 3 % [4].
Кроме штамма Saccharomyces сerevisiae Y-1693 для сбраживания гидролизатов в работе использовали штамм Pachysolen tannophilus ВКПМ
Y-1532, способный превращать ксилозу в этанол. Установлено, что скорость сбраживания РВ продуцентом P. tannophilus ВКПМ Y-1532 в 2,3 раза ниже, чем S. Сerevisiae ВКПМ Y-1693. Одновременное внесение культур ускоряет сбраживание редуцирующих веществ и позволяет снизить количество несброженных РВ в гидролизате [5].
Таким образом, спиртовое брожение – это сложный непрерывный процесс распада сахара, катализируемый разными ферментами, при котором необходимо учитывать ряд факторов, влияющих на выход спирта.
Список литературы:
1 Шарков, гидролизных производств / , , М.: Лесная промышленность, 1973. – 408 с.
2 Яровенко, спирта / , , [и др.]. – Под ред. проф. – М.: Колос, 1999. – 464 с.
3 , Скиба биологически активных веществ на биосинтез этанола на среде ферментативного гидролизата технической целлюлозы плодовых оболочек овса_/ Химия биологически активных веществ: тезисы Всерос. школы-конф. молодых учёных, аспирантов и студентов с международным участием «ХимБиоАктив-2012», (24-28 сентября 2012 г., г. Саратов) – (В печати).
4 , Байбакова биоэтанола штаммами Pachysolen tannophilus Y-1532 и Saccharomyces сerevisiae Y-1693 на гидролизной среде / Технологии и оборудование химической, биотехнологической и пищевой промышленности: материалы 5-й Всероссийской научно-практической конференции студентов, аспирантов и молодых ученых с международным участием (24-26 мая 2012 г., г. Бийск). – В 2 ч. Часть I. – Бийск: Изд-во Алт. гос. техн. ун-та, 2012. – С. 284-287.
УДК 665.7 + 547.281.1 + 546.221.1
1, 2, 1,2
РЕАКЦИЯ ЦИКЛОПЕНТАДИЕНА С ФОРМАЛЬДЕГИДОМ
И СЕРОВОДОРОДОМ
1Башкирский государственный университет, г. Уфа
2Институт нефтехимии и катализа РАН, г. Уфа
E-mail: *****@***ru, *****@***ru
Интерес к получению на основе циклопентадиена различных спиртов и их производных, вызван тем обстоятельством, что последние могут быть мономерами в различных полимерных синтезах, служить модификаторами в композиционных материалах [1]. Между тем, известно [2], что взаимодействие циклопентена и параформа в присутствии соляной кислоты приводит к изомерам 1,3-диоксана 1a, b в соотношении 2 : 1.
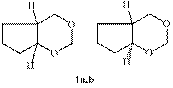
В настоящей работе изучено каталитическое взаимодействие циклопентадиена с формальдегидом и сероводородом. Установлено, что реакция циклопентадиена с тиометилирующим реагентом «СН2О-H2S» в присутствии каталитического количества H2SO4 (0,5 ммоль), проходит с разложением целевого продукта 2 до 4.5-бис(гидроксиметил)циклопентан-1.3-диола 3 (76%). А взаимодействие с тиометилирующим реагентом в присутствии 0,5 ммоль BuОNa в н-бутаноле приводит к смеси продуктов – тетраола 3 с выходом 61% и тетрацикло[13.2.1.47.17.49.16.022.26]3,5,11,13-тетраокса-19,21,23,25-тетратиагексакозана 4 (35%). Строение синтезированных соединений установлено на основании спектральных данных и элементного анализа.
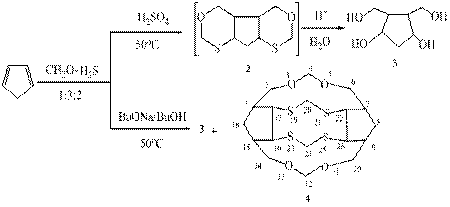
Таким образом, каталитическое взаимодействие циклопентадиена с формальдегидом и сероводородом в присутствии BuОNa приводит к продукту межмолекулярной гетероциклизации 4.
Список литературы:
1 . Фульвены и фульвенилметанолы на основе нефтехимического циклопентадиена и формальдегида //Автореферат на соискание ученой степени к. х.н., Кубанский ун-т. 2001, С. 24.
, , и др. Реакция Принса с циклопентеном и синтез оксиметилциклопентена-2 // Изв. АН СССР. Сер. хим. 1973, С. 1080–1085.
УДК 612.015.161
,
ИЗУЧЕНИЕ БИОХИМИЧЕСКИХ СВОЙСТВ SACCHAROMYCES СEREVISIAE ВКПМ Y-1693 ПРИ ДЛИТЕЛЬНОМ КУЛЬТИВИРОВАНИИ
Бийский технологический институт (филиал) ФГБОУ ВПО
«Алтайский государственный технический университет
им. », г. Бийск
Федеральное государственное бюджетное учреждение науки
Институт проблем химико-энергетических технологий
Сибирского отделения Российской академии наук, г. Бийск
E-mail: *****@***ru
Целью данной работы было изучение биохимических особенностей дрожжей Saccharomyces сerevisiae при длительном культивировании. Штамм Saccharomyces сerevisiae ВКПМ Y-1693 был выделен из ферментера Котласского целлюлозно-бумажного комбината.
Штамм культивировали в течение одного года на двух средах: стерильном солодовом сусле и стерильной дистиллированной воде при температуре 28 ºС. Культивирование проводили в химических пробирках с ватно-марлевыми пробками. С целью исключения возможности инфицирования анализа каждый раз отбиралась одна пробирка. Через год культивирования жидкость в пробирках полностью испарилась, дрожжи были распределены по стенкам.
Содержимое пробирки переносилось в стерильное солодовое сусло с соблюдением правил асептики. После этого проводилось спиртовое брожение в анаэробных условиях при 28 ºС в течение двух суток. Редуцирующие вещества (РВ) в средах определялись спектрофотометрическим методом в пересчете на глюкозу. Крепость бражек (объемная доля спирта) определялась ареометром для спирта в дистилляте, полученном после предварительной перегонки спирта из бражки, согласно ГОСТ Р 03. По крепости полученных бражек и концентрации РВ в исходном сусле был рассчитан выход этанола.
При сбраживании сусла дрожжами, культивированными в течение года на среде солодового сусла, получен выход этанола 93 % от теоретического, а при сбраживании сусла дрожжами, культивированными в течение года на дистиллированной воде, выход этанола составил 96 %. Сравнивая эти данные, можно сделать вывод, что продукты обмена оказывают негативное воздействие на клетки дрожжей и их присутствие в среде более критично, чем отсутствие в среде питательных веществ. В то же время, дрожжи очень жизнеспособны и устойчивы к продуктам своего обмена, их биохимическая активность сохраняется высокой в течение года культивирования в истощенных средах. Эти характеристики предопределяют успешность применения штамма Saccharomyces сerevisiae ВКПМ Y-1693 для сбраживания гидролизатов растительного сырья.
Штамм используется в ИПХЭТ СО РАН для синтеза биоэтанола на средах ферментативных гидролизатов нетрадиционного недревесного растительного сырья.
УДК 634.0.813
ЛЕКТИНЫ RICINUS COMMUNIS КАК ИНСТРУМЕНТ ДЛЯ БОРЬБЫ С ГРИБКОВЫМИ ИНФЕКЦИЯМИ РАСТЕНИЙ
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Уфимский государственный нефтяной технический университет, г. Уфа
E-mail:baichicli@mail.ru
Лектины – углеводсвязывающие белки-агглютинины, способные обратимо и специфически связывать углеводные остатки различной химической природы [2]. В литературе встречается много информации о рицине – лектине семян клещевины обыкновенной. Однако сведений о лектинах из других органов растения клещевины практически нет, их биохимические свойства до настоящего времени не изучались. Знания биохимических свойств и углеводной специфичности данных лектинов может быть использовано для агглютинации клеток паразитических микроскопических грибов, содержащих в своих клеточных стенках известные углеводные детерминанты.
Лектины экстрагировали ацетатным буфером рН 3,8 из стеблей, листьев, семян, корней, далее определяли концентрацию белка по методу Лоури. Гемагглютинирующую активность лектинов определяли реакцией гемагглютинации с самопроизвольным оседанием эритроцитов I группы крови. Углеводную специфичность определяли методом подавления активности лектина углеводами, выступающими в роли гаптенов. Брали набор гаптенов – моно-, ди-, полисахаридов, в частности хитин из клеточных стенок грибов. Для определения состава и функциональности лектины из различных частей растения клещевины инкубировали с растворами трипсина для разрушения белкового компонента лектина и с KIO4 для разрушения углеводной части [1; 3]. Исчезновение активности рассматривали как доказательство наличия и функциональной активности соответствующей части. Для определения стабильности применяли кипячение раствора лектина, последовательное замораживание и оттаивание при комнатной температуре [4]. При определении количества белка по методу Лоури было выявлено, что в зависимости от исследуемого органа растения клещевины наблюдается различное содержание белка, в том числе лектинов (табл. 1).
Таблица 1 - Содержание лектинов в различных частях Ricinus communis
Часть растения | Показ. ФЭК | V, мл | Показ. графика | Количество белка, мг/мл |
Стебель | 0,17 | 3,5 | 1,17 | 8,2±0,3 |
Семена | 0,57 | 4,5 | 2,87 | 22,9±0,6 |
Листья | 0,45 | 5,5 | 2,315 | 50,9±0,7 |
Корни | 0,85 | 5 | 3,15 | 63±0,7 |
Наибольшее количество белка обнаружено в корнях, что, возможно, можно объяснить тем, что этот орган часто подвергается инфицированию со стороны фитопатогенов, и лектины выполняют в данном органе защитную функцию. Небольшое содержание лектинов выявлено в семенах, это может быть связано с фазой развития растения и сезоном года.
Гемагглютинирующая активность лектинов Ricinus communis к поверхностным углеводам эритроцитов I группы крови оказалась высокой и отличалась по титру: у корней и семян (1:6), стеблей и листьев (1: 3) (рис. 1).

Рисунок 1 - Гемагглютинирующая активность лектинов Ricinus communis:
А–стебли, В–листья, С–корни, D–семена
Высокая гемагглютинирующая активность лектинов корней также может быть причиной того, что данные гликопротеины выполняют защитную функцию в корнях.
Для определения углеводной специфичности использовались лектины корней и листьев. Лектины корней клещевины обыкновенной специфичны к N-ацетилглюкозамину, маннозе, галактозе, а также к хитину. У лектинов листьев выявлена специфичность лишь к маннозе и галактозе. Для определения состава и функциональности брали лектины корней. Инкубация препарата лектина с трипсином приводила к исчезновению его гемагглютинирующей активности, что указывает на наличие в его составе белковой части и ее функциональной необходимости. Кроме того, это свидетельствует о наличии на поверхности молекулы агглютинина лизин-аргининовых детерминант. Агглютинирующая активность пропадала при воздействии на лектин перйодатом калия, окисляющего сахара, но слабо влияющего на белковый компонент, это свидетельствует о наличии и функциональной значимости в составе лектина углеводной части. Полученные данные позволяют заключить, что лектин корней клещевины имеет гликопротеиновую природу, причём как его белковый, так и углеводный компоненты необходимы для проявления гемагглютинирующей активности, что характерно для большинства лектинов.
Высокотемпературная обработка лектина приводила к исчезновению его агглютинирующей активности. Это вызывается диссоциацией лектиновой субъединицы, либо всей молекулы гликопротеина или изменением пространственно-конформационной структуры. Серия последовательных замораживаний и оттаиваний препарата лектина не приводила к исчезновению его агглютинирующей активности.
Список литературы:
1 Баймиев углеводсвязывающих участков лектинов бобовых растений как детерминант специфичности взаимодействия с клубеньковыми бактериями // Автореферат докт. дисс. – Уфа, 2007. – 46с.
2 , , Луцик .–Львов: Вища школа. Изд-во при Львов. ун-те, 1981.–156с.
3 , Хавкин растений: предполагаемые функции // Физиология растений, 1983.–Т.30. Вып.5.–С. 852-865.
4 Ямалеева растений и их биологическая роль.–Уфа: Изд-е Башкирск. ун-та, 2001.–204с.
УДК 547.598
(мл.)1, 1,
СИНТЕЗ НОВЫХ ДИПЕПТИДНЫХ ПРОИЗВОДНЫХ ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ
Федеральное государственное бюджетное учреждение науки Институт органической химии Уфимского научного центра РАН, г. Уфа
E-mail: *****@***ru
Глицирризиновая кислота (ГК) (1) – основной тритерпеновый гликозид корней солодки голой (Glycyrrhiza glabra L.) и уральской (Glycyrrhiza uralensis Fisher) относится к числу лидирующих растительных гликозидов, представляющих большую ценность для медицины в качестве скаффолда (матрицы) для создания новых высокоэффективных иммуностимуляторов и противовирусных агентов [1].
В продолжение наших работ по созданию библиотеки новых производных ГК для изучения зависимости структура-противовирусная активность нами осуществлен синтез новых коньюгатов ГК с дипептидами, являющимися участками расщепления протеинов gag и gag-pol, с использованием реагента Вудворда К (RWK).
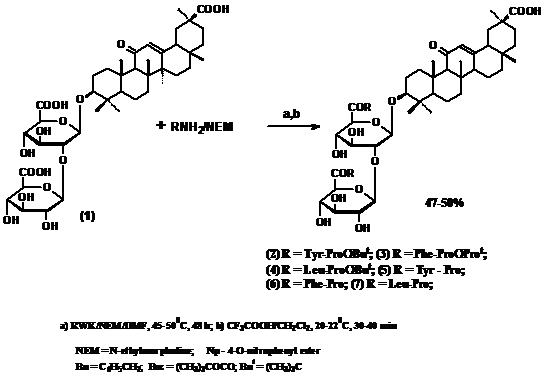
Работа поддержана РФФИ (грант ).
Список литературы:
1 , , Толстикова : биоразнообразие, химия, применение в медицине. Новосибирск: Академическое изд-во «Гео», 20с.
УДК 537.363 + 541.183.5 : 661.185.4
Очистка Сырдарьинской воды от патогенных бактерии
ПРИРОДНыми СОРБЕНТАМи
Кызылординский государственный университет им. Коркыт-Ата, Казахстан
E-mail: bal_gulzhan@mail.ru
На экологическую обстановку в области большое влияние оказывает химический состав воды Сырдарьи. Вода по степени загрязненности относится к третьему классу, т. е. умеренно –загрязненной. По данным санитарной службы области, в г. Кызылорде питьевой воды не соответствовало требованиям ГОСТа. Потребление жителями г. Кызылорды недоброкачественной воды с высокой степенью минерализации и жесткости привело к резкому возрастанию уровня инфекционных и почечно-легочных заболеваний [1].
Эффект обеззараживания воды зависит от сочетания многих факторов, среди которых наибольшее значение имеют биологические особенности микроорганизмов, бактерицидное действие реагентов, состояние водной среды условия, в которых происходит процесс обеззараживания [2-3].
Применение в качестве коагулянта – сорбента монтмориллонита повышает эффективность удаления микроорганизмов и вирусов в процессе контактного осветления воды, что предопределяет в дальнейшем введение более низких концентраций препаратов хлора для заключительного обеззараживания воды [4].
В этой связи очистка Сырдарьинской воды от патогенных бактерии является важной и сложной задачей, требующей комплексного подхода к решению. Сочетание различных способов очистки и анализа вод, основанных на успехах современной химической науки, позволяет раскрыть новые перспективные возможности в этой области.
В последнее время приоритетным направлением является использование для обеззараживания от патогенных бактерии природных сорбентов, что обусловлено их достаточно высокой сорбционной ёмкостью, селективностью, катионо-обмен-ными свойствами и возможностью практически полного удаления ионов. Немаловажным фактором является также их сравнительно низкая стоимость и доступность [5].
Целью настоящего исследования является изучение возможности исполь-зования различных форм бентонитовой глины для очистки Сырдарьинской воды от патогенных бактерии в статических условиях. Объектом исследования является Сырдарьинская вода в г. Кызылорда.
Кислотную активацию бентонитовой глины проводили по методике предложенной и др. [3]. Известно, что важной особенностью природных сорбентов – возможность их модификации и активации с помощью различных методов (термическая, кислотная, солевая и др.).
При воздействии термоактивированного бентонита на Е. соli, дизентерийная палочка в течение 5, 30, 60 мин, 3 и 24 часа не оказывает антимикробного эффекта. Для стафилокока в течение 5, 30, 60 мин, 3 и 24 часа термо-активированного бентонита отмечен значительный антимикробный эффект.
Кислотоактивированный бентонит эффективно угнетает испытуемые тест-микробы, для стафилокока этот бентонит не оказывает антимикробного эффекта. Наилучший способ активации бентонитовых глин является кислотная активация при повышенной температуре. При кислотной активации бентонита заметно уменьшается содержание в образцах оксидов магния, железа, щелочных и щелочноземельных металлов. При кислотной обработке уменьшается величина катионообменной емкости, что является результатом частичного разрушения кристаллической решетки минерала, изменяется состав обменного комплекса.
При кислотной активации высвобождается некоторое количество силика-геля, который приводит к увеличению поверхности активированных образцов в 2-4 раза по сравнению с поверхностью немодифицированных образцов, например, для естественного бентонита удельная поверхность составила 90 м2/г, а при кислотной активации стала 200 м2/г. Следует отметить также, что кислотоактивированный бентонит в водном растворе приобретает кислую среду (рН = 3,2), что создает благоприятное условие для прекращения существования микроорганизмов.
Анализ полученных экспериментальных результатов позволяет сделать вывод о том, что бентонит 14-горизонта Таганского месторождения после 6 часо-вой активации 20 % - ной серной кислотой, предварительно прошедший термо-обработку при 120 оС в течение 6 часов является наилучшим сорбентом для обеззараживание патогенных бактерии (Е. соli, дизент. пал) из Сырдарьинской воды. Оптимальный режим очистки: рН среды 6,0-6,5, время контакта 24 час, расход адсорбента 0,2 г/дм3 .
Список литературы:
1 , Алиева и биотехнология очистки и промышленных сточных вод. – Алма –Ата: Ѓылым,1990 – 280с.
2 Заявка2375/05 Великобритания, МПК7С02F1/50. Способ обеззараживания воды / Bredner Graham Colin. - Опубл. 06.11.2002; Бюл. №11.
3 Пат.2150320РФ, МПК7В01J20/20,С01В31/08.Способ получения бактериостати-ческого сорбента для очистки питьевой воды/ , , - Опубл.10.06.2000; Бюл. №10.
4 , Гембицкий как средство борьбы с инфекций, биокоррозией и биообрастанием // Сб. ст. Всерос. конф.-1998.- №11-С.92-95.
5 , , Тусупбаев приготовления средства для обеззараживания воды. № 000 Предпатент РК Астана, 2006 г
УДК 634.0.813.2
, ,
ОЗОН-КИСЛОРОДНОЕ ОКИСЛЕНИЕ ПРИРОДНОГО БИОПОЛИМЕРА АРАБИНОГАЛАКТАНА В ВОДНОЙ СРЕДЕ
ФГБОУ ВПО «Башкирский государственный университет», г. Уфа
E-mail: *****@***ru
Настоящая работа посвящена изучению химической модификации природного полисахарида арабиногалактана Сибирской лиственницы путем его окисления озон-кислородной смесью в водной среде. Данный метод позволяет уменьшить молекулярную массу биополимера и одновременно с этим увеличить число реакционно-способных функциональных групп в макромолекуле. Такой окисленный арабиногалактан может использоваться в косметической и медицинской промышленностях для улучшения свойств уже существующих лекарственных препаратов.
В работе использовали арабиногалактан, выделенный из древесины лиственницы Сибирской, фирмы «Химия древесины» (г. Иркутск). Окисление полисахарида проводили в водной среде при температуре 90°С и скорости барботажа озон-кислородной смеси 6 л/час.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 |




