МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
МИНИСТЕРСТВО ОБРАЗОВАНИЯ РЕСПУБЛИКИ БАШКОРТОСТАН
АКАДЕМИЯ НАУК РЕСПУБЛИКИ БАШКОРТОСТАН
ОТДЕЛЕНИЕ ХИМИКО-ТЕХНОЛОГИЧЕСКИХ НАУК
институт органической химии УНЦ РАН
Институт нефтехимии и КАтализа РАН
БАШКИРСКОЕ РЕСПУБЛИКАНСКОЕ ОТДЕЛЕНИЕ
РХО ИМ. Д. И. МЕНДЕЛЕЕВА
башкирский государственный университет
Уфимский Государственный нефтяной
технический университет
ИННОВАЦИОННЫЕ ТЕХНОЛОГИИ
в области химии и биотехнологии
Материалы Всероссийской научно-технической
конференции
г. Уфа, 22-23 ноября 2012 г.
Уфа
Изд-во УГНТУ
2012
УДК 378.147:54+547+577.1+60
ББК 28.072+24.2+74.58р+30.16
И73
Редакционная коллегия:
- д. т.н., проф., проректор по НИР УГНТУ
Ю. Р. Абрахимов – д. х.н., проф. (ИОХ УНЦ РАН)
А. Ф. Ахметов – д. т.н., проф. (УГНТУ)
Ф.З. Галин - д. х.н., проф. (БашГУ)
- член-корр. АН РБ, д. х.н., проф. (УГНТУ)
У. Б. Имашев - акад. АН РБ, д. х.н., проф. (УГНТУ)
М. Н. Рахимов – д. т.н., проф. (УГНТУ)
– д. х.н., проф. (БашГУ)
Р. И. Хуснутдинов – д. х.н., проф. (ИНК УНЦ РАН)
М. С. Юнусов - акад. РАН, д. х.н., проф. (ИОХ УНЦ РАН)
Г. Г. Ягафарова - д. т.н., проф. (УГНТУ)
Инновационные технологии в области химии и биотехнологии: Материалы Всероссийской научно-технической конференции / Уфа: Издательство Уфимского государственного нефтяного технического университета, 2с.
(Материалы помещены в сборник без редакторской правки)
Всероссийская научно-техническая конференция «Инновационные технологии в области химии и биотехнологии» проводится в рамках реализации «Программы развития и совершенствования инновационной инфраструктуры ФБГОУ ВПО УГНТУ» (Шифр программы 1.052) в целях популяризации современных достижений в области био - и органической химии, биотехнологии, нефтехимии, экологии, а также развития интеграции высшей школы, науки и производства.
В сборнике приведены материалы, отражающие результаты научно-исследовательских работ инновационных проектов, выполняемых в высших учебных заведениях, НИИ, институтах РАН, проектных организациях и предприятиях Российской Федерации
ISBN 1015-3 ©Уфимский государственный нефтяной технический университет, 2012
©Коллектив авторов, 2012
СЕКЦИЯ
«Био- и органическая химия, биотехнология»
УДК 547.517+547.78
, А. Пешич, ,
Структурные аналоги элеутеробина на основе производных 8-оксабицикло[3.2.1]октана
Московский Государственный Университет им. , г. Москва
E-mail: *****@***ru
Элеутеробин (Eleutherobin) – природный терпен, проявляющий на порядок более высокую противоопухолевую активность, чем имеющий аналогичное действие препарат таксол (паклитаксел). Основным фармакофором элеутеробина считают остаток N-метилурокановой [3-(1-метил-имидазол-4-ил)-проп-2-еновая] кислоты [1, 2].
Для поиска синтетически более доступных аналогов, в данной работе нами был проведен молекулярный докинг различных сложных эфиров
N-метилурокановой кислоты с каркасными диолами – производными
8-оксабицикло[3.2.1]октана в сайт связывания паклитаксела на белке тубулине (программный пакет SYBYL). В результате в качестве спейсеров были выбраны диастереомерно-чистые диолы 1 и 5, легко доступные из продукта реакции Дильса-Альдера фурана и тетрахлорциклопропена [3, 4].
Симметричный диол 1 был трансформирован в моноэфиры бензойных кислот 2 и 3 по реакциям с соответствующими хлорангидридами. Также была проведена модификация двойной связи. Для этого вначале был получен диацетат, который в результате син-гидроксилирования в системе N-оксид-N-метилморфолина (NMO) / OsO4 был превращен в диол 4. Было найдено, что гидроксилирование проходит стереоселективно, с образованием экзо-диола.
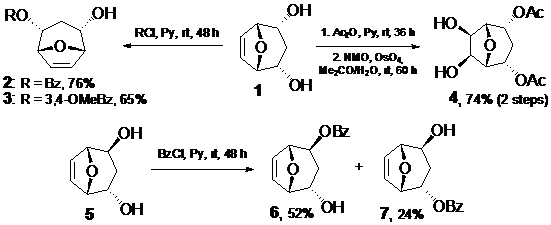
Разработанная нами методика получения моноэфиров была использована для синтеза бензоильных производных несимметричного диола 5 – моноэфиров 6 и 7. Было установлено, что преимущественно образуется производное 6, содержащее бензоильный заместитель в экзо-положении, что, очевидно, связано со стерическими факторами.
Следующим шагом нашей работы стало получение эфиров
N-метилурокановой кислоты и оксабициклических диолов. Для синтеза была использована известная методика на основе дициклогексилкарбодиимида (DCC) и диметиламинопиридина (DMAP) как сшивающих реагентов. Введение в реакцию спиртов 2, 3 и 6 позволило выделить эфиры 8, 9 и 10 с хорошими выходами.
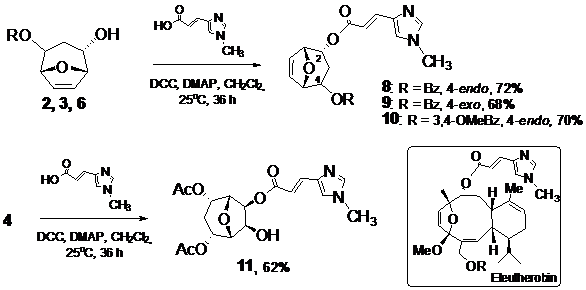
Также было исследовано получение сложного эфира диола 4 с
N-метилуроканой кислотой. Было показано, что реакция с одним эквивалентом кислоты приводит к моноэфиру 11, который был выделен с умеренным выходом. Таким образом, нами было синтезировано 4 новых производных
N-метилуроканой кислоты – структурных аналога элеутеробина.
Список литературы:
1 B. H. Long, J. M. Carboni, A. J. Wasserman, L. A. Cornell, A. M. Casazza, P. R. Jensen, T. Lindel, W. Fenical, C. R. Fairchild. Eleutherobin, a novel cytotoxic agent that induces tubulin polymerization, is similar to paclitaxel. Cancer Research, 1998, 58, .
2 D. J. Newman, G. M. Cragg. Advanced preclinical and clinical trials of natural products and related compounds from marine sources. Curr. Med. Chem, 2004, 11, 1693.
3 , , . Успехи в синтезе полигидроксипроизводных 8-оксабицикло[3.2.1]октана. Башкирский химический журнал, 2010, 17, 148-149.
4 D. A. Khlevin, S. E. Sosonyuk, M. V. Proskurnina, N. S. Zefirov. Stereoselective synthesis of highly substituted 8-oxabicyclo[3.2.1]octanes and 2,7-dioxatricyclo[4.2.1.03,8]nonanes. Tetrahedron 2012, 68, 5785–5792.
УДК 542.91:547.1’128
А.С. Солдатенко, С.В. Басенко, М.Г. Воронков
НОВЫЕ Si-ПЕРМЕТИЛЦИКЛО(1-МЕТОКСИФОСФОНА)СИЛОКСАНЫ
Федеральное государственное бюджетное учреждение науки Иркутский институт химии им. СО РАН, г. Иркутск
E-mail: *****@
Химия фосфорсодержащих циклогетеросилоксанов, продолжает привлекать внимание ученых [1-6].
Развивая исследования по поиску новых методов низкотемпературной генерации диорганилсиланонов, мы изучили взаимодействие диметил-дихлорсилана с триметилфосфатом. Реакция протекает уже при комнатной температуре, в отсутствии растворителя. По данным ЯМР 1Н, 13С, 29Si, 31P и хромато-масс-спектрометрии продуктами реакции являются P-метокси-фосфона-Si-гексаметилциклотри- (1) 38% и - циклотетрасилоксаны (2) 33%, а также перметилциклосилоксаны Dm [m = 3 (3) 4%, 4 (4) 15%, 5 (5) 10%]:
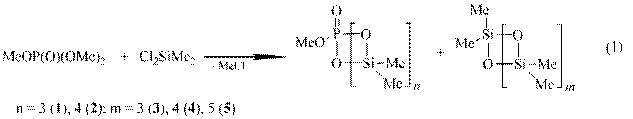
На начальном этапе реакции диметилдихлорсилана с триметилфосфатом ЯМР мониторинг обнаружил образование линейного диметил(диметокси-фосфаноилокси)хлорсилана (6),
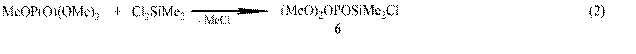
который через стадию внутримолекулярной циклизации распадается с образованием диметилсиланона и метилметафосфата:
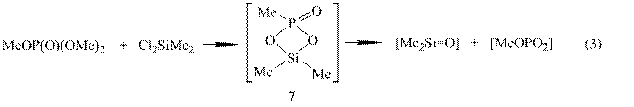
Диметилсиланон внедряется в соединения 6 и 7 с образованием (MeO)2OP(OSiMe2)2Cl, P-метоксифосфона-Si-гексаметилциклотри- (1) и –ци-клотетрасилоксанов (2).
При взаимодействии 1,3-дихлортетраметилдисилоксана с триметил-фосфатом методами ЯМР 1Н, 13С, 29Si, 31P был зафиксирован шестичленный
P-метоксифосфона-Si-тетраметилциклодисилоксан (8), однако конечными продуктами реакции являются восьми-, десяти - и двенадцатичленные P-метоксифосфона-Si-метилциклосилоксаны 1, 2, 9 с выходами 65, 31 и 4% соответственно:
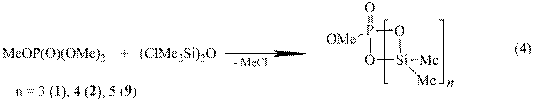
ЯМР мониторинг реакции (4) показал первоначальное образование 1,1,3,3-тетраметил-1-диметоксифосфаноилокси-3-хлордисилоксана (10),
![]()
а также 1,1,3,3,5,5-гексаметил-1-диметоксифосфаноилокси-5-хлортрисилоксана (11), продукта внедрения диметилсиланона в фосфордисилоксан:
![]()
Однако, как и в реакции с диметилдихлорсиланом, основными продуктами по данным ЯМР 1Н, 13С, 29Si, 31P и хромато-масс-спектрометрии оказались P-метоксифосфона-Si-гексаметилциклотри- (1), - циклотетрасилокса-ны (2), перметилциклосилоксаны 3-5.
Полученные результаты указывают на высокую лабильность исследуемых нами циклических фосфорсилоксановых структур, уменьшающуюся в ряду 7 > 8 > 1 > 2 > 9.
Список литературы:
1 , , Лукевиц производные фосфора и серы. Ленинград: Химия, 1968, 292 С.
2 Borisov S. N., Voronkov M. G., Lukevits E. J. Organosilicon Derivatives of Phosphorus and Sulfur. New York, London: Plenum Press, 1971, 343 P.
3 , , Роман соединения неметаллов. Производные азота и фосфора. Новосибирск: Наука. 1988. С. 146.
4 Voronkov M. G., Maletina E. A., Roman V. K. Heterosiloxanes. Derivatives of nitrogen and phosphorus. London: Hardwood academic publishers. 1991. P. 489.
5 Haoudi-Mazzah A., Dhamelincourt P., Mazzah A., Lazraq M. // J. Raman Spectrosc. 1998. V. 29, N 12. P. 1047.
6 Hänish von C., Hampe O., Weigend F., Stahl S. // Angew. Chem. Int. Ed. 2007. V. 46, N 25. P. 4775.
УДК 547.426.23
, ,
, ,
СИНТЕЗ ОПТИЧЕСКИ ЧИСТЫХ МАКРОГЕТЕРОЦИКЛОВ
С ГИДРАЗИДНЫМ И СЛОЖНОЭФИРНЫМИ ФРАГМЕНТАМИ
ИЗ l-МЕНТОЛА И ТРИГЛИЦЕРИДА РИЦИНОЛЕВОЙ КИСЛОТЫ
Институт органической химии УНЦ РАН, г. Уфа
E-mail: *****@***ru
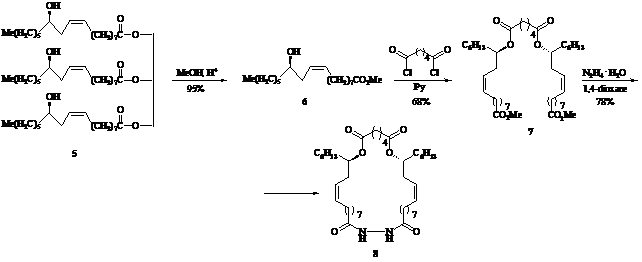
В данном сообщении представлен короткий и эффективный синтез оптически чистых содержащих гидразидный фрагмент макролидов (4) и (8) – соединений с потенциально комплексообразующими свойствами и биологической активностью, исходя из природных l-ментола (1) и касторового масла (5).
Синтезы макрогетероциклов (4) и (8) основаны на последовательно протекающих реакциях [2+1]-конденсации гидроксиэфиров (2) и (6) с хлорангидридами глутаровой и адипиновой кислот соответственно и [1+1]-взаимодействия полученных бис-производных (3) и (7) с гидразингидратом при комнатной температуре в 1,4-диоксане (мольное соотношение субстрат : реагент : растворитель, 1:1:100).
Строение макролидов (4) и (8) установлено методами ИК, ЯМР 1Н и 13С спектроскопии и хромато-масс-спектрометрии высокого разрешения, чистота подтверждена методом ВЭЖХ.
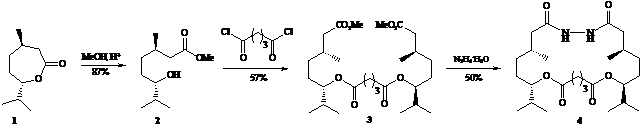
УДК 547.475.124
, ,
,
ГИДРОБОРИРОВАНИЕ-ОКИСЛЕНИЕ СЛОЖНОЭФИРНЫХ ПРОИЗВОДНЫХ РИЦИНОЛЕВОЙ КИСЛОТЫ
Институт органической химии УНЦ РАН, г. Уфа
E-mail: *****@***ru
Ранее [1] было показано, что в реакции гидроборирования-окисления оптически активный центр непредельных спиртов (I и II) – производных рицинолевой кислоты – незначительно влияет на региоселективность, о чем свидетельствует преобладание на 6 и 10% 1,3-диолов (III и IV) над их
1,4-изомерами (V и VI) соответственно, но индуцирует образование новых асимметрических центров преимущественно (S)-конфигурации, что доказано циклизацией 1,3-гликолей (III, IV) (de 32 и 50% соответственно) в соответствующие стереоизомерные 1,3-диоксаны, а 1,4-диолов (V и VI) (de 40 и 22% соответственно) – в 2,5-диалкилзамещенные тетрагидрофураны.
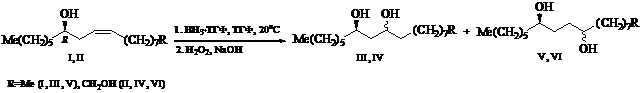
В продолжение исследований по влиянию оптически активного
12R-центра в рицинолевой кислоте на регио - и стереоселективность реакции гидроборирования-окисления двойной связи использованы его сложноэфирные производные – касторовое масло (содержание рицинолевой кислоты ~90%) (VII) и метиловый эфир (VIII).
При взаимодействии касторового масла (VII) даже с двухмольным избытком ВН3•ТГФ (ТГФ, 20оС) двойная связь не затрагивается, при этом проходит лишь гидридное восстановление карбоксильной группы с образованием непредельного диола (II) (табл., оп. 1). Инертность триглицерида (VII) по отношению к комплексу ВН3•ТГФ в этих условиях мы объясняем стерическими факторами.

В более жестких условиях (кипячение) триглицерид (VII) с 85% выходом превращен в смесь (57:43, по данным ВЭЖХ и ЯМР 1Н) 1,3- (IV) и
1,4-региоизомерных (VI) триолов – продуктов восстановления сложноэфирной группы и гидроборирования-окисления двойной связи (табл., оп. 2).
Гидроборирование метилового эфира (VIII) избытком ВН3•ТГФ при комнатной температуре приводило после окисления щелочной перекисью водорода к смеси и (87:13) региоизомерных триолов IV и VI (табл., оп.3), тогда как при кипячении региоселективность несколько снижалась, и была получена смесь (72:28) тех же региоизомеров (табл., оп. 4).
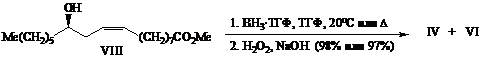
Сравнительный анализ спектров ЯМР 1,3- (IV)- и 1,4- (VI) - триолов со спектрами соединений III-VI, полученных при гидроборировании енолов I и II [2], показывает, что во всех случаях преобладают диастереомеры с
(S)-конфигурацией образующихся асимметрических центров. Данные по регио - и стереоселективности гидроборирования-окисления производных рицинолевой кислоты (VII и VIII) приведены в таблице.
Таблица - Состав продуктов гидроборирования-окисления производных рицинолевой кислоты (VII и VIII)
№ опыта | Исходное соеди-нение | темпера-тура реакции, оС | Содержание IV в реакционной смеси, % | Соотношение (10S,12R)-/(10R,12R)-IV | Содержание VI в реакционной смеси, % | Соотношение (9S,12R)-/(9R,12R)-VI |
1 | VII | 20 | - | - | ||
2 | VII | Δ | 57 | 1.8 : 1.0 | 43 | 1.0 : 1.0 |
3 | VIII | 20 | 87 | 5.0 : 1.0 | 13 | 1.0 : 0 |
4 | VIII | Δ | 72 | 1.3 : 1.0 | 28 | 5.0 : 1.0 |
Таким образом, в реакции гидроборирования-окисления среди производных рицинолевой кислоты наибольшая регио - и стереоселективность наблюдается для метилового эфира рицинолевой кислоты, о чем свидетельствует преобладание на 74% 1,3-диола над его 1,4-изомером и асимметрических центров преимущественно (S)-конфигурации: 1,3-гликолей до 87% и 1,4-диолов до 100%.
Список литературы:
1 , , Ж. орган. химии. 2008, 44, 1145.
УДК 547.256.2+547.473.41
, ,
, ,
НИЗКОТЕМПЕРАТУРНОЕ ВОССТАНОВЛЕНИЕ
МЕТИЛ-3R,7-ДИМЕТИЛ-6S-ГИДРОКСИОКТАНОАТА
ДИИЗОБУТИЛАЛЮМИНИЙГИДРИДОМ В ДИХЛОРМЕТАНЕ
Институт органической химии УНЦ РАН, Уфа, Россия
Е-mail: *****@***ru
Ранее [1] нами сообщалось об образовании О-изобутилового ацеталя
(-)-ментолактола (2) по новой реакции в химии алюминийорганических соединений – образование О-изобутильных производных семичленных лактолов в процессе низкотемпературного (-70оС) восстановления оксепанонов избытком (³ 2 экв.) диизобутилалюминийгидрида в хлористом метилене.
Нами обнаружено, что этот же циклический ацеталь (2) является главным продуктом [наряду с минорным лактолом (4)] в реакции низкотемпературного (-70оС) восстановления метил (3R,6S)-6-гидрокси-3,7-диметилоктаноата (3) – ациклического продукта метанолиза лактона (1) – диизобутилалюминийгидридом (4 экв.) в том же растворителе.

Список литературы:
1. , , Толстиков реакция в химии алюминийорганических соединений // Ж. орган. химии, 2011, Т. 47, Вып. 3. С. 471-472.
УДК 547.256.2+547.473.41-314
, ,
, ,
НОВЫЕ ПРИМЕРЫ НОВОЙ РЕАКЦИИ В ХИМИИ АЛЮМИНИЙОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Институт органической химии УНЦ РАН, г. Уфа
Е-mail: *****@***ru
Ранее нами сообщалось о новой реакции в химии алюминийорганических соединений – образование О-изобутильных производных семичленных лактолов (1-3) в процессе низкотемпературного (-70оС) восстановления
(-)-ментолактона (4), карвоментолактона (5) и α-камфолида (6) избытком (³ 2 экв.) диизобутилалюминийгидрида в хлористом метилене [1].
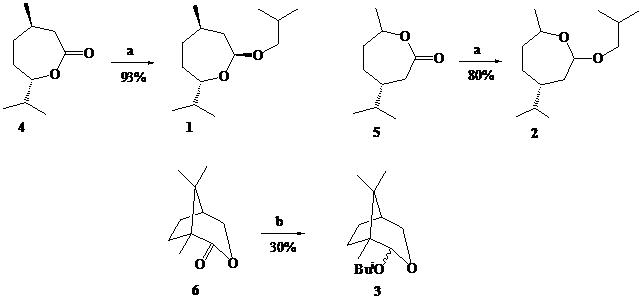
Реагенты: a. 2 eq. Bui2AlH, CH2Cl2, –70oC; b. 6 eq. Bui2AlH, CH2Cl2, –70oC.
В данном сообщении представлены новые примеры этой реакции – образование О-изобутилоксепанолов (11-13) – при восстановлении в тех же условиях адамантанолактона (7), b-камфолида (8) и лактона (10), полученного, в свою очередь, из аллобетулина (9) по методу [2].
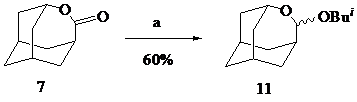
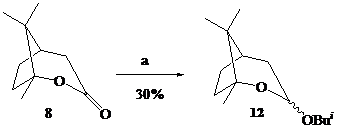

Реагенты: a. 4 eq. Bui2AlH, CH2Cl2, –70oC.
Список литературы:
1 , , // Ж. орган. химии, 2011, Т. 47, Вып. 3, С. 471-472.
2 Pradhan B. P., Chakraborty S. // Tetrahedron Lett., 1989, V. 30, N 40, P. .
УДК 542.943.5 + 546.172 + 547.313 + 547.497.1
Г.Ю. Ишмуратов, Ю.В. Легостаева, Л.П. Боцман, Л.Р. Гарифуллина,
, ,
ПРЕВРАЩЕНИЯ ПЕРЕКИСНЫХ ПРОДУКТОВ ОЗОНОЛИЗА ОЛЕФИНОВ В СИСТЕМЕ «МЕТАНОЛ-ВОДА»
Институт органической химии УНЦ РАН, г. Уфа
E-mail: insect@anrb.ru
Представлены результаты превращений перекисных продуктов озонолиза олефинов различной степени замещенности (1) – (4) под действием азотсодержащих органических соединений (гидрохлоридов семикарбазида и гидроксиламина) в системе «метанол-вода».
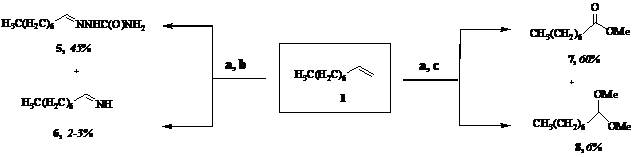
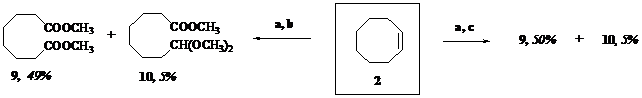
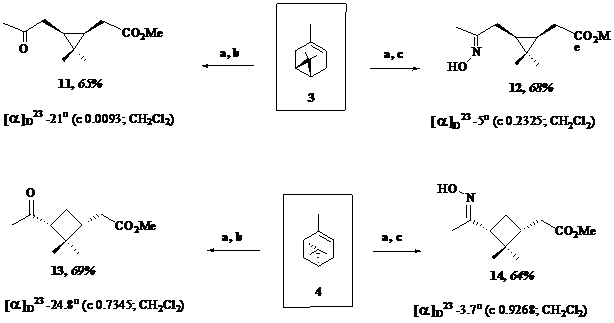
a) O3, MeOH - H2O, 0oC; b) NH2C(O)NHNH2×HCl; c) NH2OH×HCl.
УДК 542.943.5 + 547.596
Г.Ю. Ишмуратов, В.С. Тухватшин, А.В. Баннова, Э.Р. Латыпова,
ПРЕВРАЩЕНИЯ ПЕРЕКИСНЫХ ПРОДУКТОВ ОЗОНОЛИЗА
(R)-4-МЕНТЕН-3-ОНА ПОД ДЕЙСТВИЕМ АЗОТСОДЕРЖАЩИХ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Институт органической химии УНЦ РАН, г. Уфа
Башкирский государственный университет
E-mail: *****@***ru
Ранее нами были представлены [1] пути превращений (R)-4-ментен-3-она (I) в реакции озонолиза, осуществляемой в среде апротонных растворителей (CH2Cl2 или CCl4) и их смесей с метанолом, которые заключались в перегруппировке промежуточного цвиттер-иона (II) в смешанный ангидрид (3R)-метил-5-оксопентановой и изомасляной кислот (III) либо в стабилизации интермедиата (II) в виде α-метоксигидропероксида (IV) соответственно. Этот перекисный продукт, как и ангидрид (III) и, вероятно, через стадию образования последнего, переводился кислотным метанолизом в ацеталеэфир (V).
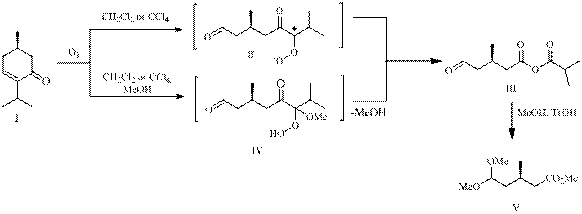
В данном сообщении нами приведены результаты исследований озонолитических превращений сопряженного циклоенона (I) в среде хлористого метилена или метанола и их смеси в присутствии азотсодержащих органических соединений (пиридин, триэтиламин, гидрохлорид семикарбазида) – известных акцепторов пероксидного кислорода.
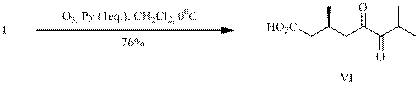
Установлено, что проведение озонолиза енона (I) в хлористом метилене с добавкой пиридина приводит с хорошим выходом к дикетокислоте (VI) (опыт А).
При замене хлористого метилена на метанол и сохранении остальных параметров (опыт В) с высоким выходом получен монометиловый эфир
(3R)-метилглутаровой кислоты (VII) – полупродукт в синтезах митозенов, проявивших фармакологическую активность против кишечной палочки и лейкемии у мышей; производных веррукарина, обладающих противоопухолевой, фунгицидной, цитотоксической, антибактериальной активностью, кетона Виндауза и Грундмана – синтона для витаминов D2 и D3.
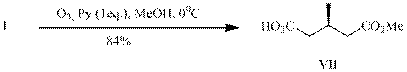
Применение в качестве растворителя в реакции озонолиза смеси (1:1) хлористого метилена и метанола (опыт С) снизило выход эфирокислоты (VII) до 63%. При этом в качестве минорных продуктов были зарегистрированы дикетокислота (VI), кетоэфир (VIII) – полупродукт в синтезе
(S)-(+)-гидропрена, и альдегидоэфир (IX).
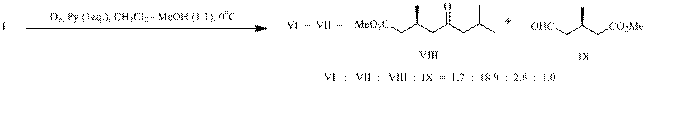 Аналогичные результаты были получены при замене пиридина на триэтиламин (опыт D).
Аналогичные результаты были получены при замене пиридина на триэтиламин (опыт D).
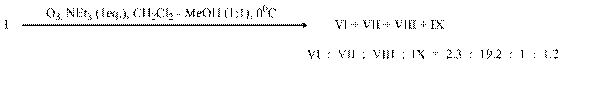
Использование для превращения перекисного продукта озонолиза циклоенона (I), образующегося в смеси (1:1) хлористого метилена и метанола, солянокислого семикарбазида (опыт Е) дало с высоким выходом ацеталеэфир (V) – ключевой синтон в синтезе целого ряда низкомолекулярных биорегуляторов насекомых.
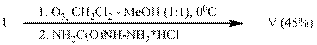
Список литературы:
1 , , ЖОрХ. 2002, 38, 1047.
УДК 547.512:547.25: 547.333
,1 ,2 ,2
,2 3
Новый метод получения циклопропилзамещенных аминов
1Башкирский государственный университет, инженерный факультет,
г. Уфа, E-mail: iramazan@inbox.ru
2 Федеральное государственное бюджетное учреждение науки
Институт нефтехимии и катализа РАН, г. Уфа.
3 Федеральное государственное бюджетное учреждение науки
Институт органической химии им. , г. Москва.
В последние годы авторы статьи развили новый подход к синтезу циклопропановых соединений, основанный на взаимодействии замещенных ацетиленов и алленов с карбеноидами алюминия [1,2]. В реакцию были успешно вовлечены пропаргиловые спирты и пропаргиламины [3,4]. Несмотря на простоту получения карбеноидов алюминия, их реакции с соединениями олефинового ряда были мало изучены. Так, к моменту начала наших исследований были известны лишь единичные примеры циклопропанирования карбеноидами алюминия гераниола, периллилового спирта, γ‑кремнийзамещенных аллиловых спиртов [5-7]. В продолжение наших исследований с целью разработки общего метода селективного получения функционально-замещенных циклопропанов изучены реакции карбеноидов алюминия с рядом ненасыщенных аминов.
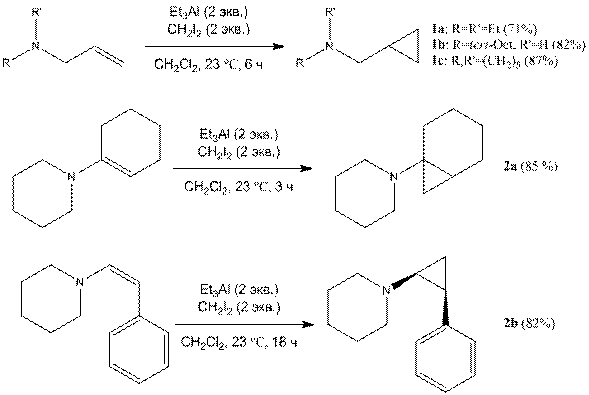
Нами установлено, что замещенные аллиламины и енамины (аллилдиэтиламин, аллил-трет-октиламин, аллилпиперидин, 1‑циклогексенилпиперидин, (Z)-1-стирилпиперидин) реагируют с двумя эквивалентами Et3Al и CH2I2 при комнатной температуре в дихлорметане с образованием соответствующих циклопропилметиламинов 1a-с и циклопропиламинов 2a, 2b с высокими выходами (71-87%). Аналогично, с высоким выходом продукты циклопропанирования образуются при проведении реакции в гексане. Использование в качестве растворителя бензола и толуола нежелательно вследствие побочной реакции алкилирования ароматического ядра. Проведение реакции в тетрагидрофуране и диэтиловом эфире ингибируют сам процесс образования карбеноидов алюминия из CH2I2 и Et3Al. В случае енаминов превращение проходит с сохранением конфигурации заместителей при двойной связи.
Преимущества предложенной методологии можно продемонстрировать на примере циклопропанирования 1-циклогексенилпирролидина. Продукт циклопропанирования был получен лишь с 8% выходом при использовании процедуры Симмонса-Смита (CH2I2-Cu/Zn) [8], с 48% выходом с помощью реагента Фурукава (CH2I2-Et2Zn) [9] и с 22% выходом посредством реагента CH2Br2-Zn/Cu-AcCl [10]. Наилучший результат (61%) был достигнут при использовании диазометана в присутствии каталитических количеств CuCl2 [9]. Предлагаемый реагент CH2I2-Et3Al позволяет получать 1‑аминобицикло[n.1.0]алканы с гораздо более высоким выходом. Мы не обнаружили следов исходного енамина в реакционной массе после завершения реакции, что является важным преимуществом при выделении продукта циклопропанирования в чистом виде методом вакуумной дистилляции, поскольку температуры кипения исходного субстрата и продукта превращения очень близки.
Список литературы:
1 I. R. Ramazanov, L. K. Dil'mukhametova, U. M. Dzhemilev, O. M. Nefedov, J. Organomet. Chem., 2010, 695, .
2 I. R. Ramazanov, A. V. Yaroslavova, U. M. Dzhemilev, O. M. Nefedov, Tetrahedron Lett., 2010, 51, .
3 I. R. Ramazanov, A. V. Yumagulova, U. M. Dzhemilev and O. M. Nefedov, Tetrahedron Lett., 2009, 50, .
4 I. R. Ramazanov, A. V. Yaroslavova, L. M. Khalilov, U. M. Dzhemilev, O. M. Nefedov, Russ. Chem. Bull., 2010, 59, .
5 К. Maruoka, Y. Fukutani, H. Yamamoto, J. Org. Chem., 1985, 50, 4412–4414.
6 A. B. Charette, A. Beauchemin, J. Organomet. Chem., 2001, 617-618, 702-708.
7 Y. Ukaji, K. Inomata, Chem. Lett., 1992, .
8 E. P. Blanchard , H. E. Simmons, J. S. Taylor, J. Org. Chem., 1965, 30, 4321–4322.
9 M. E. Kuehne, J. C. King, J. Org. Chem., 1973, 38, 304–311.
10 E. C. Friedrich , E. J. Lewis, J. Org. Chem., 1990, 55, 2491–2494.
УДК 634.0.813.2:542.61
Г.Г. Аминева, Н.С. Борисова, Ю.С. Зимин, А.Г. Мустафин

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 |




