Башкирский государственный университет
Институт физики молекул и кристаллов УНЦ РАН
E-mail: *****@***ru
Одним из методов модификации свойств полимеров является введение в состав макромолекул функциональных групп различной химической природы. Удобным объектом для осуществления химической модификации являются 1,2-полибутадиены (ПБ), содержащие боковые двойные углерод-углеродные связи.
В настоящей работе был осуществлён синтез жидкокристаллического (ЖК) фрагмента с целью его дальнейшего присоединения к стереорегулярному 1,2-полибутадиену с синдиотактической структурой, что должно привести к получению нового ЖК полимера.
Для синтеза ЖК фрагмента использовали стандартный ЖК 4-окси-4-дифенил-1-карбонитрил 5, который был модифицирован по следующим схеме (схема1):
· синтез 4’ - [(6-бромгексил) окси] дифенил-4-карбонитрила 4;
· синтез тиоурониевой соли 3;
· синтез 4’- [(6-тиогексил) окси] дифенил-4- карбонитрила 1;
При взаимодействие 4-окси-4-дифенил-1-карбонитрил 5 с 1,6-дибромгексаном в спирте получили 4’-[(6-бромгексил) окси] дифенил-4-карбонитрил 4, который был вовлечен в реакцию с тиомочевиной с образованием тиоуронивой соли 3. Синтез 4’- [(6-тиогексил) окси] дифенил-4- карбонитрила 1 в дальнейшем вели через образование тиолята калия и его подкисления уксусной кислотой. Продукт 1 выделяли с помощью экстракции из хлороформа, выход 33%.
Схема 1


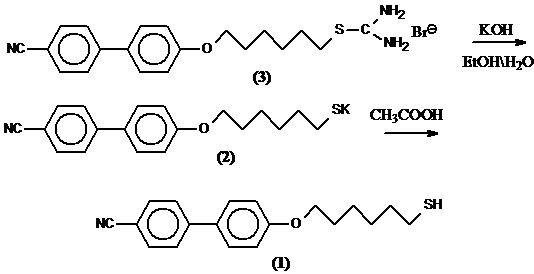
Структура всех соединений подтверждена спектрами ЯМР и ИК спектроскопии.
Таким образом, на основе 4-окси-4-дифенил-1-карбонитрила синтезирован 4’- [(6-тиогексил) окси] дифенил-4- карбонитрил – ЖК фрагмент для дальнейшего присоединения его к двойным связям 1,2-СПБ.
УДК 615.322
, ,
ВЛИЯНИЕ КАВИТАЦИИ НА ВЫДЕЛЕНИЕ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ МЕТОДОМ ЭКСТРАКЦИИ
ФГБОУ Башкирский государственный университет, г. Уфа
E-mail: *****@***ru
Растительное сырье является богатым источником ценных биологически активных веществ различного спектра действия. Они получаются в качестве главных компонентов биосинтеза, либо как вторичные метаболиты и играют важную роль во многих биохимических процессах, протекающих в растительном и животном мире. Следует отметить также, что многие физиологически активные соединения, используемые человеком для регулирования своей жизнедеятельности впервые были выделены из натурального сырья и только затем получены с помощью химических или биохимических методов. Однако, несмотря на то, что современная органическая химия обладает достаточным арсеналом средств и методов синтеза даже очень сложных молекул, сырье растительного и животного происхождения и в настоящее время служит основным источником многих ценных биологически активных соединений. Так в современном арсенале лекарственных средств на долю препаратов на основе экстрактивных веществ растительного происхождения приходится 30-40%. Это в равной степени относится к парфюмерно-косметической и пищевой промышленности.
Поскольку многие биологически активные компоненты присутствуют в растениях в небольших количествах, то необходимо обращать внимание на эффективность методов, используемых для их извлечения из природных источников. Поэтому наряду с традиционными подходами необходимо рассматривать и новые методы, позволяющие наиболее полно извлекать ценные вещества из природного материала. Вопрос наиболее рационального выбора средств и методов экстрактивного выделения полезных компонентов важен как с технологической так и с экономической точки зрения.
Целью данной работы является изучение влияния кавитации на эффективность выделения полифенольных соединений экстракцией из плодовых оболочек гречихи.
Извлечение полифенольных соединений проводили водными растворами этанола различной концентрации. Дистиллированную воду, используемую для приготовления растворов, предварительно подвергали кавитации на аппарате, изготовленном в Самарском аэрокосмическом университете.
Доказательством образования кластеров в водно-спиртовых растворах при использовании кавитированной воды служат данные ЯМР 1Н спектра, согласно которым происходит смещение Δδ на 0,08 м. д. по сравнению с исходной, некавитированной водой.
Показано, что экстракция кавитированными растворами позволяет увеличить выход полифенольных соединений из плодовых оболочек гречихи на 4 %, причем соотношение спирт – вода играет ключевую роль, в то время как кавитации можно подвергать растворитель или раствор в момент экстракции.
Нами изучено влияние присутствия полифенольных соединений на структурирование в растворе и размер кластеров. С этой целью на лазерном анализаторе наночастиц Shimadzu SALD-7101 было определено сравнительное молекулярно-массовое распределение частиц относительно исходных кавитированных водно-спиртовых растворов (табл.).
Таблица - Средние значения размеров частиц в экстрагированных водно-спиртовых растворах.
Исследуемые растворы | Среднее значение размеров частиц при перемешивании растворов, нм | Среднее значение размеров частиц при остановке перемешивания растворов, нм |
Экстракт | 0,178 | 0,020 |
Экстракт | 0,300 | 0,102 |
Экстракт | 0,110 | 0,020 |
Экстракт | 0,121 | 0,102 |
Экстракт | 0,137 | 0,020 |
Данные таблицы свидетельствуют в пользу того, что экстрагируемое вещество не включается в организованные кластеры растворителя, а разрушает их, по-видимому, образуя собственную сольватную оболочку.
Таким образом, в результате проведенных исследований был предложен технологичный метод экстракции суммы флавоноидов из шелухи гречихи, заключающийся в обработке сырья 70%-ным раствором этанола в предварительно кавитированной воде, позволяющий увеличить выход на 4%. Также было установлено, что эффект кавитации сохраняется в воде в течение 20 суток, в последующем плавно затухает.
УДК 579.66
, ,
ИССЛЕДОВАНИЕ РОСТА ГРИБА MORTIERELLA ALPINA ГР-1 – ПРОДУЦЕНТА АРАХИДОНОВОЙ КИСЛОТЫ НА РАСТИТЕЛЬНЫХ СУБСТРАТАХ И ОТХОДАХ ПРОИЗВОДСТВА ПОДСОЛНЕЧНОГО МАСЛА
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Уфимский государственный нефтяной технический университет, г. Уфа
Е-mail: *****@***net
В современном сельскохозяйственном производстве используются различные средства защиты растений от болезней, насекомых и разнообразных воздействий среды. Большинство из них являются синтетическими, используются в высоких концентрациях и не разрушаются ферментативными системами растений. Это приводит к накоплению таких соединений в сельхозпродуктах и, как следствие, в организме людей и животных.
Известно, что растения способны синтезировать собственные защитные соединения в ответ на неблагоприятные климатические условия и заражение патогенными микроорганизмами. Но скорость их биосинтеза может быть недостаточно высокой. В связи с этим требуются экзогенные биологически активные вещества, которые могут активировать уже идущие иммунные процессы или индуцировать новые механизмы защиты. В этом аспекте особое внимание заслуживают регуляторы нового поколения, воздействующие на растения в минимальных дозах.
Перспективным действующим соединением для создания препаратов, модулирующих иммунную систему растений является арахидоновая кислота и ее эфиры низших спиртов, которые уже используются в сельском хозяйстве в качестве стимулятора устойчивости растений к фитопатогенам (как в процессе их культивирования, так и хранения).
Основными природными источниками эфиров арахидоновой кислоты, использующимися при производстве этих препаратов являются печень и надпочечная железа животных, желток куриных яиц, а также морские водоросли. Однако содержание арахидоновой кислоты в этих источниках настолько мало, что они не могут удовлетворить растущую потребность в этой физиологически активной кислоте. Кроме того, требуются значительные затраты на ее очистку от сопутствующих жирных кислот.
Ограниченность природных источников арахидоновой кислоты диктует необходимость развития ее микробиологического производства. В настоящее время процессы получения арахидоновой кислоты с использованием различных штаммов грибов рода Mortierella запатентованы в Европе, Китае, Японии и США. Промышленное производство микробных липидов с высоким содержанием арахидоновой кислоты.
В настоящей работе с целью поиска экономичного и эффективного метода получения биомассы Mortierella alpina ГР-1 – продуцента арахидоновой кислоты был исследован рост гриба на различных растительных субстратах и отходах их переработки (сусло-агаре, овсе, пшенице, ячмене, рисе, шроте и жмыхе производства подсолнечного масла).
В результате исследования культивирования гриба Mortierella
alpina ГР-1 при 25 оС в течение 20 суток было обнаружено, что гриб способен эффективно расти на большинстве исследованных субстратов, за исключением отходов производства подсолнечного масла. Установлено, что на среде с сусло-агаром наиболее активно развивается субстратный мицелий, тогда как воздушный мицелий, из которого затем выделяются липиды, образуется медленно. Наиболее эффективной средой для формирования воздушного мицелия является овсяная среда, содержащая 1-3% глицерина. Показано, что отходы производства подсолнечного масла могут быть использованы как добавки к овсяной среде (10 – 50%).
УДК 620.193.10
,
СНИЖЕНИЕ БИОЛОГИЧЕСКИХ ОБРАСТАНИЙ ПОСРЕДСТВОМ ИСПОЛЬЗОВАНИЯ РЕАГЕНТА КОМПЛЕКСНОГО ДЕЙСТВИЯ
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования Уфимский государственный нефтяной технический университет, г. Уфа
E-mail: *****@***ru
Эффективность производства любого нефтехимического комплекса тесно связана с высоким потреблением сырьевых и энергетических ресурсов – в частности, с необходимостью использования огромного количества очищенной воды.
Опыт эксплуатации систем оборотного водоснабжения как средства оптимизации водных потоков показал, что водный режим оборотных систем создает большой потенциал для возникновения биологического обрастания, что ведет к интенсивной коррозии оборудования [1].
Поскольку в настоящее время методики, удовлетворяющей потребностям микробиологического экспресс-анализа не существует, была разработана методика исследования эффективности действия биодисперсантов. Предложенная методика основана на определении прироста биомассы на образцах в случае использования биоцида «Railan bio», дисперсанта «ОП-7» или биодисперсанта.
Предварительно эффективность дисперсанта определяли визуальным методом. Для выбора эффективного бактерицида оценивали микробиологический рост аэробных бактерий с помощью тестов «Easicult Combi».[2]
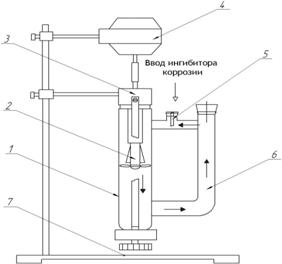
1 – U-образная ячейка; 2 – мешалка; 3 – герметичный привод; 4 – электродвигатель; 5 – образцы; 6 – испытуемая среда; 7 – штатив
Рисунок 1 – Принципиальная схема установки
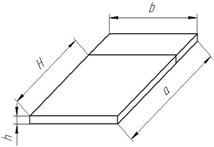
Рисунок 2 – Образец для испытания
Результаты испытаний реагентов по предложенной методике представлены в Таблице 1. Максимальный защитный эффект может быть достигнут путем использования биодисперсанта (99,2 %).
Эффективность реагентов рассчитали по формуле:
![]()
где Z – степень защиты материала от коррозии, %;
K0 – скорость коррозии в контрольной среде, г/м2⋅час;
Km – скорость коррозии в защищенной среде, г/м2⋅час.
Таблица 1 - Результаты испытаний биоцида, дисперсанта и биодисперсанта
Рабочая среда | Масса образца до испытания m0, г | Масса образца после испытания m1, г | Изменение массы ∆m, г | Эффективность реагента Z, % | ||
Оборотная вода | 3,5890 | 3,5884 | 3,6015 | 3,6010 | 0,0126 | - |
3,5882 | 3,6003 | |||||
3,5880 | 3,6011 | |||||
Оборотная вода с дисперсантом «ОП-7» | 3,5923 | 3,5902 | 3,5956 | 3,5960 | 0,0058 | 53,5 |
3,5899 | 3,5953 | |||||
3,5885 | 3,5971 | |||||
Оборотная вода с биоцидом «Railan bio» | 3,5896 | 3,5885 | 3,5889 | 3,5894 | 0,0009 | 92,9 |
3,5874 | 3,5894 | |||||
3,5886 | 3,5899 | |||||
Оборотная вода с биодисперсантом | 3,5889 | 3,5886 | 3,5890 | 3,5887 | 0,0001 | 99,2 |
3,5879 | 3,5887 | |||||
3,5889 | 3,5884 |
В ходе данной работы было экспериментально показано, что применение биодисперсанта, обладающего как диспергирующими так и биоцидными свойствами позволяет существенно снижать количество биоотложений, а следовательно и скорость коррозии на металле внутренней поверхности оборудования, способствуя тем самым уменьшению удельной аварийности в системах оборотного водоснабжения.
Список литературы:
1 / / Защита от коррозии, старения и биоповреждеиий машин, оборудования и сооружений. – 1987. – М. – Т. 1 – С. 687. – Т. 2 – С. 783.
2 / / Методика выделения микроорганизмов, способных развиваться в аэробных и анаэробных условиях в зависимости от конечного акцептора электронов. – 1987 – М. – С. 92-93.
УДК 004.94
1, 2
вопросы математического моделирования физиологических процессов
1,
2Башкирский государственный университет, г. Уфа
E-mail: lindyub@yandex.ru
Одним из наиболее важных, но недостаточно изученных физиологических процессов является мышечная активность. С мышечным сокращением связано функционирование всех систем в организме человека, любое нарушение в работе мышц может привести к различным патологиям или даже к летальному исходу. Поэтому изучение процессов, происходящих в сокращающейся мышце, является одной из важных и актуальных задач биомеханики. В данной работе рассматривается механизм мышечного сокращения на молекулярном уровне, то есть в элементарной сократительной единице мышцы – саркомере.
Изучение молекулярных механизмов мышечного сокращения связано с определенными трудностями, которые, главным образом, заключаются в сложности отслеживания этих механизмов непосредственно в мышце. Исследование же изолированных сократительных белков может дать только косвенную информацию о процессе мышечного сокращения. Таким образом, актуальным является исследование молекулярных механизмов мышечного сокращения путем математического моделирования, основанного на знаниях о молекулярной конструкции саркомера и его физико-химических свойствах.
Механизм мышечного сокращения основан на взаимодействии актиновых и миозиновых нитей, которое осуществляется за счет энергии, выделяющейся при расщеплении молекулы АТФ до АДФ и фосфорной кислоты [1].
Для исследования кинетики протекания указанных реакций авторами на основе закона действующих масс построена математическая модель, представляющая собой задачу Коши для системы обыкновенных нелинейных дифференциальных уравнений:
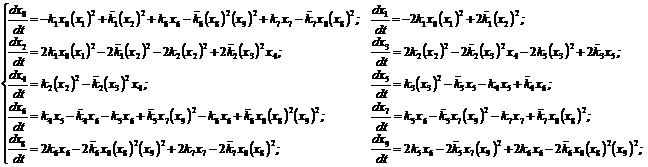 с начальными условиями: xi(t0)=xi0.
с начальными условиями: xi(t0)=xi0.
Здесь xi, i=0,…,9 – концентрации веществ, участвующих в акте мышечного сокращения, ![]() и
и ![]() , i=1,…,7 – соответственно, кинетические константы скоростей прямой и обратной стадий, t – время протекания реакции, t0 – начальное время.
, i=1,…,7 – соответственно, кинетические константы скоростей прямой и обратной стадий, t – время протекания реакции, t0 – начальное время.
Для полученной системы были решены прямая и обратная кинетические задачи. Прямая задача решена методом Кутты-Мерсона с динамической проверкой выполнения законов сохранения. Решение обратной задачи сводится к нахождению минимума критерия оптимизации, для которого предложен адаптированный вариант генетического алгоритма [2]. Для решения обратной кинетической задачи был поставлен псевдоэксперимент путем решения прямой задачи для набора кинетических констант, определенных на основании физико-химических соображений: k1=10, k2=0,1, k3=1, k4=5, k5=1, k6=1, k7=1, ![]() =1,
=1, ![]() =1,
=1, ![]() =1,
=1, ![]() =0,5,
=0,5, ![]() =1,
=1, ![]() =1,
=1, ![]() =0,5. В результате был получен следующий набор кинетических констант: k1=2,1, k2=0,1, k3=1,1, k4=4,3, k5=2,2, k6=2,3, k7=0,8,
=0,5. В результате был получен следующий набор кинетических констант: k1=2,1, k2=0,1, k3=1,1, k4=4,3, k5=2,2, k6=2,3, k7=0,8, ![]() =0,2,
=0,2, ![]() =1,
=1, ![]() =1,2,
=1,2, ![]() =0,4,
=0,4, ![]() =2,3,
=2,3, ![]() =1,2,
=1,2, ![]() =0,4, т. е. показана неединственность минимума критерия оптимизации.
=0,4, т. е. показана неединственность минимума критерия оптимизации.
Проведена проверка генетического алгоритма на макроуровне моделирования мышечного сокращения, которая показала корректность реализованного подхода [2], на основании чего был сделан вывод о том, что расхождение значений кинетических параметров с эталонными (для модельного примера) может быть вызвано существованием областей неопределенности решения обратной задачи, когда кинетические измерения задаются внутри некоторого интервала точности, определяемого величиной погрешности измерений. В настоящее время производится разработка алгоритмов оценки указанных областей неопределенности.
Таким образом, получена математическая модель мышечного сокращения на молекулярном уровне, которая может служить основой для построения математических моделей сокращения мышцы на других, более высоких, уровнях исследования.
Список литературы:
1 , Охотников нелинейных биологических процессов. Переход к хаосу. − Екатеринбург: Изд-во Урал ун-та, 2008, – 154 с.
2 , , Губайдуллин вычисления при моделировании мышечного сокращения. // В мире научных открытий. Красноярск: НИЦ, 2011. №8 (20), С. 242-248.
УДК 547.94
, ,
ПОЛУЧЕНИЕ ГИБРИДНОЙ МОЛЕКУЛЫ
2,3:20,22-БИС-О-[2-(6-ГИДРОКСИ-2,5,7,8-ТЕТРАМЕТИЛХРОМАН-2-ИЛ) ЭТИЛИДЕН]-20-ГИДРОКСИЭКДИЗОНА
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Уфимский государственный нефтяной технический университет, г. Уфа
E-mail: *****@***ru
Экдистероиды – гормоны линьки, метаморфоза и диапаузы насекомых и ракообразных были впервые выделены из куколок непарного шелкопряда Bombyx mori в середине 1950-х годов. Спустя 10 лет зоогормоны были выделены из растений, причем в значительно более высоких концентрациях. К настоящему времени выделено и идентифицировано более 300 зоо - и фитоэкдистероидов.
Решающим событием, определившим интенсивное развитие области химии природных соединений, послужило открытие в
1966 г. веществ, близких по структуре α-экдизону, в растениях. В корневищах папоротника Polipodium vulgare содержание смеси экдистероидов достигало 2% от веса сухих корневищ. Эти вещества, выделенные из растений и по структуре близкие к α-экдизону получили название фитоэкдизонов или фитоэкдистероидов. Обнаружение гормонов насекомых в многократно больших количествах в растениях представляло практический интерес для эндокринологических исследований, поиска возможностей применения в медицине, а также для изучения химических трансформаций.
Характерными элементами структуры экдистероидов являются Δ7-6-кето-14α-группировка, цис-сочленение колец А и В, гидроксильные группы в стероидном скелете.
В качестве природного источника экдистероидов в работе используется растение Serratula coronata, а доступным природным экдистероидом является 20-гидроксиэкдизон.
Был синтезирован бис-конъюгат 2,3:20,22-Бис-О-[2-(-6-бензилокси-2,5,7,8-тетраметилхроман-2-ил)этилиден]-20-гидроксиэкдизон реакцией взаи-
модействия исходной молекулы 20-гидроксиэкдизона с 6-бензилокси2,5,7,8-
тетраметилхроман-2-ил) ацетальдегидом при катализе ТsOH и последующим
гидрогенолизе 6-бензильной функциональной группы в условиях (H2 /Pd-C).
Реакция взаимодействия 20-гидроксиэкдизона с хроманилальдегидом кислотно-
катализируемая.
Для целевого бисаддукта был снят масс-спектр MALDI TOF и зарегистрирован ион [М+Н]+. В спектрах ЯМР 1Н и 13С полученных гибридных соединений присутствуют сигналы всех атомов водорода и углерода экдистероидного и хроманильного фрагментов молекул.
УДК 579.66, 579.852.11, 577.15
, ,
ОЦЕНКА ВОЗМОЖНОСТИ ИСПОЛЬЗОВАНИЯ БАКТЕРИЙ BACILLUS SUBTILIS В КАЧЕСТВЕ ДЕСТРУКТОРОВ НОВЫХ БИОРАЗЛАГАЕМЫХ ПОЛИМЕРОВ
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования Башкирский государственный аграрный университет, г. Уфа
e-mail: *****@***ru
Несмотря на то, что в настоящее время масштабы производства биоразлагаемых полимеров крайне невысоки, их использование представляется перспективным в различных отраслях промышленности, например, при производстве различных упаковочных материалов и одноразовой посуды [1]. Одним из этапов создания биодеградируемых материалов является оценка способности полимера разрушаться под действием продуктов метаболизма редуцентов (бактерий и грибов). Эффективность и экспрессность скрининга данного свойства в большой степени определяется особенностями используемых в эксперименте микроорганизмов. Так как в состав биоразлагаемых полимеров наряду с синтетическими входят полимеры биогенные, такие как хитин, хитозан, целлюлоза, крахмал, пектин, коллаген, эластан и т. д., скорость разложения будет зависеть от активности и уровня синтеза гидролитических ферментов микроорганизмов-биодеструкторов. Данный факт, а также относительная небезопасность работы со смешанными и неидентифицированными культурами микроорганизмов, обуславливают целесообразность использования чистых культур продуцентов гидролаз в лабораторных экспериментах по оценке биодеградируемости сополимеров. В данной работе мы исследовали активность некоторых гидролитических ферментов трех эндофитных штаммов Bacillus subtilis 26Д, 11В и 49РН, выделенных из растений пшеницы. Активность ферментов определяли в культуральной жидкости, полученной после культивирования штаммов в жидких средах с добавлением коллоидного хитина, целлюлозы или пектина в качестве источников углерода. Отборы проб культуральной жидкости осуществляли через 12, 24, 36 и 48 часов культивирования. Активность хитиназы, целлюлазы и пектиназы, продуцируемых штаммами B. subtilis, определяли по реакции с динитросалициловой кислотой [2]. Активность протеаз определяли по реакции фермента с азоказеином (Sigma, США) [3]. В результате проведенных исследований нам не удалось обнаружить заметной активности для целого ряда гидролаз – хитиназы, целлюлазы и пектиназы, несмотря на наличие в среде культивирования штаммов субстратов и индукторов синтеза данных ферментов. В то же время все исследованные штаммы оказались способны продуцировать протеолитические ферменты в созданных условиях (рис. 1). Таким образом, было показано, что использование эндофитных бацилл в качестве биодеструкторов сополимеров на основе природных полисахаридов не представляется перспективным. Однако наличие высокой активности протеаз у штаммов открывает возможности их использования в качестве деструкторов биоразлагаемых полимеров на основе белковых молекул. В дальнейшей работе планируется провести выделение, идентификацию бактериальных изолятов из различных природных сред и скриниг активности их гидролаз для создания эффективной системы оценки биоразлагаемости новых полимеров на основе природных полисахаридов и белков.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 |




