Список литературы:
1 Strunz G. M. Stud. Nat. Prod. Chem. 2000, 24, 683.
2 Saadali B., Boriky D., Blaghen M., Vanhaelen M., Talbi M. Phytochemistry. 2001, 58, 1083.
3 Ee G. C.L., Lim C. M., Rahmani M., Shaari K., Bong C. F.J. Molecules. 2010, 15, 2398.
4 Silva R. V., Navickiene H. M.D., Kato M. J., Bolzani V. S., Meda C. I., Young M. C.M., Furlan M. Phytochemistry. 2002, 59, 521.
5 Reddy S. V., Srivinas P. V., Praveen B., Kishore K. H., Raju B. C., Murthy U. S., Rao J. M. Phytomedicine. 2004, 11, 697.
6 Rukachaisirikul T., Siriwattanakit P., Sukcharoenphol K., Wongvein C., Ruttanaweang P., Wongwattanavuch P., Suksamrarn A. J. Ethnopharmacol. 2004, 93, 173.
7 Likhitwitayawuid K., Ruangrungsi N., Lange G. L., Decicco C. P. Tetrahedron. 1987, 43, 3689.
8 Linday M. E. Practical Introduction to Microbiology. E and F. N. Spon Ltd., United Kingdom, 1962, Р. 177.
УДК547.811.78
,
РЕАКЦИИ 1, 3- ДИПОЛЯРНОГО ЦИКЛОПРИСОЕДИНЕНИЯ С - ФЕНИЛКАРБАМОИЛ -N-ФЕНИЛНИТРОНА С НЕКОТОРЫМИ ПОЛИЕНАМИ
Федеральное бюджетное государственное учреждение высшего профессионального образования Башкирский Государственный Университет,
г. Уфа
E-mail: *****@***ru
В настоящей работе мы изучили реакцию С-фенилкарбамоил-N-фенилнитрона I с полиенами, имеющими различное взаимное расположение и экранирование двойной связи. По реакционной способности I близок к С-бензоил-N-фенилнитрону, однако в отличие от последнего не вызывает дальнейшего превращения аддукта.
Среди ациклических полиенов Е-пиперилен II полностью присоединяет нитрон I за 15 мин, под действием Е, Е – 2, 4 - гексадиена III за это время I расходуется на 20%. Сопряженная винильная группа в IV за 3 часа образует аддукт ХII с количественным выходом. Менее активным является 2, 7 – диметилоктатриен – 1,3,7 V, который через 72 часа дает изоксазолидин ХIII с выходом 48 %.
Чрезвычайно пассивны Z, Z –диены с изолированными двойными связями: так 4,5-диметил-Z, Z-2,6-октадиен не вступает в реакцию с I. Винильная группа 2,5-диметил-1,5-гексадиена VI присоединяет нитрон с образованием моноизоксазолидина ХIV, этот олефин с изолированными кратными связями обнаруживает такую же диполярофильную активность, как и III.
Винилциклогексен VII, лимонен VIII присоединяют нитрон I исключительно по экзоциклической кратной связи. Внутрикольцевая Z– связь сохраняется. При продолжительности реакции 10-20 дней выход ХV, ХVI составляет 50%. Из VIII нами были получены изомерные изоксазолидины XVII и XVIIа. Норборнодиен IХ с исходным нитроном дает моно - ХVIII или бисаддукты ХIХ в зависимости от соотношения вводимых в реакцию 1,3-циклоприсединения нитрона и олефина.
Сопряженная Z– связь в циклопентадиене X при длительном контакте присоединяет I, образуя 2-окса-3-аза-бицикло [3,3,0] октен-6 XХ.
ИК и ПМР спектры полностью подтверждают строение синтезированных соединений. Для всех аддуктов X– XVII характерно наличие полос поглощения С-О группы изоксазолидинового кольца (1060, 1090 см-1), С=О группы (1690 см-1), амидной группы (3300, 3380 см-1) и другие [2].
В спектрах ПМР полученных соединений отчётливо проявляются сигналы протонов изоксазолидинового кольца, ароматических ядер, олефиновых протонов. Рассмотрение спектров ПМР аддуктов из Е-пиперилена X и гексадиена– 2, 4 XI показывает, что имеет место нормальное присоединение нитрона с образованием 5- замешённых изоксазолидинов [3]. В их спектрах ПМР сигналы протонов Н3 и Н5 наблюдаются в слабом поле; в случае обратной ориентации метиленовые протоны изоксазолидинового кольца резонировали бы в более слабом поле, а метиновые– в более сильных полях. Аналогично можно показать на основании спектров ПМР, что такая же ориентация нитрона имеет место и для аддуктов XII, XIII. Соотнесение сигналов протонов изоксазолидинового кольца было сделано с помощью ЯМДР.
Анализ спектров ПМР аддуктов из 5-метилгептатриена-1,3,6 XII и 2,7-диметилоктатриена-1,3,7 XIII, содержащих сопряжённую и изолированную двойные связи, показывает, что присоединение нитрона имеет место по сопряжённой связи с образованием 5-замещённых изоксазолидинов.
Спектры ПМР аддуктов из винилциклогексена и лимонена указывают на присоединение нитрона по экзоциклической двойной связи. Например, в спектре ПМР соединения XIV имеются сигналы протонов двух метиновых и метиленовых групп изоксазолидинового цикла.
Для лимонена характерно образование диастереомерных изоксазолидинов, различающихся расположением заместителя у С3-кольца. В спектре изомера XVIa сигналы протона Н3 и метиленовой группы проявляются в форме триплета и дублета, соответственно. В спектре изомера XVI сигналы этих же протонов наблюдаются в виде квартетов.
Рассмотрение спектра ПМР аддукта из циклопентадиена позволило установить ориентацию нитрона по отношению к двойной связи. В спектре сигнал протона Н5 изоксазолидинового кольца наблюдается в более слабом поле, чем сигнал такового в аддуктах XI- XV по-видимому, протон Н5 связан с углеродом при двойной связи.
УДК 541.124
, ,
Влияние текстурных характеристик частиц активированного угля на их способность усиливать массопереноса кислорода в системе газ-жидкость
Пермский национальный исследовательский политехнический университет,
г. Пермь
E-mail: kazakovbiotech@mail.ru
Химические и биотехнологические процессы в системах газ – жидкость достаточно часто протекают в диффузионном режиме, при этом их скорость определяется интенсивностью массопереноса малорастворимого в жидкости газа через границу раздела фаз. Так, массоперенос кислорода в системе газ (воздух) - жидкость (вода) может ограничивать скорость процессов биологического и химического окисления органических соединений [1]. Традиционные способы повышения интенсивности массопереноса кислорода, основанные на барботаже и (или) усилении перемешивания потоков жидкости и газа, достаточно энергозатратны, в связи с чем разработка новых подходов к интенсификации межфазного транспорта является сегодня актуальной задачей. В качестве одного из наиболее перспективных способов повышения скорости массопереноса в системах газ-жидкость в настоящее время рассматривается применение активаторов межфазного транспорта (АМТ) – тонкодисперсных твердых веществ, усиливающих массоперенос через пограничный слой жидкости. По литературным данным одним из наиболее эффективных АМТ является активированный уголь (АУ) [2]. Однако систематическая информация, позволяющая проследить взаимосвязь физико-химических характеристик АУ и его способности усиливать межфазный транспорт О2 в системах газ-жидкость, к настоящему времени отсутствует, что не позволяет проводить целенаправленный выбор образцов АУ для использования в качестве АМТ.
Целью настоящей работы является изучение влияния текстурных характеристик частиц АУ на их способность усиливать массоперенос О2 в системе газ (воздух) – жидкость (вода).
В качестве объёктов исследования были выбраны активированные угли производства (Россия) трёх марок (берёзовый активированный уголь марки БАУ-А; активированный уголь на каменноугольной основе марки АГ-3; активированный уголь на кокосовой основе марки КАУСОРБ), различающихся своими текстурными характеристиками (таблица 1).
Воздействие частиц АУ на процесс массоотдачи в жидкой фазе, как показано в работах [2], реализуется по «челночному» механизму, в соответствии с которым предполагается, что суспендированные частицы АУ в условиях перемешивания циркулируют между пограничным слоем и основным объёмом жидкости, перенося на своей развитой поверхности адсорбированные молекулы О2. Реализация «челночного» механизма усиления массопереноса связана с процессом циклической адсорбции-десорбции О2 на частицах АУ. В связи с этим можно предположить, что эффективность данного механизма будет определяться кинетикой сорбционных процессов с участием частиц. Как показано в работе [3], сорбция О2 частицами АУ происходит в две стадии: быстрое начальное поглощение, связанное с макропористой сорбцией, с последующим медленным достижением равновесия за счёт сорбции в микропорах. Таким образом, можно ожидать, что эффективный коэффициент диффузии О2 внутри частиц АУ (![]() ) будет возрастать с увеличением доли в нём удельного объёма макропор. Увеличение
) будет возрастать с увеличением доли в нём удельного объёма макропор. Увеличение ![]() , приводящее к повышению скорости сорбции и десорбции О2, должно повышать эффективность реализации «челночного» переноса. В соответствии с этими представлениями можно предполагать, что способность частиц АУ к усилению межфазного массопереноса будет возрастать с повышением в нём удельного объёма макропор. Исходя из данной зависимости, изучаемые образцы АУ по убыванию способности интенсифицировать транспорт О2 можно было бы расположить в следующий ряд: БАУ-А > АГ-3 > КАУСОРБ. Эта зависимость соответствует результатам проведённого эксперимента: коэффициент усиления массопереноса О2 (Е) под действием частиц АУ, действительно, повышается с увеличением в них удельного объёма макропор (таблица 1).
, приводящее к повышению скорости сорбции и десорбции О2, должно повышать эффективность реализации «челночного» переноса. В соответствии с этими представлениями можно предполагать, что способность частиц АУ к усилению межфазного массопереноса будет возрастать с повышением в нём удельного объёма макропор. Исходя из данной зависимости, изучаемые образцы АУ по убыванию способности интенсифицировать транспорт О2 можно было бы расположить в следующий ряд: БАУ-А > АГ-3 > КАУСОРБ. Эта зависимость соответствует результатам проведённого эксперимента: коэффициент усиления массопереноса О2 (Е) под действием частиц АУ, действительно, повышается с увеличением в них удельного объёма макропор (таблица 1).
Таблица 1 - Влияние текстурных характеристик образцов АУ на их способность усиливать массоперенос кислорода, выраженную величиной Е
Активированный уголь | S, м2/г |
| Распределение пор по размерам, % от суммарного объёма | Е | ||
макропоры (>50 нм) | мезопоры (2-50 нм) | микропоры (<2 нм) | ||||
БАУ-А | 561 | 1,66 | 80 | 6 | 14 | 3,7 |
АГ-3 | 1192 | 0,82 | 2 | 22 | 76 | 2,9 |
КАУСОРБ | 1315 | 0,73 | 2 | 13 | 85 | 2,0 |
Примечание: S – удельная поверхность; ![]() - удельный суммарный объем пор; Е - коэффициент усиления массопереноса О2.
- удельный суммарный объем пор; Е - коэффициент усиления массопереноса О2.
Список литературы:
1 Guillermo Q. Determining the effect of solid and liquid vectors on the gaseous interfacial area and oxygen transfer rates in two-phase partitioning bioreactors // Journal of Hazardous Materials. 2010. V. 175. P. .
2 Ruthiya K. C., van der Schaaf J., Kuster B. F.M., Schouten J. C. Mechanisms of physical and reaction enhancement of mass transfer in a gas inducing stirred slurry reactor // Chem. Eng. J. 2003. V. 96. P. 55-69.
3 Matsis V. M., Grigoropoulou H. P. Kinetics and equilibrium of dissolved oxygen adsorption on activated carbon // Chem. Eng. Sci. 2008. V. 63. P. 609-621.
547.914.2:547.89.2
1, 2
КОНЪЮГАТЫ 6-ГЕМИСУКЦИНАТА КАРКАСНОГО ПРОИЗВОДНОГО ХИНОПИМАРОВОЙ КИСЛОТЫ С АМИНОКИСЛОТАМИ
1ФГБОУ ВПО Башкирский госуниверситет, г. Уфа
2Институт органической химии УНЦ РАН, г. Уфа,
e-mail: vafina@anrb.ru
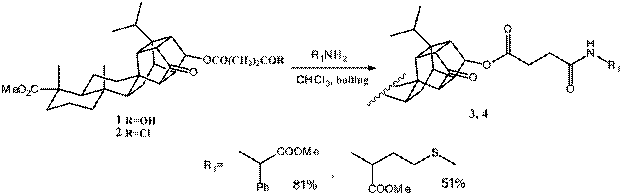
Широкая доступность смоляных кислот – основного компонента сосновой живицы, а также большой синтетический и фармакологический потенциал этих кислот представляют несомненный интерес для химиков-органиков. Значительный интерес представляют аддукты левопимаровой кислоты с хинонами, обладающие противораковой, противовоспалительной, кардиостимулирующей активностью [1]. В связи с этим, синтез новых производных левопимаровой кислоты становится перспективным. Конъюгаты 3, 4 получены по реакции хлорангидрида 6-гемисукцината каркасного производного хинопимаровой кислоты 2, синтезированного действием оксалил хлорида на 6-гемисукцинат 1, с метиловыми эфирами L-β-фенил-α-аланина и метионина в среде безводного хлороформа с выходами 51 и 81% соответственно. Структура соединений 3, 4 доказана на основании спектральных данных.
Список литературы:
1 , , . «Синтез и превращения диеновых аддуктов смоляных кислот» // Химия и компьютерное моделирование. Бутлеровские сообщения, 2004, 5(2), 9.
Работа выполнена при финансовой поддержке гранта Президента Российской Федерации для ведущих научных школ № НШ-7014.2012.3, программы фундаментальных исследований Президиума РАН №8П и федеральной целевой программы «Научные и научно-педагогические кадры инновационной России» на годы – гос. контракт № 14.740.11.0367
УДК 547.972
1,2, 2, 1
СИНТЕЗ 3-О-ЭТИЛОВОГО ЭФИРА
2,3,6,8,5’-ПЕНТАБРОМКВЕРЦЕТИНА
1Башкирский государственный университет, г. Уфа
2Институт органической химии УНЦ РАН, г. Уфа
E-mail: *****@***ru
Кверцетин – биологически активное вещество из группы флавоноидов, которое входит в группу витамина Р. Обладает антиоксидантным, противоопухолевым, гиполипидемическим, иммуномоделирующим эффектом, улучшает клеточный метаболизм, укрепляет сосудистую стенку и снижает ее проницаемость, выявляет антигистаминное действие.
Бромпроизводные кверцетина представляют интерес в качестве новых биологически активных веществ и исходных субстратов для введения новых функциональных групп в ароматическое ядро.
Ранее были изучены реакции кверцетина с бромом в различных условиях с получением 6-моно- и 6,8-дибромпроизводных: бромирование КВ в 50% серной кислотой бромом, выделяемым in situ, при взаимодействии KBr с 30% H2O2, радикальное бромирование N-бромсукцинимидом, электрофильное бромирование кверцетина в диоксане и в уксусной кислоте. Увеличение количества реагента до 3.5 ммоль на 1 ммоль кверцетина, времени реакции и нагревание приводило к увеличению чистоты 6,8-дибромкверцетина и выхода до 82%. Структуры всех полученных соединений подтверждены спектральными методами.
Нами изучена реакция кверцетина с бромом в этиловом спирте. Взаимодействием кверцетина 1 с тремя эквивалентами брома в абсолютном EtOH в присутствии молекулярных сит 4 À при 0-5 °С с последующим выдерживанием реакционной смеси при 20-22 °С в течение 22-24 ч получен 6,8,5'-трибромкверцетин 2, с пятью эквивалентами брома – 3-О-этиловый эфир 2,3,6,8,5’-пентабромдигидрокверцетин 3. Данное соединение получено нами впервые.
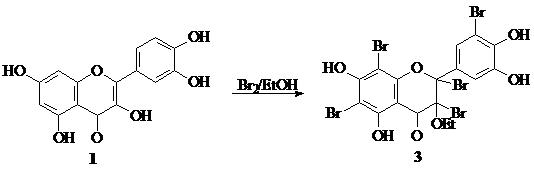
Работа выполнена при поддержке НШ - 7014.2012.3
УДК 547.413
, ,
Исследование влияния ультразвука на синтез акридонуксусной и a-акридонпропионовой кислот и их эфиров
Уфимский государственный нефтяной технический университет, г. Уфа
E-mail: *****@***net
Одной из групп иммуномодулирующих средств цитокининового ряда являются интерфероны, обладающие противовирусной и противоопухолевой активностью. Некоторые производные акридинов проявляют противоопухолевые свойства, в частности, путем ингибирования фермента теломеразы. В настоящее время препараты на основе 9-оксоакридин-10-уксусной кислоты и ее солей предлагаются для лечения и профилактики широкого круга заболеваний в онкологии и гинекологии.
С целью оптимизации условий синтеза и поиска новых физиологически активных соединений, нами исследованы новые подходы к синтезу акридонуксусной, α-акридонпропионовой кислот и их эфиров, а так же изучена возможность интенсификации реакций, лежащих в основе их синтеза, с помощью ультразвука.
Установлено, что при взаимодействии пропилового эфира хлоруксусной (1) и бутилового эфира α-бромпропионовой (2) кислот с акридоном металлированным натрием при температуре 100 оС в ДМСО в течение 6 часов образуются соответствующие алкиловые эфиры акридонуксусной (3) и α-акридонпропионовой (4) кислот с выходами 90% и 93%, соответственно.

При проведении синтеза в ультразвуковом поле необходим отвод тепла, поэтому реакцию осуществляли в ледяной бане. В этих условиях синтез продуктов (3) и (4) завершается через 3.5 часа с выходами 95% и 96%, соответственно.
Кислотно-катализируемый гидролиз полученных эфиров (3, 4) приводит к образованию акридонуксусной (5) и α-акридонпропионовой (6) кислот с выходами 93% и 95%, соответственно.
Строение и чистота полученных соединений подтверждены данными ЯМР 1H, 13C - спектроскопии и хроматомасс-спектрометрии.
УДК 615.322
, ,
НЕКОТОРЫЕ ХИМИЧЕСКИЕ ТРАНСФОРМАЦИИ ХРИЗОФЕНОЛА С
ФГБОУ Башкирский государственный университет, г. Уфа
Институт органической химии УНЦ РАН, г. Уфа
E-mail: *****@***ru
Широкое распространение флавоноидов в растительных организмах и разнообразное биологическое действие обусловливает интерес исследователей к этому классу соединений. Основное внимание ученых направлено на изучение группового состава фенольных соединений различных растений, в то время как публикации по химическим свойствам флавоноидов весьма малочисленны. Флавоноиды относятся к веществам с высокой реакционной способностью, имеющих несколько разноплановых центров: ароматические кольца А и В, гетероциклическое кольцо С и большое число гидроксильных групп (обычно от 3 до 5-6) [1]. В связи с этим становится актуальным поиск путей направленной модификации флавоноидов для изменения или усиления имеющегося биологического действия.
Было показано, что, попадая в организм человека, природные полифенолы претерпевают биодеградацию ферментами ЖКТ, превращаясь в метаболиты. Более того, содержание данных метаболитов в крови и лимфе очень мало. Однако имеются данные о превращении некоторых их ацилпроизводных после прохождения биологических барьеров в исходные флавоноиды [1-4]. Поэтому становится актуальным синтез прекурсоров природных полифенолов с целью увеличения их биодоступности для организма, а именно повышение устойчивости к действию ферментов, проникающей способности и растворимости в биологических жидкостях. Данная задача решается путем введения в молекулу флавоноида сложноэфирных групп, в частности синтезированы полифенолы содержащие остатки аминокислот и другие ацильные группы.
Использование в качестве ацилирующего агента хлорангидрида жирной кислоты позволяет получить сложные эфиры хризофенола С с хорошим выходом. Полученные сложные эфиры разделяли колоночной хроматографией (SiO2, элюэнт этилацетат – хлороформ 3:7). Как оказалось, в случае линолевой кислоты ацилирование условиях протекает с образованием двух продуктов. Ацилирование во всех случаях не затрагивает гидроксил в 5 положении, по-видимому, в связи с тем, что он связан с карбонильной группой при С4 прочной водородной связью и идет неселективно, хотя для олеиновой кислоты получен единственный продукт 6,4’–диолеат с удовлетворительным выходом (36%). Образование сложных эфиров подтверждено ИК - спектрами (сигнал в области см-1) и данными ЯМР С13 – (сигнал в области 170 м. д.) COOR.

Хризофенол С в силу своей малой растворимости в воде и липидах обладает низкой биодоступностью и способностью проникать через трансдермальные барьеры. Кроме этого известно, что метаболизм флавоноидов осуществляется через стадию этерификации жирными или желчными кислотами и последующим эмульгированием в липидах.
Для сложных эфиров хризофенола и жирных кислот была определена их растворимость в липидах, а также тип образуемой ими эмульсии. Оказалось, что сложные эфиры хризофенола и ненасыщенных жирных кислот хорошо растворимы в масле, бензоле и образуют прямые или обратные эмульсии в зависимости от порядка смешения компонентов. Эфиры стеариновой кислоты практически не растворимы в масле и образуют малоустойчивые эмульсии обратного типа. Результаты измерений сравнивались с контролем. Контролем являлась эмульсионная смесь водной и масляной фазы в соотношении 1:3 без добавления эмульгатора: В результате было установлено, что устойчивость эмульсии эфиров хризофенола С зависит от степени ненасыщенности жирной кислоты. Эфиры хризофенола и олеиновой кислоты образуют более устойчивые эмульсии, по сравнению с эфирами линолевой кислоты.
Список литературы:
1 Manson, M. M.; Farmer, P. B.; Gescher, A.; Steward, W. P. Innovative agents in cancer prevention. Recent Results Cancer Res. 2005, 166, 257-275.
2 Kundu, J. K.; Surh, Y. J. Molecular basis of chemoprevention by resveratrol: NF-kappaB and AP-1 as potential targets. Mutat. Res. 2004, 555, 65-80.
3 Bode, A. M.; Dong, Z. Cancer prevention by food factors through targeting signal transduction pathways. Nutrition 2004, 20, 89-94.
4 Aggarwal, B. B.; Shishodia, S. Molecular targets of dietary agents for prevention and therapy of cancer. Biochem. Pharmacol. 2006, 71, .
УДК 579.66
, ,
ДЕСТРУКЦИЯ 2,4-ДИХЛОРФЕНОКСИУКСУСНОЙ КИСЛОТЫ МИКРООРГАНИЗМАМИ
Федеральное государственное бюджетное учреждение науки Институт биологии Уфимского научного центра РАН, г. Уфа
E-mail: *****@***ru
На сегодняшний день в результате хозяйственной деятельности в биосфере циркулирует большое число различных чужеродных для человека и животных соединений, многие из которых имеют исключительно высокую токсичность. Из органических соединений - загрязнителей выделены "приоритетные", то есть те из них, которые представляют наибольшую опасность для человека сейчас и в будущем. Это прежде всего хлорсодержащие органические соединения, в том числе пестициды, используемые для борьбы с болезнями и вредителями сельского хозяйства. Одним из наиболее широко применяемых галогенсодержащих ароматических соединений является 2,4-дихлорфеноксиуксусная кислота (2,4-Д), на основе которой создан ряд гербицидов для уничтожения сорной растительности [1].
В настоящее время для переработки пестицидов предлагаются главным образом физические и химические методы. Однако использование их требует значительных затрат энергии и экономически невыгодно, а самое главное - они не решают проблем экологической безопасности. Преимущество применения биологических методов дезактивации пестицидов объясняется тем, что микроорганизмы минерализуют эти соединения и другие продукты органического синтеза в естественном цикле круговорота веществ, не оказывая отрицательного влияния на экосистему. Поэтому скрининг и идентификация штаммов микроорганизмов-деструкторов хлорсодержащих веществ является актуальной задачей.
Целью данной работы был поиск и выделение микроорганизмов, способных разлагать 2,4-Д, с перспективой их дальнейшего использования для биоремедиации окружающей среды.
Выделение штаммов-деструкторов из образцов техногенно загрязненной почвы с территории промышленного предприятия осуществлялось методом накопительных культур. Навески почвы помещали в колбы со 100 мл питательной среды Раймонда [2] без пептона, добавив 1 мл 2,4-Д в качестве единственного источника углерода. Культивирование происходило при температуре 30 °С в лабораторном термостатируемом встряхивателе П-5.10–Э5960 при скорости вращения 160 об/мин. Определение титра клеток в инокуляте проводили путем нанесения культуральной жидкости на агаризованную мясо-пептонную среду для получения отдельных колоний с дальнейшим подсчетом их числа. Далее инокулят высевали на твердую питательную среду Раймонда без пептона, применяя в качестве субстрата 2,4-дихлорфеноксиуксусную кислоту.
Рост титра на 5 сутки эксперимента составил два порядка. В дальнейшем планируются работы по идентификации и использованию выделенных штаммов микроорганизмов для утилизации иных хлорсодержащих соединений.
Список литературы:
1 , , Кузмичева пестицидов и агрохимикатов, разрешенных к применению в Российской Федерации // Защита и карантин растений.-1998.-№ 5.-С.119-125.
2 Raymond R. L. Microbial oxidation of n-paraffinic hydrocarbons // Develop. Industr. Microbiol.-1961.-№ 1.-P.23-32.
УДК 573.6.086.83
, ,
МИКРООРГАНИЗМЫ, ДЕГРАДИРУЮЩИЕ УГЛЕВОДОРОДЫ НЕФТИ ПРИ НИЗКИХ ПОЛОЖИТЕЛЬНЫХ ТЕМПЕРАТУРАХ
Федеральное государственное бюджетное учреждение науки
Институт биологии Уфимского научного центра РАН, г. Уфа
E-mail: biolab316@yandex.ru
Попадание нефти и её компонентов в окружающую среду вызывает изменение физических, химических и биологических свойств и характеристик природной среды обитания, нарушает ход естественных биохимических процессов. При трансформации углеводородов нефти могут образоваться стойкие к микробиологическому расщеплению и ещё более токсичные соединения, обладающие канцерогенными и мутагенными свойствами.
Микробиологические методы являются неотъемлемым компонентом современной биотехнологии удаления из почвы и воды нефти и нефтепродуктов. Биоремедиация обеспечивает экономически выгодную, высокоспецифичную очистку, приводящую к уменьшению концентрации, как отдельного загрязнителя, так и смеси поллютантов. Препятствиями в достижении этой цели являются низкая температура, повышенная концентрация соли, низкое содержание питательных веществ, отсутствие или низкая деструкционная активность природных микробных популяций. Эти особенности характерны для Западной Сибири и северных регионов европейской части нашей страны, т. е. для тех районов, где расположено большинство месторождений нефти России и где чаще всего происходит загрязнение нефтью наземных и водных экосистем.
Процесс естественного восстановления загрязненной окружающей среды является очень длительным. Ауторемедиация нефтезагрязненных почв при уровне загрязнения 5 г/кг длится от 2 до 30 лет и более. В северных широтах скорость этих процессов еще ниже [1]. Поэтому внесение эффективных микроорганизмов-деструкторов в почву совершенно необходимо в северных районах, где тёплый период года непродолжителен и природная микрофлора не успевает адаптироваться к изменяющимся условиям окружающей среды. Работ, посвященных селекции микроорганизмов, способных к деструкции нефти и нефтепродуктов при низких положительных температурах, мало. В связи с этим поиск и исследование психротолерантных микроорганизмов-деструкторов нефтяных углеводородов является актуальным.
Целью настоящей работы был скрининг и идентификация углеводородокисляющих микроорганизмов из техногенно загрязненной почвы Крайнего Севера и отбор культур, способных эффективно утилизировать нефтяные углеводороды при температуре 4-6оС.
в процессе работы выделены и идентифицированы 8 бактериальных изолятов, разлагавших нефть в жидкой среде в условиях низкой положительной температуры. Среди них оказались представители рр. Pseudomonas, Rhodococcus и Acinetobacter, что согласуется с данными литературы [2, 3, 4, 5, 6, 7]. Исследованные культуры различались по способности утилизировать индивидуальные углеводороды нефти - декан, толуол и β-метилнафталин в качестве единственного источника углерода и энергии при 4-6оС.
Изолят Pseudomonas sp.1.1 демонстрировал очень высокую активность в отношении декана (71,3%), которая намного превышает показатели других штаммов (25,5 - 48%).
Степень деструкции толуола изучаемыми культурами микроорганизмов составляла 72,3 – 93,4%.
β-метилнафталин лучше всего деградировал под действием Pseudomonas sp.,7%). Способность к разложению этого углеводорода у штамма Rhodococcus sp. 3.2. составляет 14,0%. Другие штаммы утилизируют субстрат в пределах 20,0 - 33,3%.
Таким образом, выделенные штаммы могут активно развиваться при низких положительных температурах, что делает перспективным их использование для ликвидации последствий нефтяных загрязнений почв в регионах с активной нефтедобычей и коротким весенне-летним периодом.
Список литературы:
1 , , // Восстановление нефтезагрязнённых почвенных экосистем.- М.: Наука, 1988.- С. 140-159.
2 Коронелли и методы интенсификации биологического разрушения углеводородов в окружающей среде // Прикладная биохимия и микробиология.-1996.-№ 6.-С.579-585.
3 , , и др. Создание и применение жидкого препарата на основе ассоциации нефтеокисляющих бактерий // Прикладная биохимия и микробиология.-2000.-№ 6.-С.666-671.
4 , , и др. Биодеградация нефтепродуктов штаммами-деструкторами и их ассоциациями в жидкой среде // Прикладная биохимия и микробиология.-2001.-№ 5.-С.542-548.
5 Hanson K. G., Nigan A., Kapadia M., Desai A. J. News & Notes: Bioremediation of Crude Oil Contamination with Acinetobacter sp. A3 // Curr. Microbiol. Issue.-1997.-№ 3.-P.191-193.
6 Van Hamme J. D., Ward O. P. Physical and metabolic interactions of Pseudomonas sp. strain JA5-B45 and Rhodococcus sp. strain F9-D79 during growth on crude oil and effect of a chemical surfactant on them // Appl. Environ. Microbiol.- 2001.-№ 10.-P..
7 Margesin R., Labbe D., Schinner F., et al. Characterization of hydrocarbon-degrading microbial populations in contaminated and pristine alpine soils // Appl. Environ. Microbiol.-2003.-№ 3.-P..
УДК 54.057
, ,
СИНТЕЗ ЖИДКОКРИСТАЛЛИЧЕСКИХ ПОЛИМЕРОВ НА ОСНОВЕ СИНДИОТАКТИЧЕСКОГО 1,2-ПОЛИБУТАДИЕНА

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 |




