![]()
![]()
или
![]()
где ![]() радиус действия поля
радиус действия поля ![]() а
а ![]() порядок его величины в основной области его существования. При выполнении первого условия рассматриваемое приближение применимо при всех скоростях. Из второго же условия видно, что оно во всяком случае применимо для достаточно быстрых частиц.
порядок его величины в основной области его существования. При выполнении первого условия рассматриваемое приближение применимо при всех скоростях. Из второго же условия видно, что оно во всяком случае применимо для достаточно быстрых частиц.
Ищем волновую функцию в виде ![]() где
где ![]() соответствует падающей частице с волновым вектором
соответствует падающей частице с волновым вектором ![]() . Имеем:
. Имеем:
![]()
Выбрав рассеивающий центр в качестве начала координат, введем радиус - вектор ![]() в точку наблюдения
в точку наблюдения ![]() и обозначим посредством
и обозначим посредством ![]() единичный вектор в направлении
единичный вектор в направлении ![]() . Пусть радиус-вектор элемента объема
. Пусть радиус-вектор элемента объема ![]() есть
есть ![]() , тогда
, тогда ![]() На больших расстояниях от центра
На больших расстояниях от центра ![]() так что
так что
![]()
Подставляя это, получим следующее асимптотическое выражение для ![]()
![]()
(где ![]() есть волновой вектор частицы после рассеяния). Сравнивая с определением амплитуды рассеяния, получим для нее выражение
есть волновой вектор частицы после рассеяния). Сравнивая с определением амплитуды рассеяния, получим для нее выражение
![]() ,
,
в котором мы произвели переобозначение переменных интегрирования и ввели вектор
![]()
с абсолютной величиной
![]()
![]()
где ![]() - угол между
- угол между ![]() и
и ![]() т. е. угол рассеяния.
т. е. угол рассеяния.
Наконец, возводя в квадрат модуль амплитуды рассеяния, получим следующую формулу для эффективного сечения рассеяния в элемент телесного угла ![]()
![]() .
.
Мы видим, что рассеяние с изменением импульса на ![]() определяется квадратом модуля соответствующей компоненты Фурье поля
определяется квадратом модуля соответствующей компоненты Фурье поля ![]() . Формула была впервые получена М. Борном (1926); соответствующее приближение в теории столкновений часто называют борновском приближением.
. Формула была впервые получена М. Борном (1926); соответствующее приближение в теории столкновений часто называют борновском приближением.
Рассеяние в кулоновском поле представляет особый интерес с точки зрения физических применений. Оно интересно также и в том отношении, что для этого случая квантомеханическая задача о столкновениях может быть решена до конца точно.
При наличии выделенного направления (в данном случае – направление падающей частицы) уравнение Шредингера в кулоновском поле удобно решать в параболических координатах ![]() . Задача о рассеянии частицы в центральном поле обладает аксиальной симметрией. Поэтому волновая функция
. Задача о рассеянии частицы в центральном поле обладает аксиальной симметрией. Поэтому волновая функция ![]() не зависит от угла
не зависит от угла ![]() . Частное решение уравнения Шредингера пишем в виде:
. Частное решение уравнения Шредингера пишем в виде:
![]()
Таким образом получаем для эффективного сечения рассеяния ![]() формулу
формулу
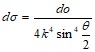 ,
,
или в обычных единицах
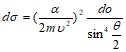
(мы ввели скорость частицы ![]() ). Эта формула совпадает с известной формулой Резерфорда, к которой приводит классическая механика. Таким образом для рассеяния в кулоновском поле квантовая и классическая механика дает одинаковый результат.
). Эта формула совпадает с известной формулой Резерфорда, к которой приводит классическая механика. Таким образом для рассеяния в кулоновском поле квантовая и классическая механика дает одинаковый результат.
Тема: Молекулы. Гетерополярная и гомеополярная связи.
Химические свойства элементов, так же как и их оптические спектры, определяются в основном электронами внешнего слоя, который может содержать только s и p –оболочками. Поэтому закономерности, лежащие в основе оптической периодичности (например, повторяемость расщепления термов а атомных спектрах и т. д.), должны служить также основной и в построении теории периодически повторяющихся химических свойств элементов. Кстати, заметим, что последние свойства проявляются не у изолированного атома, а при наличии нескольких атомов, образующих молекулу.
Электроны внутренних слоев почти не оказывают влияния на химические процессы, так как они гораздо сильнее связаны с ядром, чем внешние. Поэтому энергия, выделяемая при химических реакциях, гораздо меньше, чем энергия связи электронов внутренних слоев.
Следует различать два основных типа химической связи: ионная (гетерополярная) и атомная (гомеополярная или спиновая). Рассмотрим более подробно каждые из этих типов химической связи. Известно, что неорганические соли построены из положительных и отрицательных ионов, между которыми имеет место электрическое (кулоновское) притяжение, удерживающее атомы в молекуле.
Соединения этого типа называются ионными, а соответствующие молекулы – гетерополярными. Как известно, ионы могут быть двоякого рода: положительные и отрицательные. Знак заряда иона зависит, с одной стороны, от потенциала ионизации, т. е. от той энергии, которую необходимо затратить, чтобы удалить внешний электрон, а с другой – от степени сродства к электрону, т. е. от той энергии, с которой нейтральный атом может удерживать дополнительный электрон на внешнем слое.
Атомы щелочных и щелочноземельных металлов легко отдают свой валентный электрон другому атому (потенциал ионизации для них наименьший), превращаясь при этом в положительный ион (например, в ион ![]()
![]() ).
).
Наоборот, атомы VII группы (галогены), а также VI группы (кислород и др.) обладают наибольшим по сравнению с другими элементами значением потенциала сродства к электрону.
Энергия сродства к электрону у натрия практически, так же как и у инертных газов, равна нулю.
Первая попытка построить теорию ионной связи принадлежит Косселю (1916), исходившему из представлений боровской теории атома.
В основу его теории была положена замкнутость восьмиэлектронных слоев атомов инертных газов, не обладающих никакой валентностью.
Наряду с ионными соединениями существуют молекулы, которые образуется не из ионов, а непосредственно из нейтральных атомов. Простейшей из них является молекула ![]()
![]() . Подобные молекулы получили название атомных или гомеополярных.
. Подобные молекулы получили название атомных или гомеополярных.
Заметим, что образование гомеополярных молекул нельзя понять даже качественно на основе классических или полуклассических (боровских) представлений. Эти теории могли подойти к объяснению молекулярных соединений только в том случае, когда в основе их образования лежат силы электростатического происхождения, например гетерополярные молекулы.
Теория простейшей гомеополярной молекулы водорода впервые была построена Гайтлером и Лондоном (1927) с помощью введения квантовых обменных сил.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 |



